Anatomic peculiarities of the optic nerve disc
Kasyumova M.S.
Kasyumova M.S.
Optic nerve disc on it’s tissue architecture belongs to amyelinic nerve structures and is conditionally divided into 3 parts: surface lamina, prelaminar and laminar parts. Surface lamina is blood supplied from central retinal arteria. Prelaminar part – at the expence of capillars of peripapilar chorioidal network. Laminar and retrolaminar parts of the disc are blood supplied from branches of Cinn–Galer circle with branches of peripapilar chorioidal vessels and partly from branches of posterior short ciliar vessels. There is a big variability in the embranchment of posterior short ciliar vessels both in their quantity and in topography of entering the posterior pole of the eye. Blood outflow is carried out by central retinal vein and to the peripapilar chorioidal veins which carry the blood to the venae varticosae. Ultrastructure of disc vessels’ walls turned out to be similar to these of retinal and central nerve system capillars.
Сосудистая патология зрительного нерва (ЗН) и на сегодняшний день остается одной из наименее изученных проблем офтальмологии в связи со сложностью его структурно–функционального строения [1].
Клинико–морфологические, электрофизиологические исследования значительно расширили наши представления об анатомии диска зрительного нерва (ДЗН), но благодаря современным неинвазивным диагностическим технологиям стали возможными изучение более тонких структур и прижизненная оценка изменений в них на более высоком уровне [8,9]. Однако в связи с этим стали появляться новые данные, не согласующиеся с прежними представлениями. В этой статье предпринята попытка создания целостной картины строения ДЗН с учетом современных изысканий.
Диском зрительного нерва называют интраокулярную часть зрительного нерва, который образуется аксонами оптикоганглионарных невроцитов [2,3]. Поскольку слой нервных волокон и вся сетчатка по мере приближения к нему утолщаются, это место несколько выступает внутрь глаза в виде сосочка [7]. Общее количество аксонов ганглиозных клеток в ЗН от 564 776 до 1 200 000 [10], но с возрастом оно уменьшается. Топография их отличается строгой закономерностью. От макулярной области сетчатки в средне–височную часть ДЗН идет короткий, но плотный пучок аксонов, который оттесняет дуговые волокна, исходящие от верхне– и нижневисочных квадрантов сетчатки, в соответствующие его сегменты [7]. При этом в самом центре папилло–макулярного пучка два аксона несут информацию от одной колбочки, расположенной в фовеольной зоне 2°. В периферических участках ЗН каждый аксон несет информацию от значительно большего количества фоторецепторов. На периферии сетчатки соотношение фоторецепторов и ганглиозных клеток составляет 1000:1 [7,10]. Радиальные волокна, отходящие от верхне–и нижненосовых квадрантов сетчатки, занимают в ДЗН сегменты той же пространственной ориентации. Затем собранные в нем волокна делают дугообразный загиб (на 90°) и в виде обособленных пучков формируют начальную часть ЗН.
По данным ряда авторов [1,2,3,5,6,7,11], ДЗН имеет длину около 1 мм, диаметр 1,75–2,0 мм, площадь – 2–3 мм. Он локализуется медиальнее заднего полюса глаза на 2,5–4 мм и на 0,5–1 мм книзу от него [2,7], или на 15° кнутри и на 3° кверху от заднего полюса глаза [3,5]. Соответственно проекции ДЗН в пространство, в височной половине поля зрения каждого глаза имеется слепое пятно (физиологическая скотома).
Более точную характеристику биометрических показателей ДЗН получили при использовании трехмерной оптической томографии и ультразвукового сканирования [9]. При УЗ–сканировании ширина продольного УЗ–сечения внутриглазной части ДЗН составляет 1,85±0,05 мм; ширина ретробульбарной части ЗН в 5 мм от ДЗН – 3,45±0,15 мм; на расстоянии в 20 мм – 5,0±0,25 мм. По данным трехмерной оптической томографии горизонтальный диаметр ДЗН – 1,826±0,03 мм; вертикальный диаметр – 1,772±0,04 мм; площадь ДЗН – 2,522±0,06 мм2; площадь экскавации – 0,727±0,05 мм2; площадь ободочной рамки – 1,801±0,03 мм2; глубина экскавации – 0,531±0,05 мм; высота – 0,662±0,08 мм; объем экскавации – 0,622±0,06 мм3.
Область ДЗН условно делится на 4 зоны: 1 – непосредственно диск (диаметр – 1,5 мм); 2 – юкстапапиллярная (диаметр около 1,7 мм); 3 – парапапиллярная (диаметр – 2,1 мм); 4 – перипапиллярная (диаметр – 3,1 мм) [5].
Внешний вид ДЗН и размер его физиологической экскавации зависят от размера склерального канала и угла, под которым этот канал расположен по отношению к глазу. Четкость границ ДЗН определяется углом входа ЗН в склеру. Если ЗН входит в склеру под острым углом, то пигментный эпителий сетчатки оканчивается впереди края канала, образуя полукольцо хориоидеи и склеры. Если угол превышает 90°, то один край диска кажется крутым, а противоположный – пологим. Если сосудистая оболочка отстоит от края ЗН, он окружен склеральным полукольцом. Иногда край диска имеет черную окантовку из–за скопления меланина [3].
По данным некоторых авторов [2,6,7,11], по тканевой структуре ДЗН относится к так называемым безмякотным нервным волокнам. В нем отсутствуют олигодендроглия и микроглия. Зато ДЗН богато снабжен сосудами и опорными элементами. Нейроглия ДЗН состоит из астроцитов, обладающих длинными отростками, которые окружают все пучки нервных волокон и, проникая в них, сопровождают каждое волоконце. Они принимают также участие в формировании решетчатой опорной структуры ДЗН и отделяют его от соседних тканей. Граница между безмякотной и мякотной частями ЗН совпадает с наружной поверхностью решетчатой пластинки, т.е. находится еще внутри глаза [4,5].
Части ДЗН
Разные авторы [1,2,4,6,7,11] по–разному называют части безмякотного отдела ЗН, но, в сущности, они соответствуют друг другу и отражают особенности ангиоархитектоники зрительного нерва. ДЗН делится на 3 части, и сюда же можно отнести и 4–ую часть зрительного нерва, находящуюся непосредственно за решетчатой пластинкой.
1. Поверхностная пластинка ДЗН (его ретинальная часть), представляющая из себя слой поверхностных нервных волокон в виде кольца. Височная половина ниже носовой, поскольку в ней тоньше слой нервных волокон. Височные волокна образуют в середине ДЗН углубление либо в виде воронки (именуется сосудистой), либо в форме котла (физиологическая экскавация). Здесь проходят сосуды сетчатки, которые покрыты тонким чехлом из глии, образующие на дне физиологической экскавации соединительнотканный тяж. От стекловидного тела поверхностная часть ДЗН отделена несплошной глиальной мембраной [7,11].
2. Хориоидальная или преламинарная часть ДЗН. Она находится на уровне собственно сосудистой оболочки и состоит из упомянутых выше пучков нервных волокон, покрытых астроглиальной тканью с поперечными ответвлениями. Они образуют решетчатую структуру. Базальная пластинка хориоидеи имеет в этом месте округлой формы отверстие, которое каналом соединено с решетчатой пластинкой склеры. Длина этого хориосклерального канала 0,5 мм, диаметр внутреннего отверстия около 1,5 мм, наружного – несколько больше. Этот слой ДЗН снабжен густой сетью капилляров. А.П. Нестеров приводит несколько типов хориосклерального канала ДЗН: расширяющийся или суживающийся кзади; расширяющийся или суживающийся в средней части; цилиндрический и косой. Эти особенности могут объяснить некоторые вопросы патогенеза развития сосудистых нарушений в ДЗН [6,7].
3. Склеральная или ламинарная часть ДЗН. Она представлена волокнами, заключенными в канальцы решетчатой пластинки. Решетчатая пластинка делится на переднюю (хориоидальную) и заднюю (склеральную) части. В решетчатой пластинке имеется сеть соединительнотканных (коллагеновых) перекладин – трабекул, образующих при пересечении септы полигональной формы, через которые проходят пучки нервных волокон. Общее число пучков достигает 400. Средняя толщина трабекул в склеральной части решетчатой пластинки около 17 мкм. В каждой трабекуле заключен капилляр диаметром 5–10 мкм. Источником происхождения этих капилляров в хориоидальной части трабекул являются терминальные артериолы, отходящие от перипапиллярной хориоидеи или от круга Цинна–Галлера. Трабекулы задней части решетчатой пластинки содержат капилляры, происходящие из круга Цинна–Галлера. Центральная артерия сетчатки в кровоснабжении решетчатой пластинки не участвует [4,11,12].
4. Постламинарная часть ЗН (ретроламинарная) представляет собой часть ЗН примыкающую к решетчатой пластинке. Она в 2 раза толще ДЗН и диаметр ее составляет 3–4 мм [1,12].
Кровоснабжение ДЗН
Кровоснабжение ДЗН описано в работах многих авторов [1,2,4,6,7,9,11,12] и обобщенно может быть представлено следующим образом. Поверхностный слой нервных волокон ДЗН получает питание частично из центральной артерии сетчатки (ЦАС) или, точнее, из ветвей артериол сетчатки, проходящих в перипапиллярной области. Темпоральный сектор этого слоя снабжается веточками из хориоидальных сосудов.
Преламинарная часть снабжается кровью из капилляров перипапиллярных хориоидальных сосудов. Хотя эти сосуды не относятся к сосудам концевого типа, анастомозы между ними недостаточные и кровоснабжение носит сегментарный характер. Капилляры проходят в указанных выше глиальных перегородках, содержащих астроциты и окружающих пучки нервных волокон. Наиболее значительно кровоснабжается зона папилломакулярного пучка. Считается, что здесь принимают участие также веточки задних циллиарных артерий, идущих от решетчатой пластинки [4,11,12].
Ламинарная часть ДЗН получает питание из терминальных артериол перипапиллярной хориоидеи или от круга Цинна–Галлера. Необходимо отметить отсутствие достаточной информации в литературе об анатомо–функциональных особенностях этой сосудистой сети. При невыраженности или отсутствии данного круга питание задней части решетчатой пластинки происходит из системы задних коротких цилиарных артерий (ЗКЦА).
Ретроламинарная часть ДЗН получает кровь в основном из ветвей сосудистого сплетения мягкой мозговой оболочки. Это сплетение образовано возвратными артериальными ветвями перипапиллярной хориоидеи, артериолами круга Цинна–Галлера и ветвями ЗКЦА. Необходимо отметить, что возвратные ветви начинаются внутри глазного яблока и, следовательно, подвержены действию внутриглазного давления.
Таким образом, основным источником кровоснабжения переднего отдела зрительного нерва является система задних коротких циллиарных артерий. ЗКЦА при различных вариантах ветвления в количестве от 3 до 8 подходят к глазному яблоку вокруг ДЗН (иногда почти вплотную). Некоторые авторы [11], основываясь на результатах многолетних исследований, утверждают, что задние циллиарные артерии могут отходить от глазничной артерии в количестве от 1 до 5, а затем, ветвясь, давать до 20 веточек задних коротких циллиарных артерий. Эти артерии можно разделить на 2 группы: параоптическую и дистальную. Первая входит у ДЗН, вторая – между задними длинными циллиарными и параоптическими артериями. Имеются сведения о наличии анастомозов между циллиарными артериями и ЦАС. Если в дальнейшем подтвердится наличие этих анастомозов, то это существенно повлияет на картину патогенеза ишемических нейропатий. При этом можно будет исследовать существование порочного круга или «системы обкрадывания», возникающей при острой гипотензии. Совместное отхождение циллиарных артерий и ЦАС обеспечивает равные условия гемодинамики в исходном пункте. В циллиарных артериях скорость кровотока и диастолическая его часть выше, чем в ретинальных артериях, что говорит о более низком сопротивлении сосудистого ложа, чем ретинального. В зависимости от входа этих артерий разделяют верхнюю, среднюю и нижнюю группы параоптических ЗКЦА. Однако необходимо оценивать кровообращение в головке зрительного нерва с учетом высокой индивидуальной вариабельности, так как имеется значительная вариабельность в ветвлении ЗКЦА как по их количеству, так и по топографии вхождения в задний полюс глаза [8,9,11]. Но это не дает объяснения феномену двустороннего поражения при передних ишемических нейропатиях.
Весь отток крови из переднего отдела зрительного нерва осуществляется главным образом через центральную вену сетчатки. Из преламинарной части отток частично происходит в перипапиллярные хориоидальные вены, несущие кровь в вортикозные вены. Этот путь венозного оттока может иметь некоторое значение в случаях окклюзии центральной вены сетчатки позади решетчатой пластинки [4]. Еще одним путем оттока, но не крови, а ликвора является глазнично–лицевой ликворолимфатический путь из межвлагалищного пространства зрительного нерва в подчелюстные лимфатические узлы [2].
Применение ФАГД позволило выделить два сосудистых сплетения в диске зрительного нерва – поверхностное и глубокое. Поверхностное – образовано ретинальными сосудами, отходящими от ЦАС. Глубокое – снабжает кровью ДЗН и образовано капиллярами, происходящими из хориоидальных сосудов системы ЗКЦА [4]. Капиллярная сеть на периферии ДЗН более скудная. В сосудах зрительного нерва отмечается ауторегуляция кровотока [1]. По данным некоторых авторов [4], поверхностное сплетение ДЗН не участвует в его кровоснабжении. Однако известно множество случаев одновременного побледнения ДЗН при окклюзии центральной артерии сетчатки и, наоборот, при тотальной передней ишемической нейропатии – появления симптома «вишневой косточки» в макулярной области.
В ретробульбарной части зрительного нерва выявляются все звенья микроциркуляторного русла: артериолы, прекапилляры, капилляры, посткапилляры и венулы. Обращает на себя внимание извитость артериол, преобладание венозного компонента и наличие множества венуло–венулярных анастомозов. Встречаются также артерио–венулярные шунты. Капилляры образуют преимущественно сетевые конструкции [1].
Ультраструктура стенок капилляров ДЗН оказалась сходной с капиллярами сетчатки и центральной нервной системы [1,4,6]. В отличие от хориокапилляров они непроницаемы и имеют одиночный слой эндотелиальных клеток без фенестров [4]. Между слоями основной мембраны в прекапиллярных, капиллярных и посткапиллярных сосудах распределены интрамуральные перициты. Эти клетки имеют темное ядро и цитоплазматические отростки. Возможно, они происходят из зародышевой сосудистой мезенхимы и являются продолжением мышечных клеток артериол. Существует мнение, что они ингибируют неоваскулогенез и имеют свойства гладкомышечных клеток, способных к сокращению [5]. По–видимому, при нарушении иннервации сосудов происходит их распад, что вызывает дегенеративные процессы в стенке сосудов, их запустевание и облитерацию. Однако вопросы о роли перицитов и строения стенки сосудов ДЗН требуют дальнейшего разрешения.
Заключение
Нам кажется, что для изучения патогенеза любого процесса в ДЗН необходимо учитывать следующие его анатомические особенности:
1. Особое строение решетчатой пластинки.
2. Индивидуальные особенности прохождения ЦАС через ДЗН и наличие анастомозов ее.
3. Распределение задних коротких циллиарных артерий, их количество и анастомозы по отношению к межневральным септам.
4. Особенности строения круга Галлера–Цинна
5. Изменения стенок сосудов, наличие восходящего облитерирующего процесса или изменение качественного состава крови и др.
Таким образом, анатомическое строение диска зрительного нерва, его кровоснабжение имеют очень сложную структуру и индивидуальную вариабельность. Несмотря на большое количество трудов в этой области, до сих пор остаются нерешенными некоторые вопросы морфологии, физиологии и гистологии зрительного нерва с точки зрения развития в нем сосудистых нарушений.
Литература
1. Антонова А.И. Острые сосудистые оптические нейропатии, обусловленные атеросклерозом (Особенности патогенеза, клинического течения и лечения) // Автореф. Дис… .докт. мед. наук. – Донецк., 1987. – 407 с. С. 18–20.
2. Каган И.И., Канюков В.Н. Клиническая анатомия органа зрения. – С.–П. Эскулап, 1999. – 190 с. С.105–108
3. Кацнельсон Л.А., Лысенко B.C., Балишанская Т.И. Клинический атлас патологии глазного дна. М.: Гэотар медицина. – 1998. – 152 с. С.22–23.
4. Кацнельсон Л.А., Форофонова Т.И., Бунин А.Я. Сосудистые заболевания глаз. – М.: Медицина, 1990.– 270 с, С. 13–15.
5. Кацнельсон Л.А, Танковский В.Э. Тромбозы вен сетчатки (клинико–организационное исследование). М. – 2000. – С. 16.
6. Нестеров А.П. Первичная глаукома. – М.: Медицина, 1982. –288с.
7. Сомов Е.Е. Клиническая анатомия органа зрения человека. С.–П.: 1997.–С. 61–66.
8. Харлап С.И. Анатомо–диагностические параллели состояния сосудов глаза и орбитального пространства по результатам цветового допплеровского картирования.// Вестн. Офтальмологии. – 2000. – є1. – С.45 – 48.
9. Харлап С.И., Лихникевич Е.Н., Першин К.Б., Пашинова Н.Ф., Ширшиков Ю.К. Топография и ангиоархитектоника зрительного нерва по данным ультразвуковых методов исследования и трехмерного оптического анализа.// Вестн. Офтальмологии. – 2001.–є1.–С.15–19.
10. Шамшинова А.М., Волков В.В. Функциональные методы исследования в офтальмологии. – М.: Медицина, 1999. – С.12.
11. Hayreh S. Structure and blood supply of the optic nerve // Glaucome: conception disease / Ed. K. Heilman, U. Richardson. – Philadelphia, 1978, p. 78–96.
12. lsayama Y., Hiramatsu K., Asakwa S. Et al/ Posterior ischemic optic neuropathy. 1. Blood supply of the optic nerve // Ophthalmologica (Basel). – 1983. – Vol. 186. – P. 194–203.
Строение сетчатки глаза — структура и функции
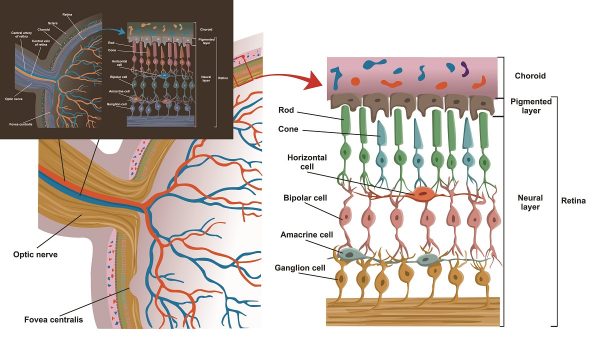
Сетчатка — функциональная единица центральной нервной системы, обеспечивающая преобразование светового сигнала в нервный импульс. Строение сетчатки представляет собой многослойную ткань. Которая состоит из шести типов нейрональных клеток (два типа фоторецепторов: колбочки и палочки; горизонтальные, биполярные, амакриновые и ганглиозные клетки). А также, трех типов глиальных (мюллеровы, глиальные, астроциты и микроглиальные). Наличие внутреннего и внешнего гемато-ретинальных барьеров и внутриретинальных соединений обусловливает тонкость регуляции обменов с кровообращением и внутри самой сетчатки. Центральная зона (макула) узкоспециализированная зона обеспечения остроты зрения, имеет специфические анатомические особенности.
Общая анатомия
Сетчатка выстилает заднюю часть глаза. Это тонкая прозрачная оболочка. Толщиной менее 500 мкм. Она выявляет васкуляризацию пигментов и васкуляризацию сосудистой оболочки, лежащую в основе розово-оранжевого цвета глазного дна. Головка зрительного нерва видна макроскопически в виде розоватого диска. Вокруг которого выходят ретинальные артерии и вены, называемые зрительным сосочком.
Макула представляет собой область задней части, центр которой аваскулярен. Ее можно различить при осмотре глазного дна по оранжевой окраске из-за присутствия пигментов ксантофилла. Расположена височно по отношению к диску зрительного нерва. Ямка в центре макулы, состоящая только из колбочек, обеспечивает остроту зрения. Простирается от зубчатой мышцы спереди до зрительного нерва на заднем полюсе глазного яблока.
Плоская часть является областью, в которую вводятся инструменты для витреоретинальной хирургии. В это место выполняются интравитреальные инъекции. Поперечный диаметр взрослого эмметропического глаза составляет около 22 мм. Она покрывает примерно 15-16 мм внутреннего диаметра глаза и 72 % поверхности глазной сферы. Склера, белая оболочка, обеспечивающая жесткость глазного яблока, имеет толщину менее миллиметра.
Васкуляризация сетчатки: сосуды и сосудистой оболочки
Сетчатка васкуляризируется двумя различными сосудистыми системами, не имеющими анатомических связей в физиологических условиях: ретинальной капиллярной сетью, обеспечивающей непосредственную неоваскуляризацию слоев, и хориоидальной сетью, обеспечивающей васкуляризацию косвенно, так как в наружной части нет капилляров. Центральная артерия отходит главным образом от внутренней сонной артерии, следует внутриневрально и выходит на диск зрительного нерва, где делится на четыре конечные ветви: височную и носовую, верхнюю и нижнюю. Конечные артерии делятся на коллатеральные артерии, которые различаются на терминальные артерии, что также имеют коллатерали. И так далее дихотомически, пока не сформируется решетчатая сеть, покрывающая каждую из артерий, квадрант внутренней сетчатки. Капилляры отходят от этих коллатеральных сосудов и организованы в поверхностные, промежуточные и глубокие сплетения.
Артерии и вены
Артерии и вены располагаются в волоконно-оптическом слое. Капилляры имеют диаметр 5-6 мкм и образованы эндотелиальными с плотным соединением, расположенными на толстой базальной мембране. Их окружают перициты и микроглии. Типы глиальных различаются в поверхностных и глубоких сосудистых сплетениях: в то время как в поверхностных и промежуточных сосудистых сплетениях глио-нейроваскулярная связь опосредована астроцитами и мюллеровскими глиальными, в глубоком сплетении отсутствуют периваскулярные астроциты и только мюллеровские глиальные могут обеспечивать, в частности, через калиевые каналы. Таким образом, в случае отказа мюллеровских глиальных глубокая капиллярная сеть более чувствительна к потере регуляции в ответ на активность фоторецепторов.
Хориоидальная сосудистая система доставляет питательные вещества и кислород к наружной сетчатке и, в частности, к фоторецепторам опосредованно, так как наружная не имеет питающей капиллярной сети. Хориоидальная сосудистая сеть происходит от ветвей глазной артерии, которая сама является ветвью внутренней сонной артерии. Сосудистая оболочка представляет собой ткань толщиной от 300 до 500 мкм у человека, ограниченную мембраной Бруха спереди и спаянную со склерой сзади.
Она состоит из пигментированных (меланоцитов), тучных клеток, микроглии и сосудов. Хориоидальный кровоток является одним из важнейших в организме. Сосуды хориокапилляров, организованные в функциональные дольки, орошаемые независимыми артериолами, образованы слоем эндотелиальных с плотными соединениями, содержащими большие диафрагмальные фенестрации (от 60 до 90 нм), открытие которых зависит от роста эндотелия сосудов, таким образом регулируя прохождение белков и макромолекул. Этот белковый градиент между сетчаткой и сосудистой оболочкой необходим для прикрепления и для состояния прозрачности, необходимого для передачи фотонов. Сосудистая оболочка богато иннервирована парасимпатическими, симпатическими и тройничными чувствительными нервными волокнами, которые регулируют хориоидальный кровоток.
Микроскопическая анатомия
Классически существует десять слоев сетчатки:
- слой клеток пигментного эпителия;
- наружный и внутренний сегменты фоторецепторов;
- наружная пограничная мембрана, место соединения мюллеровских с сегментами фоторецепторов и фоторецепторов между ними системами адгезионных и плотных контактов;
- фоторецепторных ядер или наружный ядерный;
- наружный плексиформный, образованный синапсами между биполярными клетками и фоторецепторами и с горизонтальными. Последние модулируют нервное сообщение, передаваемое по прямому пути;
- внутренний ядерный, представляющий собой слой ядер горизонтальных, биполярных, амакриновых и клеток Мюллера. Наружная часть содержит тела горизонтальных клеток, центральная часть — ядра биполярных и Мюллера, а самая внутренняя часть — амакриновые;
- плексиформный (зернистый), состоящий из дендритов ганглиозных и аксонов биполярных клеток;
- ганглиозных клеток;
- нервных волокон. Состоящий из аксонов ганглиозных, окруженных глиальными отростками, образующими зрительный нерв, связанный с головным мозгом;
- внутренняя пограничная мембрана, представляющая собой мембранное расширение, состоящее из ножек мюллеровских и их базальной мембраны.
Пигментный эпителий
Монослой пигментного эпителия (ПЭС) является основным компонентом не только из-за его физических и функциональных свойств в качестве внешнего гематоретинального барьера и его оптических свойств, но особенно из-за его многочисленных метаболических активностей. Представляет собой прилегающий эпителий с плотным соединением, сильно поляризованный, содержащий множество ионных и водных каналов на его базолатеральной и апикальной поверхностях, обеспечивающий избирательный транспорт между нейросетчаткой и хориоидальной сосудистой сетью. Необходим для зрения из-за его метаболической активности в ретиноидном цикле, а также из-за фагоцитоза и рециркуляции «использованных» внешних сегментов фоторецепторов. Содержит пигменты, образованные в основном из зерен меланина и липофуксина. Эти зерна особенно реагируют на фотоны с короткими длинами волн, которые вызывают выработку активных форм кислорода, способных вызвать окислительный стресс.
Фоторецепторы
Фоторецепторы представляют собой сильно поляризованные нейроны. Внешний сегмент фоторецептора составляет светочувствительную часть. Он образован складками плазматической мембраны, образующими стопку дисков, которые обновляются и фагоцитируются ПЭС. Внутренний сегмент содержит метаболический аппарат и соединен с внешним сегментом соединительными ресничками. Область, в которой расположены митохондрии, можно визуализировать с помощью оптической когерентной томографии. Внешняя пограничная мембрана соответствует соединительным комплексам между фоторецепторами и мюллеровскими. Содержит ядра фоторецепторов. Внешний плексиформный слой соответствует синапсам, установленным между фоторецепторами и биполярными и горизонтальными клетками, которые образуют более толстый слой волокон Генле, в макулярной области (50 мкм), где располагаются Мюллера. Эти различные структуры, образующие внешнюю часть, можно исследовать с помощью оптической когерентной томографии. Они являются маркерами целостности и зрительной функции.
Ганглиозные клетки и волоконно-оптический слой
Ганглиозные представляют собой клетки размером 10–20 мкм. Эти клетки через свои дендриты образуют синапсы с биполярными и амакриновыми во внутреннем плексиформном слое. Аксоны ганглиозных сходятся в сосочке, образуя зрительный нерв. Они образуют переплетенные волокна с отростками из мюллеровых клеток. Волокна конвергируют на уровне зрительного нерва с радиальной ориентацией. За исключением макулярных волокон, которые образуют прямолинейную межпапилломакулярную сеть.
Глиальные клетки
Глия, как и нейрональная глия в центральной нервной системе, играет несколько ролей в гомеостазе нейронов: транспорт питательных веществ, гидроионная регуляция, иммуномодуляция, продукция нейротрофических факторов. В основной физиологической ситуации астроциты и микроглия располагаются во внутренних слоях.
Астроциты располагаются также вокруг сосудов, под внутренней пограничной мембраной, и очень многочисленны у выхода диска зрительного нерва. Ядра Мюллера находятся в средней части внутреннего ядерного слоя, но их цитоплазматические отростки простираются от внутренней пограничной мембраны до сегментов фоторецепторов. Не исключено, что их отростки могут противостоять микроворсинкам пигментного эпителия.
Клетки Мюллера являются основными позвоночных. Они представляют собой анатомическую связь между нейронами и отделами, с которыми они обмениваются молекулами, а именно сосудами, стекловидным телом и субретинальным пространством. Они наделены множеством различных ионных каналов, рецепторов лигандов, трансмембранных транспортных молекул и ферментов. В частности, экспрессируют глутаминсинтетазу, которая превращает интернализованные молекулы глутамата в глутамин. Они отвечают за поддержание гомеостаза внеклеточной среды (ионы, вода, нейротрансмиттеры и рН). Одной из их основных характеристик является высокая проводимость их плазматической мембраны по отношению к калию. Они участвуют в метаболизме глюкозы, обеспечивая нейроны лактатом и пируватом для их окислительного метаболизма, а также в устранении метаболических отходов.
Астроциты бывают двух типов. С одной стороны, клетки вдвое длиннее своей ширины располагаются вдоль волоконно-оптических пучков, без контакта с сосудами. С другой стороны, другая популяция звездчатых астроглиальных пересекает слой оптического волокна и устанавливает неспециализированные контакты с сосудами. В физиологических условиях микроглии располагаются исключительно вокруг сосудов.
Макула человека
Макула человека составляет менее 5% от общей поверхности сетчатки. Это небольшая специализированная область, расположенная в центре зрительной оси. Она обеспечивает фотопическое и цветовое зрение, а также остроту.
В этой области все слои смещаются, оставляя в центре макулы центральную зону. Ямку, образованную исключительно колбочками и определенными мюллеровскими глиальными, структура и функция которых отличны от других мюллеровских. На крыше ямки мог быть другой тип глиальных, вероятно, астроцитарного типа, функцию которого еще предстоит определить. В этой области находится наибольшая плотность колбочек, которая обеспечивает остроту зрения, цветовое и фотопическое зрение. Макула развивается после рождения. Она достигает своей анатомо-функциональной зрелости примерно к 10-12 годам. Только у приматов и человека имеется одно пятно. Тогда как у других животных его нет, за исключением хищных птиц, у которых их два.
Вывод
Строение сетчатки отражает ее функциональную сложность и исключительную топографическую специализацию. Многие структурные анализы с использованием специальных методов по-прежнему необходимы. С одной стороны, для определения морфологии нормальной сетчатки человека. С другой стороны, для оценки функциональных физиологических изменений. Использование методов визуализации, а также идентификация специфических маркеров различных типов клеток остаются необходимыми для более точного морфологического анализа.
Таким образом, неинвазивные методы визуализации, такие как оптическая когерентная томография в спектральной области (SD-OCT), в сочетании или без ангиографии без красителей (OCT-A) или аналогичная адаптивная оптика, можно получить изображения в поперечных срезах (или «анфас») и даже визуализировать определенные клетки. Эти методы используются в рутинной практике для диагностических целей и принятия терапевтических решений. В настоящее время разрабатываются другие методы визуализации с очень высоким разрешением. Такие как фазово-контрастная микроскопия с транссклеральным освещением, позволит еще точнее исследовать нормальную и патологическую сетчатку.
Рефлексы – важнейшая функция организма. Ученые, которые занимались изучением рефлекторной функции, в большинстве своем были согласны с тем, что все сознательные и бессознательные акты жизнедеятельности по своей сути являются рефлексами.
Содержание
- 1 Что такое рефлекс
- 2 Виды рефлексов
- 3 Особенности строения рефлекторных дуг
- 4 Как осуществляется рефлекс
- 5 Зрительный путь
- 6 Зрачковый рефлекс
Что такое рефлекс
Рефлекс – ответ центральной нервной системы на раздражение рецептов, который обеспечивает реакцию организма на изменение во внутренней или внешней среде. Осуществление рефлексов происходит за счет раздражения нервных волокон, которые собраны в рефлекторные дуги. Проявлениями рефлекса выступают возникновение или прекращение деятельности со стороны организма: сокращение и расслабление мышц, секреция желез или ее остановка, сужение и расширение сосудов, изменения зрачка и прочее.
Рефлекторная деятельность позволяет человеку быстро реагировать и должным образом приспосабливаться к изменениям вокруг себя и внутри. Нельзя ее недооценивать: позвоночные животные настолько зависимы от рефлекторной функции, что даже частичное ее нарушение приводит к инвалидности.
Виды рефлексов
Все рефлекторные акты принято разделять на безусловные и условные. Безусловные передаются наследственным путем, они свойственны каждому биологическому виду. Рефлекторные дуги для безусловных рефлексов формируются еще до рождения организма и сохраняются в таком виде до конца его жизнедеятельности (если отсутствует влияние негативных факторов и болезней).
Условные рефлексы возникают в процессе развития и накопления определенных навыков. Новые временные связи вырабатываются в зависимости от условий. Они формируются из безусловных, при участии высших мозговых отделов.
Все рефлексы классифицируют по разным признакам. По биологическому значению разделяют пищевые, половые, оборонительные, ориентировочные, локомоторные (передвижение), позно-тонические (положение). Благодаря этим рефлексам живой организм способен обеспечивать главные условия жизнедеятельности.
В каждом рефлекторном акте в той или иной степени учувствуют все отделы ЦНС, поэтому любая классификация будет условной.
В зависимости от расположения рецепторов раздражения, рефлексы бывают:
- экстерорецептивными (внешняя поверхность тела);
- висцеро- или интерорецептивными (внутренние органы и сосуды);
- проприорецептивные (скелетные мышцы, суставы, сухожилия).
По месту размещения нейронов, рефлексы бывают:
- спинальными (спинной мозг);
- бульбарными (продолговатый мозг);
- мезенцефальными (средний мозг);
- диэнцефальными (промежуточный мозг);
- кортикальными (кора больших полушарий мозга).
В рефлекторных актах, осуществляемых нейронами высших отделов ЦНС, также участвуют волокна низших отделов (промежуточный, средний, продолговатый и спинной мозг). При этом рефлексы, которые производятся нижними отделами ЦНС, обязательно доходят до высших. По этой причине представленную классификацию нужно считать условной.
В зависимости от ответной реакции и участвующих органов, рефлексы бывают:
- моторными, двигательными (мышцы);
- секреторными (железы);
- сосудодвигательными (кровеносные сосуды).
Однако эта классификация применима лишь к простым рефлексам, которые объединяют некоторые функции внутри организма. Когда происходят сложные рефлексы, раздражающие нейроны высших отделов ЦНС, в процесс вовлекаются разные органы. Так меняется поведение организма и его соотношение с внешней средой.
К простейшим спинальным рефлексам относят сгибательный, который позволяет устранить раздражитель. Сюда также можно отнести рефлекс почесывания или натирания, коленный и подошвенный рефлексы. Самые простые бульбарные рефлексы: сосательный и корнеальный (смыкание век при раздражении роговицы). К мезенцефальным простым относят зрачковый рефлекс (сужение зрачка при ярком освещении).
Особенности строения рефлекторных дуг
Рефлекторной дугой называют путь, который проходят нервные импульсы, осуществляя безусловные и условные рефлексы. Соответственно, вегетативная рефлекторная дуга – путь от раздражения нервных волокон до передачи информации в мозг, где она преобразуется в руководство к действию определенного органа. Уникальное строение рефлекторной дуги включает цепь из рецепторных, вставочных и эффекторных нейронов. Благодаря такому составу осуществляются все рефлекторные процессы в организме.
Рефлекторные дуги как части периферической нервной системы (часть НС за пределами головного и спинного мозга):
- дуги соматической нервной системы, которые обеспечивают нервными клетками скелетную мускулатуру;
- дуги вегетативной системы, которые регулируют функциональность органов, желез и сосудов.
Строение вегетативной рефлекторной дуги:
- Рецепторы. Они служат для приема факторов раздражения и ответа возбуждением. Одни рецепторы представлены в виде отростков, другие микроскопические, но они всегда включают нервные окончания и клетки эпителия. Рецепторы являются частью не только кожи, но также и всех других органов (глаза, уши, сердце и прочее).
- Чувствительное нервное волокно. Эта часть дуги обеспечивает передачу возбуждения к нервному центру. Так как тела нервных волокон расположены непосредственно вблизи спинного и головного мозга, их не включают в ЦНС.
- Нервный центр. Здесь обеспечивается переключение между чувствительными и двигательными нейронами (благодаря мгновенному возбуждению).
- Двигательные нервные волокна. Эта часть дуги передает сигнал от ЦНС к органам. Отростки нервных волокон расположены возле внутренних и внешних органов.
- Эффектор. В этой части дуги сигналы обрабатываются, формируется ответная реакция на раздражение рецептора. Эффекторами по большей части выступают мышцы, которые сокращаются, когда центр принимает возбуждение.
Сигналы рецепторных и эффекторных нейронов идентичны, так как она взаимодействуют, следуя по одной дуге. Простейшая рефлекторная дуга в человеческом организме образуется двумя нейронами (сенсорный, двигательный). Другие включают три и больше нейронов (сенсорный, вставочный, двигательный).
Простые рефлекторные дуги помогают человеку непроизвольно адаптироваться к изменениям в окружении. Благодаря ним мы отдергиваем руку, если чувствуем боль, а зрачки реагируют на изменения освещения. Рефлексы помогают регулировать внутренние процессы, способствуют сохранению постоянства внутренней среды. Без рефлексов гомеостаз был бы невозможен.
Как осуществляется рефлекс
Нервный процесс может спровоцировать активность органа или повысить ее. При принятии нервной тканью раздражения, она переходит в особое состояние. Возбуждение зависит от дифференцированных показателей концентрации анионов и катионов (отрицательно и положительно заряженные частицы). Они расположены по двум сторонам мембраны отростка нервной клетки. При возбуждении меняется потенциал электричества на мембране клетки.
Когда рефлекторная дуга имеет сразу два двигательных нейрона в спинномозговом ганглии (нервный узел), то дендрит клетки будет длиннее (разветвленный отросток, который получает информацию через синапсы). Он направлен к периферии, но остается частью нервной ткани и отростков.
Скорость возбуждения каждого волокна составляет 0,5-100 м/с. Деятельность отдельных волокон осуществляется изолировано, то есть скорость не переходит с одного на другое.
Торможение возбуждения прекращает функционирование участка раздражения, замедляя и ограничивая движения и ответные реакции. Причем возбуждение и торможение происходит параллельно: пока одни центры угасают, другие возбуждаются. Таким образом, задерживаются отдельные рефлексы.
Торможение и возбуждение взаимосвязаны. Благодаря этому механизму обеспечивается согласованная работа систем и органов. К примеру, движения глазного яблока осуществляются за счет чередования работы мышц, ведь при взгляде в разные стороны сокращаются разные группы мышц. Когда возбуждается центр, отвечающий за напряжение мышц одной стороны, центр другой тормозит и расслабляется.
В большинстве случаев сенсорные нейроны передают информацию непосредственно в головной мозг, используя рефлекторную дугу и несколько вставочных нейронов. Мозг не только обрабатывает сенсорную информацию, но также накапливает ее для будущего использования. Параллельно с этим мозг посылает импульсы по нисходящему пути, инициируя ответ эффекторов (орган-мишень, который выполняет задачи ЦНС).
Зрительный путь
Анатомическая структура зрительного пути представлена рядом нейронных звеньев. В сетчатке это палочки и колбочки, затем биполярные и ганглиозные клетки, а дальше аксоны (нейриты, которые служат путем для импульса, исходящего от тела клетки к органам).
Эта цепь представляет периферическую часть зрительного пути, которая включает зрительный нерв, хиазму и зрительный тракт. Последний заканчивается в первичном зрительном центре, откуда начинается центральный нейрон зрительного пути, который доходит до затылочной доли мозга. Здесь же расположен кортикальный центр зрительного анализатора.
Составляющие зрительного пути:
- Зрительный нерв начинается с сетчатки и заканчивается в хиазме. Его протяжность составляет 35-55 мм, а толщина 4-4,5 мм. Нерв имеет три оболочки, он четко разделен на половины. Нервные волокна зрительного нерва разделяются в три пучка: аксоны нервных клеток (от центра сетчатки), два волокна ганглиозных клеток (от носовой половины сетчатки, а также от височной половины сетчатки).
- Хиазма начинается над областью турецкого седла. Она покрыта мягкой оболочкой, по длине составляет 4-10 мм, по ширине 9-11 мм, в толщину 5 мм. Здесь соединяются волокна от обоих глаз, образуя зрительные тракты.
- Зрительные тракты берут начало от задней поверхности хиазмы, огибают ножки мозга и входят в наружное коленчатое тело (безусловный зрительный центр), зрительный бугор и четверохолмии. Длина зрительных трактов составляет 30-40 мм. От коленчатого тела начинаются волокна центрального нейрона, а заканчиваются в борозде птичьей шпоры – в сенсорном зрительном анализаторе.
Зрачковый рефлекс
Рассмотрим рефлекторную дугу на примере зрачкового рефлекса. Путь зрачкового рефлекса проходит по сложной рефлекторной дуге. Он начинается от волокон палочек и колбочек, которые входят в состав зрительного нерва. Волокна перекрещиваются в хиазме, переходя в зрительные тракты, останавливаются перед коленчатыми телами, частично перекручиваются и доходят до претектальной области. Отсюда новые нейроны идут к глазодвигательному нерву. Это третья пара черепных нервов, которая отвечает за движение глазного яблока, световую реакцию зрачков, поднятие века.
Обратный путь начинается от глазодвигательного нерва в глазницу и ресничный узел. Второй нейрон звена выходит из ресничного узла, через склеру в перихориоидальное пространство. Здесь образуется нервное сплетение, разветвления которого проникают в радужку. Сфинктер зрачка имеется 70-80 радиальных пучков нейрона, входящих в него секторально.
Сигнал для мышцы, которая расширяет зрачок, идет от цилиоспинального центра Будге, который расположен в спинном мозге между седьмым шейным и вторым грудным позвонками. Первый нейрон идет через симпатический нерв и симпатические шейные ганглии, второй начинается от верхнего ганглия, который входит в сплетение внутренней сонной артерии. Волокно, которое обеспечивает нервами дилататор зрачка, покидает сплетение в полости черепа и через тройничный узел входит в зрительный нерв. Через него волокна проникают в глазное яблоко.
Замкнутость кольцевой работы нервных центров делает ее совершенной. Благодаря рефлекторной функции коррекция и регуляция деятельности человека может происходить произвольно и непроизвольно, защищая организм от изменений и опасности.
Используемые источники:
- Гольдовская, И. Л. Психотропная терапия и орган зрения / И.Л. Гольдовская. — М.: Медицина, 1987.
- Демирчоглян, Г. Г. Физиология и патология сетчатки глаза: Первичные механизмы зрения / Г.Г. Демирчоглян. — М.: Медицина
- Дормидонтова, К. В. Некоторые глазные заболевания и их профилактика / К.В. Дормидонтова. — Москва
- ФГБУ «НМИЦ им. В. А. Алмазова» Минздрава России
Контактные линзы каких брендов вам знакомы?
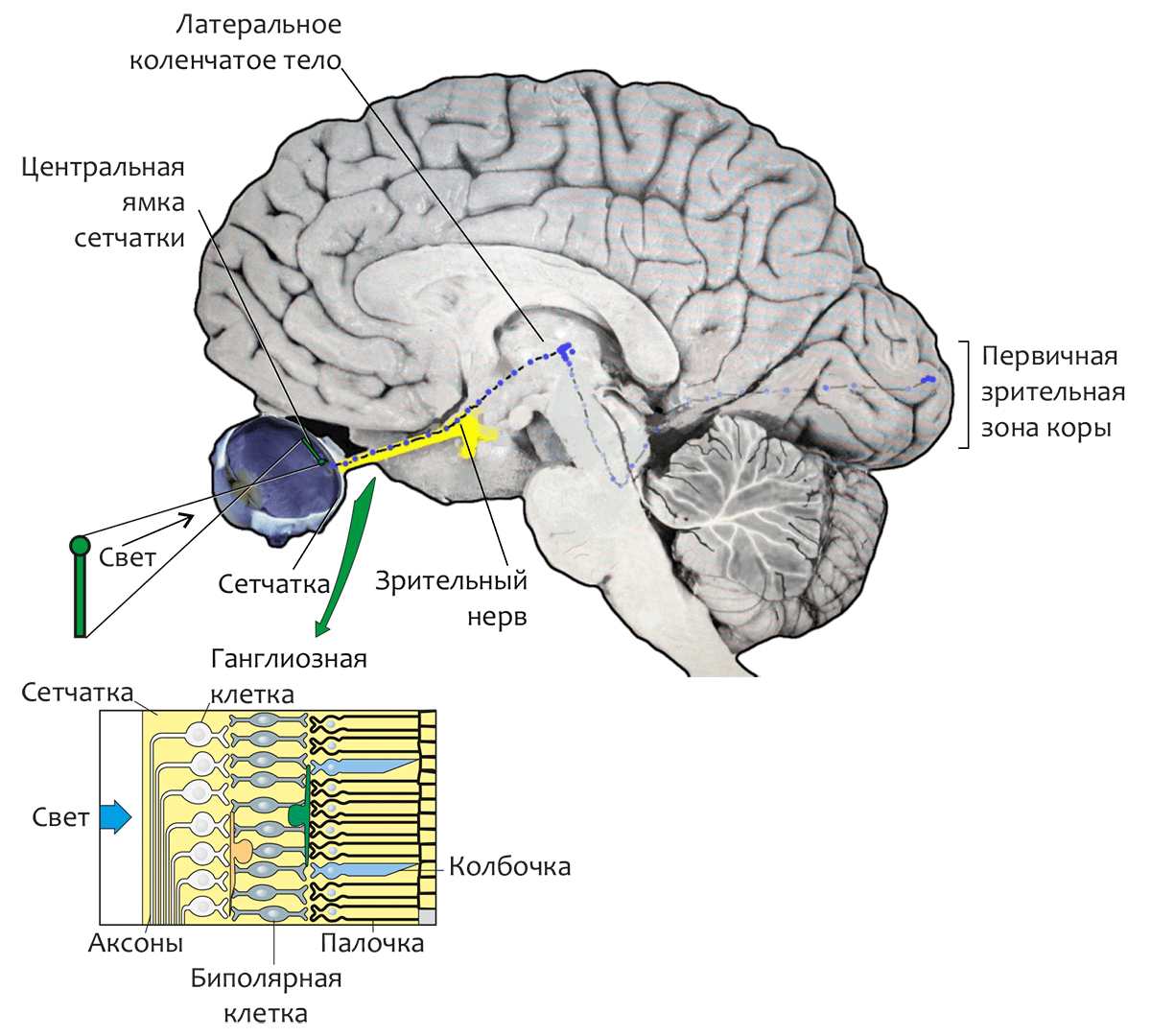
Наша способность видеть — это большая работа всего зрительного аппарата. Схему функций, задач и всей работы нервных клеток глаза и головного мозга в целом называют зрительным путем.
Зрительный путь — что это?
Зрительный путь — это путь, который проделывают нервные импульсы от фоторецепторов сетчатки (внутренней оболочки глазного яблока) до нервных центров головного мозга.
Основной рецептор глаза — сетчатка, в которой есть палочки и колбочки. Они преобразовывают пучок света в электрические импульсы и передают их нервным клеткам. Нервные импульсы в свою очередь отправляют информацию в центральный отдел в коре головного мозга, где происходит распознавание полученных характеристик и формируется реальное изображение окружающего мира.
То есть зрительный путь — это система работы нервных клеток, которая позволяет человеку видеть.
Строение зрительного пути
Начинается зрительный путь с сетчатки глаза. Именно здесь фоторецепторы — палочки и колбочки — переводят световые сигналы в нервные импульсы. Затем эти нервные импульсы передаются к биполярным клеткам (соединяют одну колбочку или несколько палочек с одной ганглионарной клеткой (нервная клетка (нейрон) сетчатки глаза, способная генерировать нервные импульсы в отличие от других типов нейронов сетчатки)) и нейронам сетчатки.
У нейронов есть длинные отростки — аксоны. Они отвечают за сбор информации со всей поверхности сетчатки. Миллионы аксонов, соединенные вместе, образуют зрительный нерв.
Группы аксонов располагаются в строго определенном порядке. Главный среди этих групп — папилло-макулярный пучок, который передает сигналы от так называемой макулярной зоны сетчатой оболочки глаза.
Далее зрительный нерв входит в череп через зрительный канал. Волокна двух зрительных нервов частично перекрещиваются. Этот перекрест — хаизма — особо важная часть нашего зрения. Так, с этой частью глазного пути связано то, что при поражениях турецкого седла (патологий нервной или эндокринной системы), а также при повреждениях внутренних сонных артерий у человека происходит выпадение частей поля зрения (внутренних и наружных).
Далее пучок нервных волокон (зрительный тракт) обходит ножки мозга — его особые парные структуры — и попадают в заднюю часть зрительного бугра. Ощущение света, которое испытывают в этот момент наш мозг, вызывает рефлекторные реакции, проявляющиеся, например, поворотом головы в сторону резкой вспышки.
В этом же отделе специальные группы клеток формируют зрительную лучистость, которая передает информацию клеткам коры головного мозга, где происходит расшифровка нервных импульсов и создается изображение окружающего мира.
Строение зрительного пути — сложно и многофункционально. Это целый механизм, который работает ежесекундно и буквально мгновенно выполняет все свои задачи, благодаря чему мы и видим предметы вокруг нас.
Симптоматика заболеваний зрительного пути
Под влиянием негативных внутренних или внешних факторов в зрительном пути могут развиваться различные патологии и заболевания. При появлении каких-либо нарушений возникают безболезненные симптомы:
Слепота одного глаза и полное сохранение зрения другого — часто так происходит при нарушениях зрительного нерва с соответствующей стороны
Выпадение определенных частей полей зрения — признак повреждений зрительной лучистости или хиазмы.
Диагностика заболеваний и лечение зрительного пути
Для выявления причин нарушений зрительного пути и постановки правильного диагноза мы используем современные диагностические методики:
Визометрия — проверка зрения с помощью специальных таблиц или автоматических проекторов
Периметрия — обследование, которое определяет поле зрение Пациента и оценивает его остроту.
Как правило, поражение зрительного пути происходит при глаукоме и атрофии зрительного нерва. Но нередко причины патологий заключаются в глубинных нарушениях организма — опухолях головного мозга, травмах головы или энцефалопатии (разрушениях нервных клеток при нарушении кровоснабжения мозга).
Врачи Глазной клиники доктора Беликовой проводят внимательный осмотр каждого Пациента и выявляют не только сами заболевания органов зрения, но и делают все возможное для определения причин, вызвавших ту или иную патологию. Лечение нарушений зрительного пути в каждом конкретном случае подбирается индивидуально и зависит от ряда особенностей организма Пациента.
Нервы глаза принято подразделять на три группы: двигательные, секреторные и чувствительные.
Чувствительные нервы отвечают за регулирование обменных процессов, а также обеспечивают защиту, предупреждая о любых внешних воздействиях. К примеру, попадании в глаз инородного тела или возникновении воспалительного процесса внутри глаза.
Задача двигательных нервов — обеспечение движения глазным яблоком посредством согласованного напряжения двигательных мышц глаза. Они отвечают за функционирование дилататора и сфинктера зрачка, регулируют ширину глазной щели. Двигательные мышцы глаза в своей работе по обеспечению глубины и объема зрения, находятся под контролем глазодвигательного, отводящего и блокового нервов. Ширина глазной щели контролируется лицевым нервом.
Мышцы самого зрачка контролируются волокнами нервов вегетативной нервной системе.
Находящиеся в составе лицевого нерва секреторные волокна, регулируют функции слезной железы органа зрения.
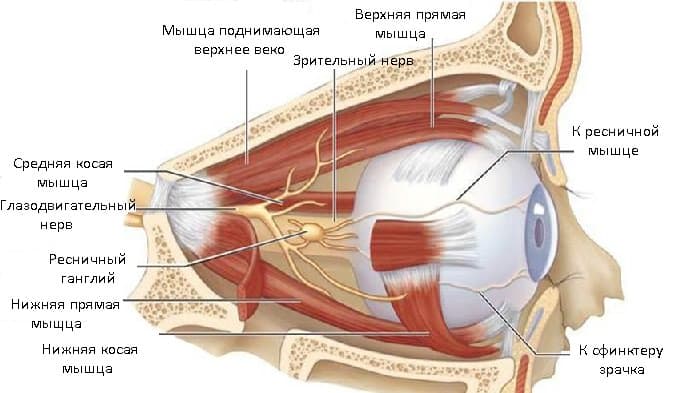
Иннервация глазного яблока
Все нервы, занятые в обеспечении функционирования глаза, берут начало в группах нервных клеток, локализованных в головном мозге и нервных узлах. Задача нервной системы глаза – регуляция работы мышц, обеспечение чувствительности глазного яблока, вспомогательного аппарата глаза. Кроме того, она регулирует реакции обмена веществ и тонус кровеносных сосудов.
В иннервации глаза участвуют 5 пар из 12 имеющихся черепно-мозговых нервов: глазодвигательный, лицевой, тройничный, а также отводящий и блоковый.
Глазодвигательный нерв берет начало от нервных клеток в головном мозге и имеет тесную связь с нервными клетками отводящего и блокового нервов, а также слухового, лицевого нервов. Кроме того, существует его связь и со спинным мозгом, обеспечивающая согласованную реакцию глаз, туловища и головы в ответ на слуховые и зрительные раздражители либо изменения положения туловища.
Глазодвигательный нерв заходит в глазницу через отверстие верхней глазничной щели. Его роль — поднятие верхнего века, с обеспечением работы внутренней, верхней, нижней прямых мышц, а также нижней косой мышцы. Также, к глазодвигательному нерву относятся веточки, регулирующие деятельность цилиарной мышцы, работу сфинктера зрачка.
Вместе с глазодвигательным, в глазницу через отверстие верхней глазничной щели входят еще 2 нерва: блоковый и отводящий. Их задача – иннервация, соответственно, верхней косой и наружной прямой мышц.
Лицевому нерву принадлежат двигательные нервные волокна, а также веточки, регулирующие деятельность слезной железы. Он регулирует мимические движения мышц лица, работу круговой мышцы глаза.
Функция тройничного нерва смешанная, он регулирует работу мышц, отвечает за чувствительность и включает вегетативные нервные волокна. В соответствии с названием, тройничный нерв, распадается на три крупные ветки.
Первой магистральной ветвью тройничного нерва выступает глазной нерв. Проходя в глазницу через отверстие верхней глазничной щели, глазной нерв дает начало трем основным нервам: носоресничному, лобному и слезному.
В мышечной воронке проходит носослезный нерв, в свою очередь делясь на решетчатые (передние и задние), длинные цилиарные, а также носовые ветви. Также он отдает соединительную ветку ресничному узлу.
Решетчатые нервы участвуют в обеспечении чувствительности клеток в решетчатом лабиринте, носовой полости, кожных покровов кончика носа и его крыльев.
Длинные цилиарные нервы пролегают в склере в зоне зрительного нерва. Далее их путь продолжается в надсосудистом пространстве в направлении переднего отрезка глаза, где они и короткие цилиарные нервы, отходящие от ресничного узла, создают нервное сплетение окружности роговицы и цилиарного тела. Это нервное сплетение регулирует обменные процессы и обеспечивает чувствительность переднего отрезка глаза. Также, длинные цилиарные нервы включают симпатические нервные волокна, которые ответвляются от нервного сплетения, принадлежащего внутренней сонной артерии. Они регулируют деятельность дилататора зрачка.
Начало коротких цилиарных нервов приходится на область ресничного узла, они пролегают через склеру, окружая зрительный нерв. Роль их — это обеспечение нервного регулирования сосудистой оболочки. Ресничный, также называемый цилиарным, нервный узел является объединением нервных клеток, принимающих участие в чувствительной (с помощью носоресничного корешка), двигательной (посредством глазодвигательного корешка), а также вегетативной (за счет симпатических нервных волокон), непосредственной иннервации глаза. Локализуется цилиарный узел на расстоянии 7мм кзади от яблока глаза снизу наружной прямой мышцы, соприкасаясь со зрительным нервом. При этом, цилиарные нервы, совместно регулируют деятельность зрачковых сфинктера и дилятатора, обеспечивают особую чувствительность роговицы, радужной оболочки, цилиарного тела. Они поддерживают тонус кровеносных сосудов, регулируют обменные процессы. Подблоковый нерв, считается последней ветвью носоресничного нерва, он участвует в осуществлении чувствительной иннервации кожных покровов корня носа, а также внутреннего угла век, части, конъюнктивы глаза.
Входя в глазницу, лобный нерв распадается на две ветки: надглазничный нерв и надблоковый. Данные нервы, обеспечивают чувствительность кожи лба и средней зоны верхнего века.
Слезный нерв, при входе в глазницу, распадается на две ветки — верхнюю и нижнюю. При этом, верхняя ветвь отвечает за нервную регуляцию деятельности слезной железы, а также чувствительность конъюнктивы. Вместе с тем она обеспечивает иннервацию кожного покрова наружного угла глаза, захватывая участок верхнего века. Нижняя ветвь объединяется со скуловисочным нервом — ответвлением скулового нерва и обеспечивает чувствительность кожи скулы.
Вторая ветвь, становится верхнечелюстным нервом и делится на две основные магистрали – подглазничную и скуловую. Они иннервируют вспомогательные органы глаза: середину нижнего века, нижнюю половину слезного мешка, верхнюю половину слезоносового протока, кожу лба и скуловой области.
Последняя, третья ветвь, отделившись от тройничного нерва, в иннервации глаза, участие не принимает.
Видео об иннервации глаза

Методы диагностики
- Внешнее визуальное обследование – ширина щели глаза, положение верхнего века.
- Определение величины зрачка, реакций зрачка на свет (прямой и содружественной).
- Оценка объема движений глазным яблоком – проверка функций глазодвигательных мышц.
- Оценка чувствительности кожи, в соответствии с иннервацией их соотносящимися нервами.
- Определение возможной болезненности на выходах тройничного нерва.
Симптомы при заболеваниях нервов глаза
- Нарушения работы слезной железы.
- Снижение остроты зрения вплоть до слепоты.
- Изменение поля зрения.
- Параличи либо парезы двигательных мышц глаза.
- Возникновение паралитического косоглазия.
- Нистагм.
Болезни с поражением нервов глаза
- Птоз века.
- Атрофия зрительного нерва.
- Синдром Маркуса-Гунна.
- Синдром Горнера.
- Опухоли зрительного нерва.
Зрение — одно из наиболее удивительных чувств, которым природа наградила человека. С помощью зрения мы получаем огромное количество информации об окружающем мире, можем наслаждаться красотами природы и великими произведениями искусства. За восприятие электромагнитного излучения «видимого диапазона», лежащее в основе зрения, отвечает рецептор белковой природы, содержащийся в фоторецепторной мембране «дисков» клеток сетчатки глаза, — родопсин.
Введение
Родопсин — светочувствительный пигмент (хромопротеин) фоторецепторных клеток сетчатки глаза позвоночных — является в настоящее время одним из наиболее изученных мембранных белков. Сетчатка глаза (рис. 1) преобразует свет в нервные сигналы, определяя чувствительность зрения в различных диапазонах освещенности — от звездной ночи до солнечного полдня. Сетчатка образована двумя главными типами зрительных клеток — палочками (около 120 млн. клеток на сетчатку человека) и колбочками (около 7 млн. клеток). Колбочки, сконцентрированные преимущественно в центральной области сетчатки (называемой центральной ямкой), функционируют только при ярком свете и отвечают за цветовое зрение и чувствительность к мелким деталям, а более многочисленные палочки ответственны за зрение в условиях слабой освещенности и отключаются при ярком освещении. (Это является причиной того, что ночью невозможно уверенно различить цвета предметов. Ночью, как известно, «все кошки серы».)
Рисунок 1. Структурные элементы зрительной системы человека. В увеличенном фрагменте сетчатки показано относительное расположение трёх её слоёв. Задний слой сетчатки состоит из длинных и узких клеток фоторецепторов — палочек и колбочек. Средний слой содержит нейроны трёх типов: биполярные, горизонтальные (соединяющие рецепторы и биполярные клетки сравнительно длинными связями, параллельными сетчаточным слоям) и амакриновые клетки. В переднем слое находятся ганглиозные клетки, аксоны которых проходят по поверхности сетчатки, собираясь в пучок, и покидают глаз, образуя зрительный нерв.
[1], рисунок адаптирован
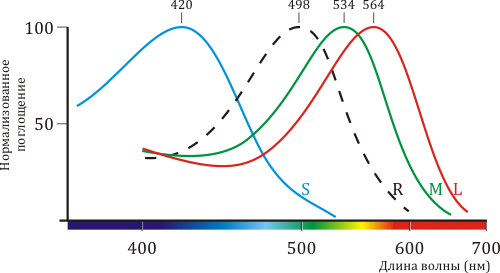
Мембраны колбочек содержат три типа рецепторов-опсинов, отвечающих за восприятие света с различными длинами волн, — синего, зеленого и красного пигментов. Аминокислотная последовательность, структура и механизм работы этих белков очень близки к таковым для родопсина, однако тонкие различия в белковом окружении светочувствительного кофактора (ретиналя) приводят к тому, что их спектральные характеристики различаются (рис. 2). В этой статье речь пойдет главным образом о зрительном родопсине, содержащемся в светочувствительных мембранах клеток-палочек.
Рисунок 2. Спектральные характеристики родопсина и трёх других типов опсинов. Цветное зрение приматов трихроматично, то есть определяется тремя типами клеток-«колбочек», содержащих каждая свой тип светочувствительного пигмента, по аминокислотной последовательности и структуре очень схожего с родопсином. На рисунке приведены нормализованные спектры поглощения «синего» (β), «зелено-голубого» (γ) и «жёлто-зеленого» (ρ) пигментов из S-, M- и L-колбочек, соответственно. Также показан спектр родопсина из клеток-«палочек» (обозначен пунктиром).
[2], рисунок адаптирован
История изучения родопсина
Открытие родопсина
Пурпурная окраска клеток-палочек была открыта Генрихом Мюллером (Heinrich Müller) в 1851 году, который приписал её гемоглобину. В 1876 году Франц Болл (Franz Boll) заметил, что сетчатка лягушки чувствительна к свету и после освещения меняет свою окраску на жёлтую с последующим обесцвечиванием. Болл также продемонстрировал, что сетчатка приобретает изначальную окраску после некоторого времени, проведенного животным в темноте. Вилли Кюхне (Willy Kühne), продолживший работы Болла, определил, что пигмент, отвечающий за окраску сетчатки — это белок наружных сегментов палочек (НСП), названный им «зрительным пурпуром» (родопсином).
Кюхне выделил родопсин из клеток пигментного эпителия сетчатки, сравнил спектроскопические свойства этого белка и препарата сетчатки, постулировал, что жёлтый и бесцветный продукты, образующиеся под действием света, химически различны и заключил, что генерация сетчаткой электрических импульсов является следствием реакции на свет. Работы Кюхне легли в основу современного понимания молекулярных механизмов зрения.
Ретиналь — светочувствительный кофактор
Джордж Уолд (George Wald) и его коллеги по Гарвардскому университету впервые открыли, что родопсин состоит из двух компонентов — бесцветного белка, называемого опсином или жёлтым пигментом и 11-цис-ретиналя, ковалентно связанного хромофора каротиноидной природы, акцептирующего свет.
В 1933 году Уолд выделил из препарата сетчатки вещество, первоначально идентифицированное как витамин А, что объяснило феномен «куриной слепоты» у пациентов с авитаминозом по этому каротиноиду (к тому времени еще мало было известно о биохимической роли витаминов). Позже оказалось, что кофактором является ретиналь — соответствующий витамину А (ацетату ретинола) альдегид. Уолд и коллеги продемонстрировали, что ретиналь, добавленный в темноте к обесцвеченному родопсину, способен восстанавливать «свежий» пигмент, причём этим действием обладает только 11-цис-изомер. В 1967 году Уолд получил Нобелевскую премию по физиологии и медицине «за исследования в области физиологии и биохимии зрения», а также за открытие биохимической роли витамина А.
На пути к пространственной структуре родопсина
Полная аминокислотная последовательность родопсина была определена в 1982 году в Институте биоорганической химии АН СССР Ю. А. Овчинниковым и сотр. [3] и несколько позже подтверждена анализом структурного гена родопсина Д. Хоггнесом и Дж. Натансом в США. Было показано, что в последовательности родопсина длиной 348 аминокислотных остатков присутствует семь протяжённых участков, состоящих из неполярных аминокислотных остатков, образующих трансмембранные (ТМ) α-спирали, соединенные вне- и внутриклеточными участками-«петлями». При этом N-конец находится во внеклеточной области, а C-конец — в цитоплазматической. Такая топология рецептора была подтверждена ограниченным протеолизом белка в составе нативной мембраны, обработкой моноклональными антителами и химической модификацией проникающими и непроникающими агентами. Также было установлено место прикрепления кофактора: ретиналь связывается альдиминной связью с остатком ЛИЗ-296, находящимся в седьмой (последней) ТМ α-спирали.
Пространственная структура родопсина долго не поддавалась изучению «прямыми» методами (такими как рентгеноструктурный анализ (РСА) и спектроскопия ядерного магнитного резонанса (ЯМР)). В то время как атомная структура другого мембранного белка со схожей семиспиральной топологией — бактериородопсина — была определена Гендерсоном и сотр. еще в 1990-м году [4], структура зрительного родопсина высокого разрешения оставалась неизвестной до 2000 года. Подробнее об этой структуре написано в главе «Структура родопсина».
Родопсин принадлежит к обширному семейству G-белоксопряжённых рецепторов (GPCR-рецепторов), названному так за механизм трансмембранной передачи сигнала, основанный на взаимодействии с внутриклеточными примембранными G-белками. Появление его пространственной структуры, полученной с высоким экспериментальным разрешением, является очень важным событием для биологии и медицины, поскольку родопсин как «родоначальник» семейства А GPCR-рецепторов является своего рода «моделью» структуры и функций множества других рецепторов, чрезвычайно интересных с фундаментальной и практической (фармакологической) точек зрения.
Молекулярная основа зрения
Строение фоторецепторных клеток
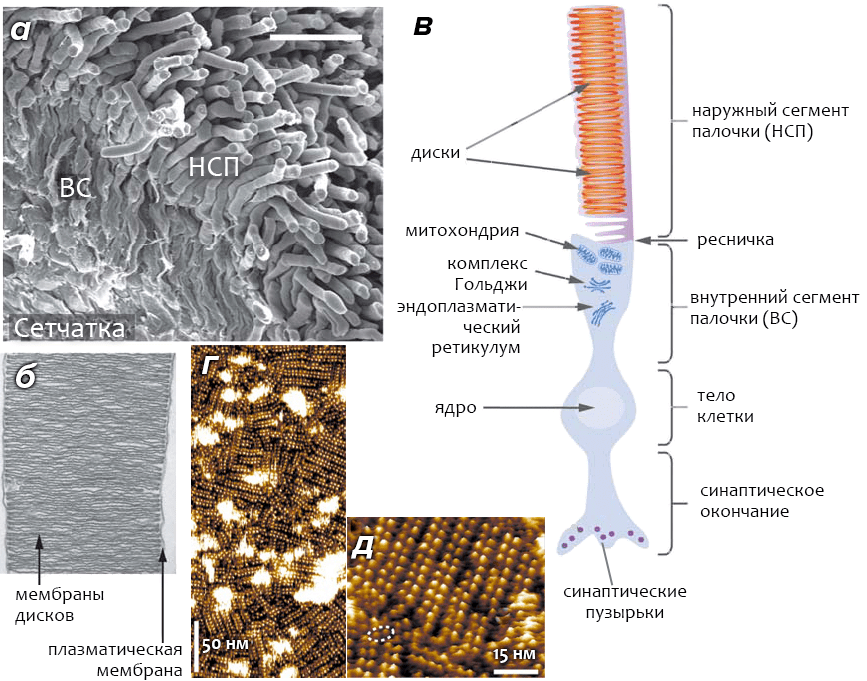
Клетки-«палочки» сетчатки (также известные как фоторецепторные клетки) — это высокоспециализированные нейроны, способные реагировать на свет. Особая часть клетки, называемая наружным сегменом палочки (НСП, см. рис. 3а), содержит 1000–2000 мембранных органелл, называемых дисками. Диски уложены в «стопки» (подобно блинам) и располагаются внутри общей с остальными частями клетки плазматической мембраны (рис. 3б). Диски как бы «отпочковываются» от плазматической мембраны, при этом их внутренняя область гомологична внеклеточному пространству (рис. 3в). Наружные сегменты колбочек имеют принципиальное отличие от НСП, заключающееся в том, что диски колбочек представляют собой складки плазматической мембраны (а не самостоятельные органеллы), и их внутреннее пространство сообщается с внеклеточной средой.
Рисунок 3. Строение сетчатки и зрительной клетки-фоторецептора — «палочки». а — Сканирующая электронная микрофотография сетчатки мыши. Палочки составляют ~70% из всех (6,4×106) клеток сетчатки, на долю колбочек приходится ~2%. Наружные сегменты палочек (НСП) содержат «диски», мембрана которых обогащена родопсином, а внутренние сегменты (ВС) отвечают за обеспечение клетки энергией и питательными веществами. б — Электронная микрофотография НСП, выделенного из сетчатки мыши. Молярное соотношение между родопсином и фосфолипидами мембраны «дисков» — ~1:60; доля других белков в мембране невелика, и их роль в процессе зрения пока остаётся невыясненной. в — Схематичное изображение клетки-палочки. Под действием света проницаемость мембраны НСП для ионов падает, что приводит к гиперполяризации и возникновению нервного импульса. г, д — Квазитопографическое изображение поверхности родопсин-содержащей мембраны диска, полученное с помощью атомно-силовой микроскопии в разном масштабе. Пунктирным овалом обведен димер родопсина, «выбившийся» из рядов, образуемых другими димерами. Считается, что активной формой рецептора, способной к реакции на свет, является именно димер.
а и б — [5], в — [6]
Основной белковый компонент (>90%) фоторецепторных мембран — родопсин, занимающий ~50% площади поверхности мембраны дисков (родопсин также присутствует в небольших количествах в плазматической мембране клетки). Мембрана дисков состоит из фосфолипидов (40% фосфатидилхолина, 38% фосфатидилэтаноламина, 13% фосфатидилсерина) и холестерина. Высокая доля ненасыщенных жирных кислот (~80%) делает фоторецепторную мембрану чрезвычайно жидкой, что имеет важное значения для функционирования родопсина.
В фоторецепторной мембране молекулы родопсина образуют димеры (см. главу «Взаимодействие родопсина с G–белком трансдуцином»), располагающиеся рядами (рис. 3г–д). Среднее число молекул родопсина на один диск — ~8×104, что в расчете на целую сетчатку даёт около 1014–1015 молекул фоторецептора.
Биохимический каскад зрения
В плазматической мембране НСП позвоночных, не сообщающейся с мембранами дисков, расположены специальные каналы, специфичные для катионов Na+ и Ca2+ и зависящие от циклического гуанозинмонофосфата (цГМФ). В темноте часть этих каналов открыта и названные катионы могут свободно диффундировать из внеклеточного пространства в цитозоль. Этот «темновой ток» ионов, открытый в 1970 году Вильямом Хейгинсом, вызывает деполяризацию плазматической мембраны НСП — «темновая» трансмембранная разность потенциалов НСП составляет ~50 мВ вместо обычных для нервной клетки 70 мВ. Как и «обычные» нейроны, палочки вырабатывают медиатор в ответ на деполяризацию, и таким образом получается, что в темноте фоторецепторы постоянно возбуждены и вырабатывают нервный импульс.
В результате поглощения кванта света молекулой родопсина инициируется цепь биохимических событий, следствием которой является закрытие катионных (Na+/Ca2+) каналов, уменьшение темнового тока и гиперполяризация плазматической мембраны (увеличение положительного заряда на внешней поверхности клетки). Свет, повышая разность потенциалов на мембране рецепторной клетки (гиперполяризуя её), уменьшает выделение медиатора, фактически «выключая» рецепторы. При этом эффективность биохимического каскада настолько высока (коэффициент усиления 105–106), что один-единственный (!) фотон может привести к гиперполяризации и быть зарегистрирован в зрительной коре мозга.
Поглощение родопсином кванта света приводит к ряду его фотохимических превращений, первым этапом которых является фотоизомеризация 11-цис-ретиналя в полностью транс-форму (подробнее об этом и других фотопревращениях родопсина см. в главе «Фотоцикл родопсина»). Изомеризация ретиналя, протекающая за очень короткое время в 200 фс, — единственный светозависимый процесс в зрительном цикле; остальные процессы сопряжены с конформационными перестройками в молекуле родопсина и являются следствием этого первичного акта поглощения света. Наибольшую важность для биохимических реакций, приводящих к возникновению фоторецепторного ответа, представляет один из интермедиатов фотолиза — метародопсин II (максимум на спектре поглощения λmax=380 нм), который содержит полностью транс-ретиналь и характеризуется значительными конформационными перестройками по сравнению с «темновой» формой родопсина.
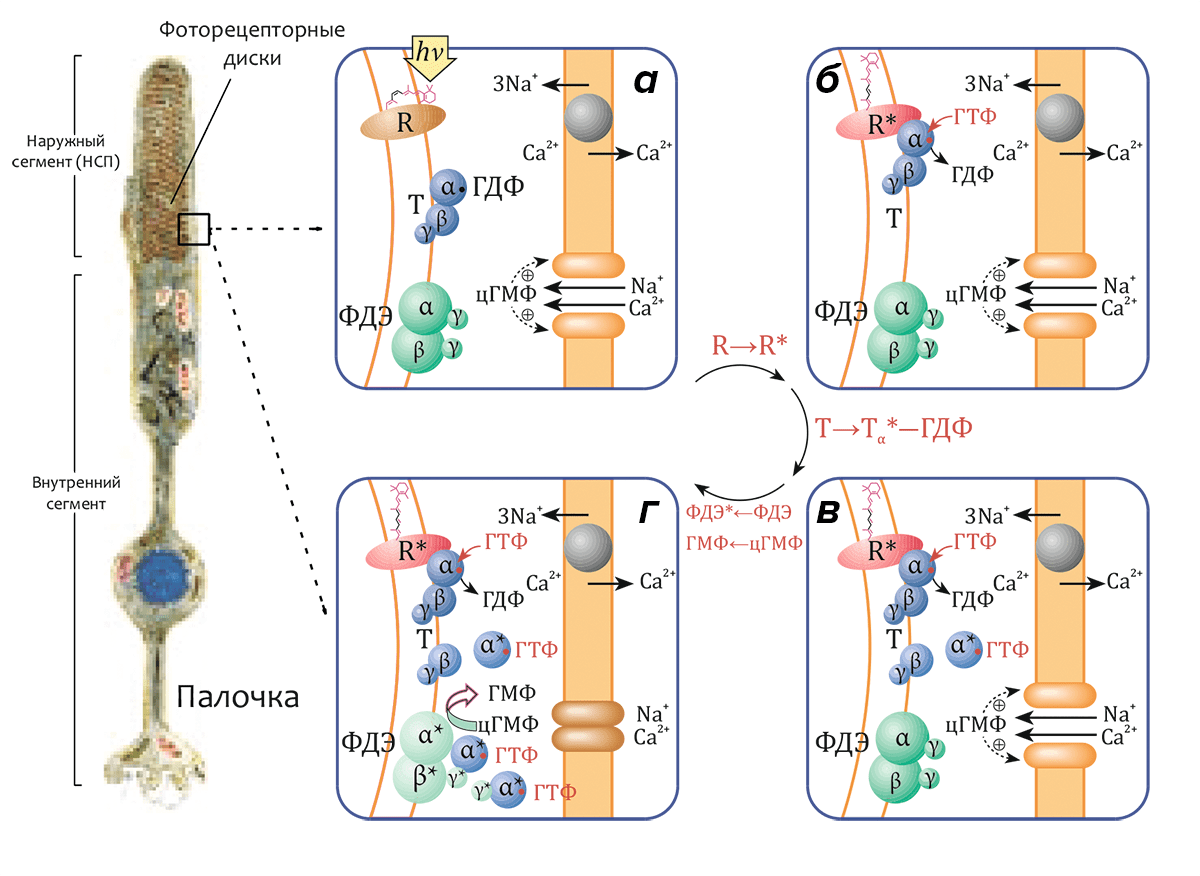
Метародопсин II (R*, «световая» или «активированная» форма родопсина R) способен связывать особый G-белок, называемый трансдуцином, передающий возбуждение, сконцентрированное на молекуле трансмембранного рецептора, в жидкую фазу цитоплазмы. Трансдуцин (Т) относится к семейству гетеротримерных G-белков и состоит из трех субъединиц (Тα, Тβ и Тγ с массами 40, 37 и 8 кДа соответственно), в первой из которых (Тα) находится сайт связывания гуанидиновых нуклеотидов ГДФ и ГТФ. В темноте (рис. 4а) Тα-субъединица содержит связанную молекулу ГДФ и образует комплекс с субъединицами Тβ и Тγ (функционирующими как димер Тβγ). Комплекс (Тα–ГДФ)–Тβγ имеет высокое сродство к метародопсину II (R*), и после реакции с ним молекула связанного ГДФ обменивается на ГТФ (рис. 4б). Комплекс R*–(Тα–ГТФ)–Тβγ быстро диссоциирует на R*, активный компонент Тα–ГТФ и димер Тβγ. Освобождённая молекула R* способна катализировать распад еще сотен или даже тысяч трансдуциновых комплексов (рис. 4в), что является первым этапом усиления сигнала в процессе передачи зрительного сигнала (см. также видео).
Активный комплекс Тα–ГТФ, в свою очередь, активирует следующий белок зрительного каскада — гетеротетрамерную фосфодиэстеразу (ФДЭ) циклического ГМФ (цГМФ). Активация этого белка, локализованного на поверхности мембран дисков, приводит к расщеплению эффекторной молекулы — до трех тысяч молекул цГМФ на одну молекулу активного фермента (рис. 4г) — и инактивации цГМФ-зависимых катионных каналов, приводящей к гиперполяризации плазматической мембраны.
Рисунок 4. Схема активации зрительного каскада. а — В «темновом» состоянии родопсин неактивен (R). α-субъединица трансдуцина (Т) находится в комплексе с ГДФ (Тα–ГДФ) и связана с димером β- и γ-субъединиц (Тβγ). цГМФ-диэстераза (ФДЭ) — гетеротетрамер, состоящий из двух гомологичных каталитических α- и β-субъединиц (ФДЭαβ) и двух идентичных γ-субъединиц, являющихся внутримолекулярными ингибиторами фермента, также неактивна. Гуанилатциклаза поддерживает высокий уровень цГМФ в цитоплазме. цГМФ-зависимые катионные каналы в плазматической мембране открыты, и катионы Na+ и Ca2+ могут диффундировать из внеклеточного пространства в цитозоль. Внутриклеточная концентрация Ca2+ поддерживается на постоянном уровне находящимся в плазматической мембране Na+/Ca2+,K+-катионообменником. б — В результате поглощения кванта света родопсин переходит в активное состояние (R→R*). Активный R* связывается с трансдуцином и индуцирует обмен связанного с Тα ГДФ на ГТФ (см. видео). в — Комплекс R*–(Тα–ГТФ)–Тβγ диссоциирует на R*, Тβγ и активный комплекс Тα*–ГТФ, после чего R* способен активировать другую молекулу трансдуцина. г — Тα*–ГТФ активирует ФДЭ (ФДЭαβ*), которая гидролизует множество молекул цГМФ. Снижение внутриклеточной концентрации цГМФ приводит к закрытию цГМФ-зависимых каналов, что влечет за собой гиперполяризацию плазматической мембраны. Слева приведено схематическое изображение палочки сетчатки.
[1], рисунок адаптирован
Электрофизиологический эффект фоторецепторной клетки на световой стимул длится в течение сотен миллисекунд, а затем прекращается благодаря специальным механизмам, «выключающим» фосфодиэстеразный каскад и восстанавливающим «темновое» состояние. «Активированная» форма родопсина (R*) трижды фосфорилирована в C-конце (см. главу «Трансмембранная топология»), и имеет сродство к цитоплазматическому белку аррестину, который блокирует взаимодействие с трансдуцином и участвует в десенсибилизации и деградации рецептора. Подробнее об этом механизме см. в статье В.М. Липкина в «Соросовском образовательном журнале» [1].
Фотоцикл родопсина
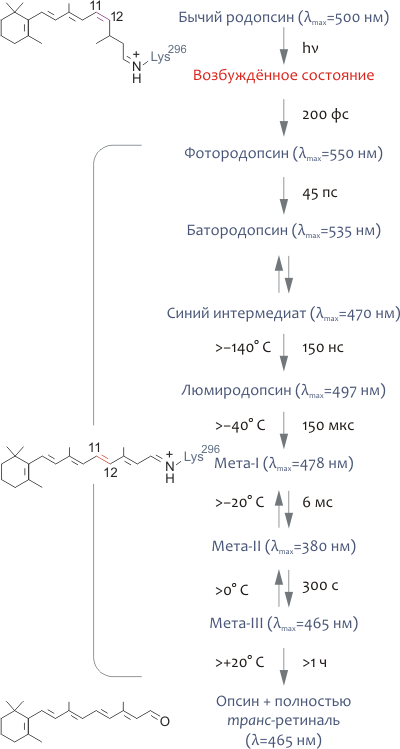
При поглощении фотона молекула родопсина меняет цвет, что связано с фотоизомеризацией 11-цис-ретиналя в полностью транс-форму и смещением максимума спектра поглощения рецептора с 498 нм до 380 нм (рис. 5). В конце концов, Шиффово основание гидролизуется и полностью транс-ретиналь выделяется в цитоплазматическую среду. Изменение спектральных характеристик родопсина, следующее за поглощением кванта света, объясняется конформационными перестройками, вызванными изомеризацией ретиналя. В большом количестве спектроскопических экспериментов с охлаждением родопсина до очень низких температур был выделен ряд промежуточных его состояний (рис. 5), что позволило охарактеризовать последовательность фотопревращений родопсина следующим образом:
- Ещё до начала каких-либо структурных перестроек родопсина энергия света аккумулируется молекулой хромофора в сильно искажённой полностью транс-форме, расположенной в том же белковом сайте связывания, где находится 11-цис-ретиналь в темноте. «Напряжённая» конформация изомеризованного хромофора трансформирует свою энергию в дальнейшие конформационные изменения родопсина.
- Фотоизомеризация хромофора чрезвычайно быстра и занимает всего 200 фс.
- Состояние мета-I (рис. 5) является переходным и довольно быстро превращается в мета II, являющееся «главным действующим лицом» биохимического каскада зрения.
- Фотоинтермедиат мета-II — физиологически и биохимически наиболее важное промежуточное состояние родопсина, поскольку именно оно ответственно за взаимодействие с примембранными белками, среди которых можно назвать и трансдуцин.
- Опсин спонтанно рекомбинирует с 11-цис-ретиналем, возвращаясь в «темновую» форму родопсина. В отличие от опсина, родопсину не свойственна «базальная» активность (т.е., в «темновой» форме он не имеет сродства к G-белку (трансдуцину)). Это обстоятельство определяет очень низкий активационный порог для клеток-«палочек» (или, что то же, высокую чувствительность).
Рисунок 5. Фотоцикл родопсина. Поглощение кванта света с длиной волны, близкой к 500 нм, приводит к чрезвычайно быстрой (200 фс) изомеризации ковалентно связанного хромофора 11-цис-ретиналя в полностью транс-форму. Как следствие, родопсин претерпевает ряд быстрых конформационных перестроек, различимых спектроскопически, и в результате превращается в сравнительно долгоживущий метародопсин-II, или мета-II, существующий в равновесии с мета-I формой. В итоге фотопревращений родопсина, полностью транс-ретиналь выделяется в цитоплазму, восстанавливается до полностью транс-ретинола (при участии ряда ретинол дегидрогеназ) и конвертируется обратно в 11-цис-ретиналь в клетках пигментного эпителия под действием специальных ферментов (так называемый ретиноидный цикл). «Восстановленный» хромофор может спонтанно рекомбинировать с опсином, превращаясь в «темновую» форму родопсина. На рисунке справа от стрелок указаны характерные времена того или иного превращения, а слева — максимальные температуры, при которых фотоинтермедиат удавалось наблюдать in vitro. В скобках указаны максимумы соответствующих спектров поглощения.
[8], рисунок модифицирован
В бόльших подробностях с фотопревращениями родопсина можно ознакомиться в [7].
Структура родопсина
Трансмембранная топология
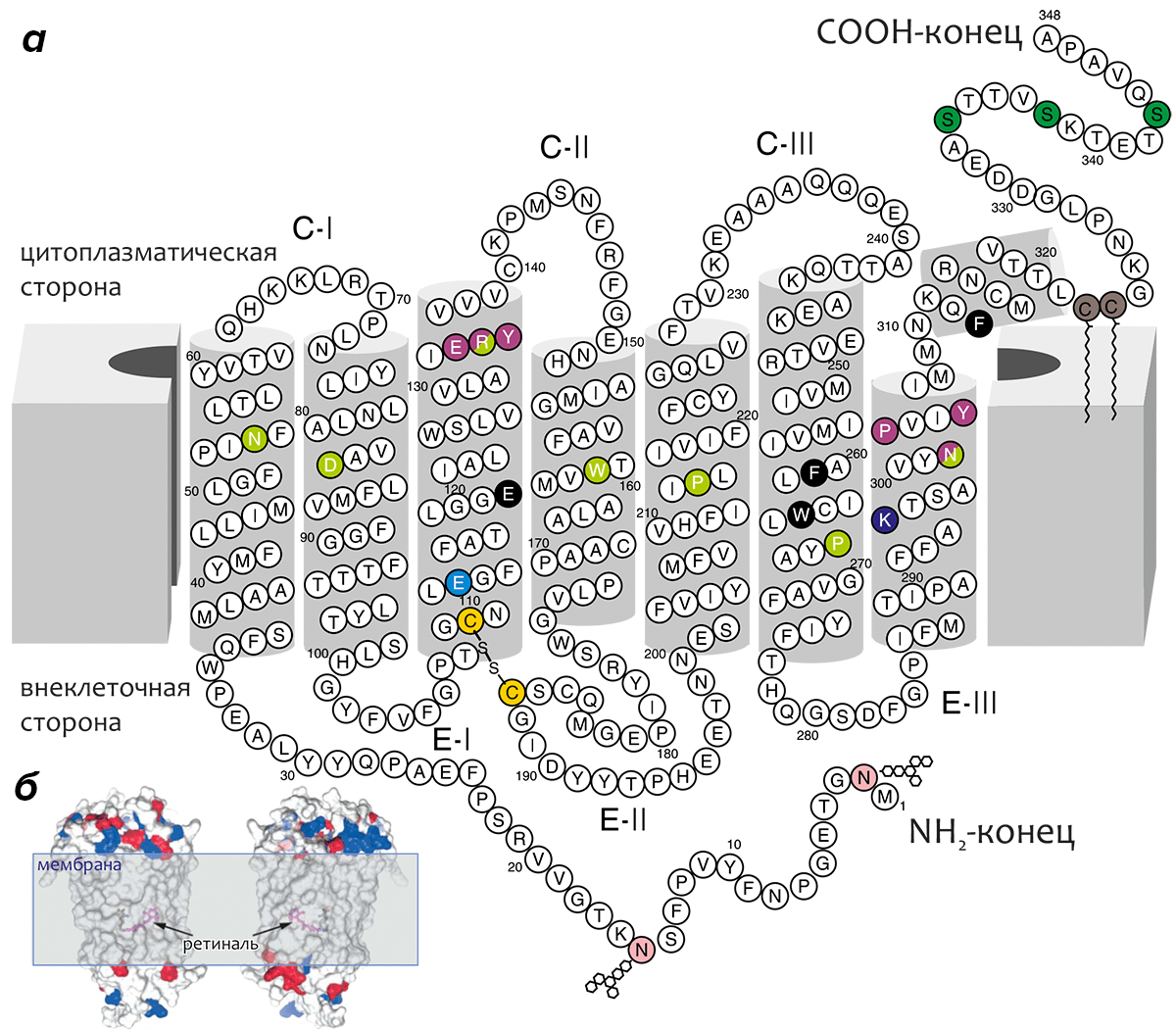
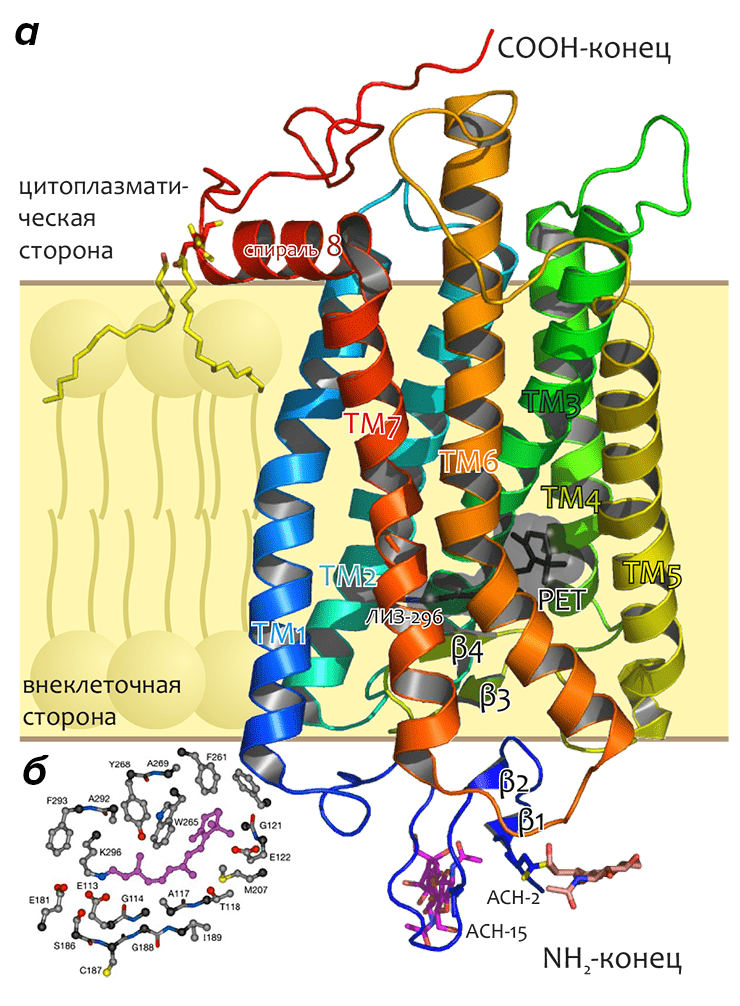
Родопсин — интегральный мембранный белок цилиндрической формы (размеры ~75×35×45 Å), трансмембранная (ТМ) часть которого образована «пучком» α-спиралей, уложенных по циклическому принципу в направлении против часовой стрелки (при виде с внеклеточной стороны) и примерно ортогональных плоскости мембраны, причем спираль ТМ3 расположена практически в центре «пучка» (рис. 6). Геометрия многих спиралей отклоняется от «идеальной» (т.е., содержит «изломы»); сильнее всего искажена спираль ТМ6 за счет влияния остатка ПРО-267 (одного из наиболее консервативных во всем семействе GPCR-рецепторов, «родоначальником» подсемейства А которых является родопсин).
Рисунок 6. Трансмембранная топология родопсина. а — «Двумерная» модель родопсина, объясняющая способ его упаковки в мембране. C-I–CIII и E-I–EIII — цитоплазматические и внеклеточные петлевые участки, соответственно. Трансмембранный домен образован α-спиралями (серые цилиндры), геометрия многих из которых отклоняется от «идеальной». Стабильность ТМ-пучка усиливается консервативной во многих GPCR-рецепторах дисульфидной связью между остатками цистеина в ТМ3 и E-II (показаны золотым). Хромофор — 11-цис-ретиналь — не изображён на рисунке; он присоединяется к остатку ЛИЗ-296 в ТМ7 (показан фиолетовым) через протонированное Шиффово основание. Положительный заряд этой альдиминной связи нейтрализуется остатком глутаминовой кислоты ГЛЮ-113 (показан голубым). Остатки аспарагина АСН-2 и АСН-15 (показаны розовым) гликозилированы ГЛЮ-N-Ац-(β1,4)-ГЛЮ-N-Ац-(β1,4)-МАН (ГЛЮ — глюкоза, МАН — манноза); МЕТ-1 ацетилирован. Два остатка цистеина в примембранной спирали 8 (показаны коричневым) пальмитоилированы. Три остатка серина в C-конце рецептора, фосфорилирующиеся в процессе фотоактивации родопсина, показаны темно-зеленым. Эти остатки в фосфорилированной форме отвечают за взаимодействие с белком аррестином, отвечающим за инактивацию и десенсибилизацию родопсина. Два консервативных мотива, важных для активации рецептора и взаимодействия с трансдуцином, (D/E)RY в ТМ3 и NPxxY в ТМ7, показаны малиновым. Наиболее консервативные во всем семействе GPCR-рецепторов остатки для каждой ТМ-спирали показаны салатовым. Некоторые другие функционально важные остатки выведены на черном фоне. Схема ТМ топологии родопсина предложена Харгрэйвом [9] и Овчинниковым [3], [10]. б — Расположение родопсина в мембране (изображён в виде молекулярной поверхности, окрашенной в соответствии с зарядом остатка: отрицательный — красный, положительный — синий). (Положение вне- и внутриклеточного пространства то же, что и в а, масштаб другой.) Положение хромофора показано с помощью удаления некоторых спиралей из структуры. Молекула родопсина показана с двух противоположных сторон.
Длина аминокислотной последовательности родопсина — 348 остатков, масса белка — около 38 кДа, а длина ТМ спиралей варьирует от 20 до 33 остатков. ТМ домен белка составляет ~65% его общей массы, а размеры вне- и внутриклеточных областей примерно равны. Хромофор (ретиналь) связывается в ТМ области белка, ковалентно присоединяясь к остатку ЛИЗ-296.
Внеклеточный домен родопсина образован N-концевым участком, а также «петлями» E-I–E-III, и содержит два сайта гликозилирования по остаткам аспарагина. N-конец и внеклеточная петля II (E-II) содержат пары β-структурных «шпилек» β1–β2 и β3–β4, причём последние связаны консервативной дисульфидной связью со спиралью ТМ3, как бы «накрывая» сайт связывания ретиналя «крышкой». Цитоплазматический домен образован петлями C-I–C-III и C-концевым участком молекулы. В состав С-конца входит примембранная амфифильная спираль 8, «заякоренная» в мембране двумя остатками пальмитоиловой кислоты, присоединёнными к остаткам цистеина в этой спирали. В C-конце также находится три остатка серина, по которым предположительно происходит фосфорилирование рецептора, связанное с его активацией (рис. 6).
Многочисленные мутагенетические эксперименты позволили выяснить роль некоторых консервативных остатков, находящихся в ТМ области родопсина. Так, консервативный мотив (D/E)R(Y/W), находящийся в цитоплазматическом конце ТМ3, регулирует конформационные перестройки, сопровождающие активацию рецептора. Остаток глутаминовой или аспарагиновой кислоты (ГЛЮ-134 в родопсине) образует солевой мостик с консервативным остатком аргинина, способствуя «удержанию» рецептора в неактивной конформации (мутация кислотной функции этого остатка приводит к получению постоянно активных форм родопсина, не зависящих от влияния света). Протонирование ГЛЮ-134, происходящее при образовании первичного фотоинтермедиата родопсина, приводит к дальнейшим конформационным перестройкам и возникновению мета-II состояния (см. главу «Фотоцикл родопсина»). Другой консервативный мотив, находящийся в цитоплазматическом конце ТМ7 — NPxxY (NPVIY в родопсине, тут “x” обозначает любой остаток) — связывают с образованием комплекса с G-белком трансдуцином.
В целом, практически любой заряженный или полярный остаток, находящийся в ТМ домене, играет свою важную для функционирования и/или создания «архитектуры» рецептора роль. Многие полярные остатки образуют «сети» водородных связей, в которых иногда участвуют молекулы воды, связанные в ТМ домене. Эти системы довольно слабых связей также важны для функционирования такой точно настроенной молекулярной структуры, как рецептор. Причём, полярные остатки ТМ домена, как правило, заглублены в белковое окружение, а «боковую» поверхность рецептора, взаимодействующую с неполярной областью бислойной мембраны, образуют незаряженные и неполярные гидрофобные остатки (рис. 6б).
Пространственная структура
Пространственная структура родопсина была впервые определена в 2000 году с помощью метода рентгеновской кристаллографии [11], и в последствии несколько раз уточнялась. До сих пор она остаётся единственной трехмерной структурой GPCR-рецептора, экспериментально полученной с высоким разрешением. Структуры других белков этого семейства до сих пор неизвестны, поскольку эти рецепторы очень сложно выделить в необходимом для метода РСА количестве и подобрать условия, в которых белок будет образовывать кристалл, дающий чёткую дифракционную картину. Методу спектроскопии ЯМР такие большие и сложно устроенные мембранные белки пока что недоступны.
В десятилетие, прошедшее с момента получения структуры бактериородопсина (белка со схожим устройством) [4] до появления структуры фоторецептора с высоким разрешением, с помощью метода криоэлектронной микроскопии была получена структура родопсина низкого разрешения [12]. На основе этой структуры с учётом вариабельности аминокислотной последовательности родопсина в различных организмах был предложен «шаблон» расположения Cα-атомов этого рецептора и других рецепторов семейства GPCR [13]. Эти модели показали отличное (по сравнению с бактериородопсином) расположение ТМ спирали 3 (ТМ3) по отношению к другим спиралям, но другие особенности строения родопсина оставались до недавнего времени неизвестными.
Структура родопсина (рис. 7) демонстрирует немного отличающуюся от таковой в бактериородопсине упаковку спиралей: они расположены под бóльшими углами к нормали к мембране, во многих случаях сильнее искажены. Кроме того, ТМ3 почти полностью окружена остальными спиралями, в то время как в бактериородопсине спирали расположены почти точно по эллипсу, в направлении против часовой стрелки при виде с внеклеточной стороны (в родопсине это направление укладки сохраняется).
Рисунок 7. Пространственная структура зрительного родопсина. а — Молекула изображена в виде ленты, обозначающей расположение основной цепи белка. N— и C-концы, а также ТМ спирали подписаны. Показаны боковые цепи двух остатков аспарагина, модифицированные молекулами углеводов, двух остатков цистеина, модифицированных пальмитоиловой кислотой, «заякоривающей» примембранную амфифильную спираль 8 в мембране, а также остатка лизина-296, образующего ковалентную связь с хромофором (структура ретиналя (РЕТ) показана черным цветом внутри полупрозрачной ван-дер-ваальсовой поверхности). Положение мембраны схематично показано жёлтым слоем. Рисунок построен на основе структуры 1U19 из Брукхейвенского банка данных белковых структур (доступны также другие структуры родопсина: 1F88, 1GZM, 1HZX, 1L9H). б — Схематическое изображение остатков, формирующих сайт связывания ретиналя в родопсине (показаны боковые цепи остатков, расположенных не далее, чем на 5 Å от хромофора).
Структурные исследования родопсина помогли установить роль молекул воды, находящихся в ТМ домене рецептора и определить конформации вне- и внутриклеточных петель родопсина. Основываясь на этих исследованиях, были предложены возможные механизмы активации белка и участия функционально важных групп и микродоменов в ТМ передаче сигнала и конформационных перестройках, связанных с поглощением света. Подробнее об этом можно почитать в недавнем обзоре Кристофа Пальцевского (Krzysztof Palczewski) [14], одного из наиболее активных участников упомянутых исследований.
Димеризация родопсина в мембране
С помощью атомно-силовой микроскопии нативных дисковых мембран показано (и подтверждено биохимическими методами), что родопсин образует димеры и даже олигомеры более высокого порядка, выстраивающиеся в «ряды» димеров с вкраплениями олигомеров (см. главу «Строение фоторецепторных клеток», [5], [6]). В настоящее время появляются свидетельства того, что именно димеры родопсина (и других GPCR-рецепторов) являются функционально активными формами [15], но механизм их димеризации и роль этого процесса в работе рецептора пока еще недостаточно хорошо изучены.
Взаимодействие родопсина с G–белком трансдуцином
Взаимодействие активированной формы родопсина с G-белком трансдуцином является ключевым биохимическим аспектом в зрительном процессе (см. главу «Биохимический каскад зрения»). Точный механизм этого процесса неизвестен, поскольку отсутствует структурная информация высокого разрешения об активированной форме родопсина, однако показано, что во взаимодействии с G-белком существенную роль может играть димеризация рецепторов.
Предположительно, с G-белком взаимодействует димер рецептора, одна молекула в составе которого «активирована» и взаимодействует с трансдуцином, а другая может быть неактивной (или даже быть другим GPCR-рецептором) и G-белок не активирует. По данным атомно-силовой микроскопии [6], димер образуется с участием спиралей ТМ4 и ТМ5. Конформационные перестройки, сопровождающие активацию родопсина, приводят к тому, что цитоплазматическая часть рецептора, находящаяся вблизи консервативных мотивов, участвующих в активации родопсина ([D/E]RY в ТМ3 и NPxxY в ТМ7), меняет свое строение. Солевой мостик, связывающий остатки ГЛЮ-134 и АРГ-135, разрушается (что связано с протонированием ГЛЮ-134 и депротонированием Шиффова основания ретиналя в ЛИЗ-296), и петлевые цитоплазматические участки родопсина приобретают сродство к трансдуцину. Схематически предполагаемый процесс взаимодействия родопсина с трансдуцином показан ниже в видео, основанном на биохимических данных и кристаллографических структурах родопсина и субъединиц трансдуцина.
Видео. Возможный механизм взаимодействия родопсина («темновая» форма — синий, «активированная» — жёлтый) с трансдуцином (Tα — оранжевый, Tβ — красный, Tγ — зелёный). Молекула ГТФ показана фиолетовым, ГДФ — светло-фиолетовым. Анимация основана на данных атомно-силовой микроскопии [5] и молекулярного моделирования с использованием индивидуальных кристаллографических структур родопсина и трансдуцина [15].
Перспективы исследования родопсина
Структурные исследования родопсина продолжаются, и среди вопросов, ждущих своего разрешения, можно назвать следующие:
- Какие структурные превращения сопровождают активацию родопсина и придают ему способность взаимодействовать с белками-партнерами (такими как трансдуцин, белки-киназы и аррестин)?
- Каковы пространственные структуры комплексов активированного состояния родопсина и трансдуцина, а также мономера или димера фосфорилированного активированного родопсина и аррестина?
- Какую роль играет димеризация GPCR-рецепторов в трансмембранной передаче импульсов и десенсибилизации рецепторов?
- Каким образом «отработанная» молекула полностью транс-ретиналя высвобождается из сайта связывания в родопсине, и как 11-цис-ретиналь встраивается обратно?
- Каков механизм клеточного «созревания» и деградации родопсина?
Дальнейшее исследование родопсина имеет не только фундаментальное значение и может быть использовано не только для лечения или предотвращения биохимических нарушений зрения. Родопсин — самый разносторонне исследованный белок из семейства GPCR-рецепторов, и закономерности, полученные для него, могут быть использованы для изучения структуры и функциональных особенностей других рецепторов этого семейства. С дисфункцией этих белков связано огромное количество заболеваний [16], и изучение их структуры и, главное, механизма взаимодействия с лигандами, может открыть новые возможности для дизайна новых лекарственных веществ [17] — эффективных и безопасных.
- Липкин В.М. (2001). Зрительная система. Механизмы передачи и усиления зрительного сигнала в сетчатке глаза. Соросовский образовательный журнал. 9, 2–8;
- Википедия: Color vision (англ.);
- Овчинников Ю.А., Абдулаев Н.Г., Фейгина М.Ю., Артамонов И.Д., Богачук А.С. (1983). Зрительный родопсин: Полная аминокислотная последовательность и топология в мембране. Биоорганическая химия. 10, 1331–1340;
- R. Henderson, J.M. Baldwin, T.A. Ceska, F. Zemlin, E. Beckmann, K.H. Downing. (1990). Model for the structure of bacteriorhodopsin based on high-resolution electron cryo-microscopy. Journal of Molecular Biology. 213, 899-929;
- Y. Liang, D. Fotiadis, T. Maeda, A. Maeda, A. Modzelewska, et. al.. (2004). Rhodopsin Signaling and Organization in Heterozygote Rhodopsin Knockout Mice. Journal of Biological Chemistry. 279, 48189-48196;
- Dimitrios Fotiadis, Yan Liang, Slawomir Filipek, David A. Saperstein, Andreas Engel, Krzysztof Palczewski. (2003). Atomic-force microscopy: Rhodopsin dimers in native disc membranes. Nature. 421, 127-128;
- Рубин А.Б. Фотопревращения бактериородопсина и родопсина // Биофизика, т.2. М.: Наука, 2004;
- Y. Shichida, H. Imai. (1998). Visual pigment: G-protein-coupled receptor for light signals. Cellular and Molecular Life Sciences (CMLS). 54, 1299-1315;
- Hargrave P.A., McDowell J.H., Curtis D.R., Wang J.K., Juszczak E., Fong S.L. et al. (1983). The structure of bovine rhodopsin. Biophys. Struct. Mech. 9, 235–244;
- Овчинников Ю.А. Зрительный родопсин // Биоорганическая химия. М.: Просвещение, 1987;
- Palczewski K., Kumasaka T., Hori T., Behnke C.A., Motoshima H., Fox B.A. et al. (2000). Crystal structure of rhodopsin: a G-protein-coupled receptor. Science. 289, 739–745;
- Schertler G.F. and Hargrave P.A. (1995). Projection structure of frog rhodopsin in two crystal forms. Proc. Natl. Acad. Sci. USA. 92, 11578–11582;
- Joyce M Baldwin, Gebhard F.X Schertler, Vinzenz M Unger. (1997). An alpha-carbon template for the transmembrane helices in the rhodopsin family of G-protein-coupled receptors. Journal of Molecular Biology. 272, 144-164;
- Krzysztof Palczewski. (2006). G Protein–Coupled Receptor Rhodopsin. Annu. Rev. Biochem.. 75, 743-767;
- Paul S.-H. Park, Slawomir Filipek, James W. Wells, Krzysztof Palczewski. (2004). Oligomerization of G Protein-Coupled Receptors: Past, Present, and Future†. Biochemistry. 43, 15643-15656;
- Torsten Schöneberg, Angela Schulz, Heike Biebermann, Thomas Hermsdorf, Holger Römpler, Katrin Sangkuhl. (2004). Mutant G-protein-coupled receptors as a cause of human diseases. Pharmacology & Therapeutics. 104, 173-206;
- Драг-дизайн: как в современном мире создаются новые лекарства.