Мотонейроны периферические (альфа- и гамма-мотонейроны)
Периферические
мотонейроны подразделяются на
альфа-мотонейроны и гамма-мотонейроны
(рис.
21.2 ).
Меньшие
по размеру гамма-мотонейроны
иннервируют интрафузальные
мышечные волокна .
Активация гамма-мотонейронов увеличивает
растяжение мышечных веретен, тем самым
облегчаясухожильные и
другие рефлексы, замыкающиеся через
альфа-мотонейроны.
Каждую
мышцу иннервирует несколько сотен
альфа-мотонейронов. В свою очередь,
каждый альфа-мотонейрон иннервирует
множество мышечных волокон — около
двадцати в наружных
мышцах глаза и
сотни в мышцах
конечностей и туловища .
В
нервно-мышечных синапсах
выделяется ацетилхолин .
Аксоны периферических
мотонейронов идут в составе черепных
нервов и передних
корешков спинного мозга .
На уровне межпозвоночных
отверстий передние
корешки и задние
корешкисливаются,
образуя спинномозговые
нервы .
Несколько соседних спинномозговых
нервов образуют сплетение, а затем
разветвляются на периферические
нервы .
Последние тоже неоднократно разветвляются
и иннервируют несколько мышц. Наконец,
аксон каждого альфа-мотонейрона образует
многочисленные разветвления, иннервируя
многие мышечные волокна.
Каждый
альфа-мотонейрон получает прямые
возбуждающие глутаматергические входы
откорковых
мотонейронов и
от чувствительных
нейронов ,
иннервирующих мышечные
веретена .
Возбуждающие влияния поступают также
к альфа- и гамма-мотонейронам от двигательных
ядер ствола мозга и вставочных
нейронов спинного мозга —
как по прямым путям, так и с переключениями.
Прямое
постсинаптическое торможение
альфа-мотонейронов осуществляют клетки
Реншоу —
вставочные глицинергические
нейроны .
Непрямое пресинаптическое торможение
альфа-мотонейронов и непрямое
пресинаптическое торможение
гамма-мотонейронов обеспечивают
другие нейроны ,
образующие ГАМКергические синапсы на
нейронах задних
рогов .
Тормозное
действие на альфа- и гамма-мотонейроны
оказывают и другие вставочные нейроны
спинного мозга, а также двигательные
ядра ствола мозга .
Если
преобладают возбуждающие входы, группа
периферических мотонейронов активируется.
Вначале возбуждаются мелкие мотонейроны.
По мере того как сила сокращения мышцы
нарастает, частота их разрядов нарастает
и вовлекаются крупные мотонейроны. При
максимальном сокращении мышцы возбуждена
вся соответствующая группа мотонейронов.
Нейронные структуры и их свойства
Тела
чувствительных клеток вынесены за
пределы спинного мозга (рис.9.1.). Часть
из них располагается в спинальных
ганглиях. Это тела соматических
афферентов, иннервирующих в основном
скелетные мышцы. Другие находятся в
экстра- и интрамуральных ганглиях
автономной нервной системы и обеспечивают
чувствительность только внутренних
органов.
Чувствительные
клетки имеют один отросток, который
вскоре после отхождения от тела клетки
делится на две ветви.
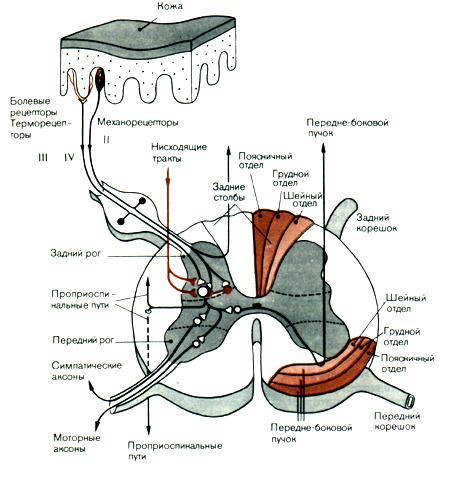
Рис.9.1.
Поперечное сечение спинного мозга и
связи кожных афферентов в спинном мозгу.
Одна
из них проводит возбуждение от рецепторов
к телу клетки, другая — от тела нервной
клетки к нейронам спинного или головного
мозга. Распространение возбуждения из
одной ветви в другую может происходить
без участия тела клетки.
Нервные
волокна чувствительных клеток по
скорости проведения возбуждения и
диаметру классифицируют на А-, В- и
С-группы. Толстые миелинизированные А-волокна с
диаметром от 3 до 22 мкм и скоростью
проведения возбуждения от 12 до 120 м/с
разбиваются еще на подгруппы: альфа—
волокна от мышечных рецепторов, бета —
от тактильных рецепторов и
барорецепторов,дельта —
от терморецепторов, механорецепторов,
болевых рецепторов. К волокнам
группы В относят
миелиновые отростки средней толщины
со скоростью проведения возбуждения
3-14 м/с. По ним в основном передается
ощущение боли. К афферентным волокнам
типа С относится
большинство безмиелиновых волокон
толщиной не более 2 мкм и скоростью
проведения до 2 м/с. Это волокна от
болевых, хемо- и некоторых механорецепторов.
Сам
спинной мозг в целом содержит, например,
у человека примерно 13 млн. нейронов. Из
их общего числа только около 3% составляют
эфферентные, двигательные или моторные
нейроны, а остальные 97 % приходятся на
долю вставочных, или интернейронов.
Двигательные нейроны являются выходными
клетками спинного мозга. Среди них
различают альфа- и гамма-мотонейроны,
а также преганглионарные нейроны
автономной нервной системы.
Альфа-мотонейроны осуществляют
передачу скелетным мышечным волокнам
сигналов, выработанных в спинном мозгу.
Аксоны каждого мотонейрона многократно
делятся, и, таким образом, каждый из них
охватывает своими терминалями до сотни
мышечных волокон, образуя в совокупности
с ними двигательную
единицу.
В свою очередь, несколько мотонейронов,
иннервирующих одну и ту же мышцу,
образуют мотонейронный
пул,
В его состав могут входить мотонейроны
нескольких соседних сегментов. В связи
с тем что возбудимость мотонейронов
пула неодинакова, при слабых раздражениях
возбуждается только часть из них. Это
влечет за собой сокращение лишь части
мышечных волокон. Другие моторные
единицы, для которых это раздражение
является подпороговым, тоже реагируют,
хотя их реакция выражается лишь в
деполяризации мембраны и повышении
возбудимости. С усилением раздражения
они еще больше вовлекаются в реакцию,
и, таким образом, все двигательные
единицы пула участвуют в рефлекторном
ответе.
Максимальная
частота воспроизведения ПД в
альфа-мотонейроне не превышает 200-300
имп/с. Вслед за ПД, амплитуда которого
составляет 80-100 мВ, возникает следовая
гиперполяризациядлительностью
от 50 до 150 мс. По частоте импульсации и
выраженности следовой гиперполяризации
мотонейроны разделяют на две группы:
фазические и тонические. Особенности
их возбуждения коррелируют с функциональными
свойствами иннервируемых мышц.
Фазически-ми мотонейронами иннервируются
более быстрые, «белые» мышцы,
тоническими — более медленные, «красные»
.
В
организации функции альфа-мотонейронов
важным звеном является наличие системы
отрицательной обратной связи,
образованной аксонными коллатералями
и специальными тормозными вставочными
нейронами — клетками Реншоу. Своими
возвратными тормозными влияниями они
могут охватывать большие группы
мотонейронов, обеспечивая, таким образом,
интеграцию процессов возбуждения и
торможения.
Гамма-мотонейроны иннервируют
интрафузальные (внутриверетенные)
мышечные волокна. Они разряжаются с
более низкой частотой, и следовая
гиперполяризация у них выражена слабее,
чем у альфа-мотонейронов. Их функциональное
значение сводится к сокращению
интрафузальных мышечных волокон, не
приводящему, однако, к появлению
двигательного ответа. Возбуждение этих
волокон сопровождается изменением
чувствительности их рецепторов к
сокращению или расслаблению экстрафузальных
мышечных волокон.
Нейроны
автономной нервной системы составляют
особую группу клеток. Тела симпатических
нейронов,
аксоны которых являются преганглионарными
волокнами, располагаются в
интермедиолатеральном ядре спинного
мозга. По своим свойствам они относятся
к группе B-волокон. Характерной особенностью
их функционирования является низкая
частота свойственной им постоянной
тонической импульсной активности. Одни
из этих волокон участвуют в поддержании
сосудистого тонуса, другие — обеспечивают
регуляцию висцеральных эффекторных
структур (гладкой мускулатуры
пищеварительной системы, железистых
клеток).
Тела парасимпатических
нейронов образуют
крестцовые парасимпатические ядра. Они
располагаются в сером веществе крестцовых
сегментов спинного мозга. Для многих
из них характерна фоновая импульсная
активность, частота которой возрастает
по мере повышения давления в мочевом
пузыре. При раздражении висцеральных
тазовых афферентных волокон в этих
эфферентных клетках регистрируется
вызванный разряд, характеризующийся
чрезвычайно большим латентным периодом.
К вставочным,
или интернейронам,
спинного мозга относятся нервные клетки,
аксоны которых не выходят за его пределы.
В зависимости от хода отростков различают
собственно спинальные и проекционные. Спинальные
интернейроны ветвятся
в пределах нескольких смежных сегментов,
образуя внутрисегментарные и
межсегментарные связи. Наряду с ними
существуют интернейроны, аксоны которых
проходят через несколько сегментов или
даже из одного отдела спинного мозга в
другой. Их аксоны образуют собственные
пучки спинного мозга.
К проекционным
интернейронам относятся
клетки, длинные аксоны которых формируют
восходящие пути спинного мозга. На
каждом интернейроне расположено в
среднем около 500 синапсов. Синаптические
влияния в них опосредуются через ВПСП
и ТПСП, суммация которых и достижение
критического уровня приводят к
возникновению распространяющегося ПД.
Соседние файлы в папке Нейрофизиология
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
- #
Спастический паралич
Параличом называют полное выпадение произвольных
движений в тех или иных мышечных группах, парезом — частичное (неполное)
выпадение произвольных движений. Напомним, что для осуществления
произвольных движений необходима сохранность корково-мышечного пути —
двухнейронного пути, соединяющего кору больших полушарий мозга со
скелетной (поперечно-полосатой) мускулатурой. Тело первого (верхнего,
или центрального) нейрона находится в коре прецентральной извилины, его
аксон направляется для образования синапса со вторым (нижним, или
периферическим) двигательным нейроном, находящимся в спинном мозге.
Аксоны периферического мотонейрона идут уже непосредственно к мышце.
Паралич (парез) возникает при поражении как центрального, так и
периферического нейронов корково-мышечного пути.
Спастический (центральный) паралич
развивается при поражении верхнего (центрального) мотонейрона
корково-мышечного пути, свидетельствуя о том, что очаг поражения
находится либо в головном, либо в спинном мозге. Основными характерными
проявлениями центрального паралича (пареза) являются следующие [П.Дуус,
1995]:
- спастическое повышение мышечного тонуса (гипертония);
- снижение мышечной силы в сочетании с утратой способности к тонким движениям;
- повышение глубоких (проприоцептивных) рефлексов;
- снижение или выпадение экстерорецептивных рефлексов (брюшных, кремастерного, подошвенного);
- появление патологических рефлексов (Бабинского, Оппенгейма, Гордона и др.);
- отсутствие дегенеративной мышечной атрофии.
Механизмы развития мышечной спастичности
Основным
признаком центрального паралича, как и основным фактором,
препятствующим восстановлению двигательных функций и значительно
ограничивающим жизнедеятельность больного, является спастичность. По
определению J. Lance [1980], спастичность — это двигательное
нарушение, являющееся одним из компонентов синдрома верхнего мотонейрона
и характеризующееся повышением тонических рефлексов на растяжение (или
мышечного тонуса) в сочетании с повышением сухожильных рефлексов.
Мышечный тонус определяется двумя факторами:
- механико-эластическими характеристиками мышечной и соединительной ткани;
- рефлекторной сократимостью мышц (тоническим рефлексом на растяжение).
Первый фактор, или «внутренняя жесткость» мышечной ткани, имеет
несомненное значение в развитии или поддержании спастической гипертонии,
поскольку в какой-то степени мышца подобна обыкновенной пружине,
возвратная сила действия которой пропорциональная изменению ее длины и в
то же время зависит от модуля упругости материала, из которого сделана
пружина [Katz R., 1996]. Однако основная роль в поддержании и изменении
мышечного тонуса отводится функциональному состоянию сегментарной дуги
рефлекса растяжения (миотатического, или проприоцептивного рефлекса).
Кратко напомним схему этого рефлекса (рис.4.1. и 4.2).
Рис. 1. Схема рефлекса поддержания длины мышцы (по П.Дуусу, 1995)
Рис. 2. Схема рефлекса поддержания тонуса мышцы (по П.Дуусу, 1995)
Рецепторным элементом миотатического рефлекса является
инкапсулированное мышечное веретено (fusus, лат.). Каждая мышца содержит
большое количество этих рецепторов. Мышечное веретено состоит из
интрафузальных мышечных волокон (в сравнении с обычными экстрафузальными
мышечными волокнами они значительно тоньше) и ядерной сумки, оплетенной
спиралевидной сетью тонких нервных волокон, представляющих собой
первичные чувствительные окончания. На некоторых интрафузальных волокнах
имеются еще и вторичные, гроздевидные чувствительные окончания. При
растяжении интрафузальных волокон первичные чувствительные окончания
усиливают исходящую из них импульсацию, которая через быстро проводящие
афферентные волокна типа Iа проводятся к альфа-большим мотонейронам
спинного мозга. Оттуда через также быстропроводящие альфа-1 эфферентные
волокна импульс идет к экстрафузальным белым мышечным волокнам, которые
обеспечивают быстрое (фазическое) сокращение мышцы. От вторичных
чувствительных окончаний, реагирующих на тонус мышцы, афферентная
импульсация проводится по тонким волокнам II типа через систему
вставочных нейронов к альфа-малым мотонейронам, которые иннервируют
тонические экстрафузальные мышечные волокна (красные мышечные волокна),
обеспечивающие поддержание тонуса и позы.
Интрафузальные волокна
иннервируются гамма-нейронами передних рогов спинного мозга.
Возбуждение гамма-нейронов, передаваясь по гамма-волокнам к мышечному
веретену, сопровождается сокращением полярных отделов интрафузальных
волокон и растяжением их экваториальной части, при этом изменяется
исходная чувствительность рецепторов к растяжению (происходит снижение
порога возбудимости рецепторов растяжения и усиливается тоническое
напряжение мышцы).
Гамма-мотонейроны находятся под влиянием
центральных (супрасегментарных) воздействий, передающихся по волокнам,
которые идут от мотонейронов оральных отделов головного мозга в составе
пирамидного, ретикулоспинального, вестибулоспинального трактов. Таким
образом, мышечный тонус может регулироваться непосредственно головным
мозгом, что очень важно для выполнения произвольных движений. При этом,
если роль пирамидной системы заключается в преимущественной регуляции
фазических (т.е. быстрых, целенаправленных) компонентов произвольных
движений, то экстрапирамидная система обеспечивает плавность
произвольных движений, их «настройку» в соответствии с решаемой задачей,
т.е. преимущественно регулирует тоническую иннервацию мышечного
аппарата.
В регуляции мышечного тонуса принимают участие и
тормозные механизмы, которые реализуются с помощью рецепторов Гольджи,
расположенных в сухожилиях мыщц, и вставочных клеток Реншоу, находящихся
в передних рогах спинного мозга. Сухожильные рецепторы Гольджи при
растяжении или значительном напряжении мышцы посылают афферентные
импульсы, которые проводятся по быстропроводящим волокнам 1b типа в
спинной мозг и оказывают тормозящее воздействие на мотонейроны передних
рогов. Вставочные нейроны Реншоу активизируются через коллатерали при
возбуждении альфа-мотонейронов и действуют по принципу отрицательной
обратной связи, тормозя активность последних. Таким образом, нейрогенные
механизмы регуляции мышечного тонуса многообразны и сложны.
Повышение
мышечного тонуса при спастических параличах происходит в результате
усиления тонического рефлекса на растяжение. В настоящее время
спастичность связывают с нарушением не какого-либо одного, а целого ряда
нейрофизиологических механизмов, среди которых решающая роль отводится
нарушению дифференцированной регуляции альфа- и гамма-мотонейронов,
гипервозбудимости спинальных альфа-мотонейронов, уменьшению активности
некоторых ингибиторных механизмов [Гехт А.Б. и соавт., 1998]. Спастичные
параличи нередко называют «пирамидными», однако в настоящее время
полагают, что повышение мышечного тонуса обусловлено поражением не
собственно пирамидных волокон, а тесно переплетенных с ними волокон
экстрапирамидной системы, в частности, кортико-ретикулярного и
вестибулоспинального трактов. При этом среди волокон, контролирующих
активность системы «гамма-нейрон — мышечное веретено», в большей степени
обычно страдают ингибирующие волокна, тогда как активирующие сохраняют
свое влияние на мышечные веретена. Следствием этого является
спастичность мышц, гиперрефлексия, появление патологических рефлексов,
первоочередная утрата наиболее тонких произвольных движений. Отсутствие
или слабая выраженность мышечных атрофии при центральном параличе
объясняется тем, что верхний мотонейрон в гораздо меньшей степени влияет
на трофику мышц в сравнении с нижним двигательным нейроном.
Степень
спастичности чаще всего определяют по модифицированной 5-ти балльной
шкале Ашфорта. Объективизацию состояния мышечного тонуса и контроль за
динамикой спастической гипертонии возможно проводить с помощью методов
биомеханики и электромиографии. Так, проводились попытки оценивать
выраженность спастичности по таким электромиографическим показателям,
как отношение величины максимального Н-рефлекса к М-ответу (Нmax/Мmax),
кривая восстановления Н-рефлекса; однако корреляция этих показателей с
клинической выраженностью спастической гипертонии оказалась низкой [Katz
R., 1996]. Более информативны биомеханические методы, например,
«маятниковый» тест. Этот тест предполагает выведение сустава из
состояния равновесия путем дозированного внешнего воздействия с
последующей регистрацией возникших колебаний соответствующего сегмента
конечности; скорость затухания этих колебаний отражает тонус мышц
конечности [Katz R. и соавт., 1992].
Лечебные мероприятия
Повышение
мышечного тонуса существенно влияет на процесс восстановления
нарушенных функций. Высокая спастичность препятствует реализации
сохранных функций и улучшению нарушенных. С другой стороны, некоторое
повышение мышечного тонуса может иметь при параличе компенсаторное
значение. Поэтому прежде чем назначать лечение, необходимо решить,
насколько необходимо и целесообразно снижать мышечный тонус конечности.
Для этого врач должен ответить на следующие вопросы:
- усугубляет ли спастичность нарушение жизнедеятельности пациента?
- имеются ли нарушения походки в связи с мышечным гипертонусом?
- беспокоят ли больного мышечные спазмы либо боль, связанная со спастичностью мышц?
- в какой степени гипертонус разгибателей нижних конечностей способствует устойчивости вертикальной позы пациента?
Добиваться снижения мышечного тонуса необходимо в первую очередь в
тех случаях, когда спастичность существенно снижает уровень
жизнедеятельности больного либо сопровождается болевым синдромом. При
этом надо помнить о том, что в ряде случаев повышение тонуса
мышц-разгибателей ног служит фактором, облегчающим стояние и ходьбу.
Основным
требованием, предъявляемым к лечебным воздействиям, является их
безболезненность, поскольку боль усиливает спастичность мышц. Важно
также тщательно контролировать функцию тазовых органов (предупреждение
инфекции мочеполовых путей), своевременно выполнять мероприятия по
профилактике контрактур и пролежней.
Комплекс лечебных мероприятий по устранению спастичности включает:
- медикаментозные средства;
- ортезирование;
- физиотерапевтические процедуры (местное применение холода или тепла, электростимуляция периферических нервов и спинного мозга);
- массаж;
- лечебная гимнастика;
- медикаментозные блокады;
- хирургические вмешательства.
Выбор методов воздействия определяется строго индивидуально в
зависимости от локализации и степени спастического паралича, а также с
учетом финансовых и технических возможностей реабилитационного
учреждения.
Медикаментозное лечение
Основными
препаратами, используемыми для снижения мышечного тонуса, являются
миорелаксанты. По механизму действия различают миорелаксанты
центрального действия (влияют на синаптическую передачу возбуждения в
центральной нервной системе) и периферического действия (угнетают прямую
возбудимость поперечно-полосатых мышц). При применении миорелаксантов
могут возникать достаточно значимые побочные действия, которые при
выборе препарата надо тщательно оценить.
К мирелаксантам центрального действия, лицензированным в России, относятся баклофен, сирдалуд, диазепам.
Баклофен
(лиорезал) — это аналог гамма-аминомасляной кислоты (gamma-aminobutyric
acid, или сокращенно GАВА, англ.) — нейротрансмиттера, участвующего в
пресинаптическом торможении импульсов. Баклофен, являясь агонистом
пресинаптических GABAb-рецепторов, угнетает моно- и полисинаптические
рефлексы и уменьшает активность гамма-эфферентов за счет уменьшения
выделения из терминалей возбуждающих аминокислот (аспартата и
глутамата). Препарат выделяется почками, период полувыведения составляет
около 3,5 часов. Легко проникает через гематоэнцефалический барьер.
Наиболее эффективен при спинальных формах спастики: баклофен не только
уменьшает тонус и снимает болезненные мышечные спазмы, но и улучшает
функцию тазовых органов за счет расслабления наружного сфинктера уретры.
Обладает некоторым противотревожным действием. У больных с поражением
головного мозга может отрицательно влиять на процессы внимания и памяти.
У взрослых баклофен назначают, начиная с 10-15 мг в сутки (в
2-3 приема), постепенно повышая затем дозу каждые 3 дня на 5-15 мг до
достижения терапевтически эффективной дозы. Средняя доза обычно
составляет от 30 до 60 мг в сутки; превышать суточную дозу 80 мг обычно
не рекомендуют. К основным побочным действиям относятся общая слабость,
гипотония, атаксия, которые, как правило, проходят при уменьшении дозы
препарата. При внезапной отмене могут возникать судороги и галлюцинации.
Достоверных данных о безопасности применения баклофена у детей пока не
получено, поэтому в детской практике препарат необходимо использовать с
особой осторожностью.
Баклофен можно назначать не только
перорально, но и интратектально [Albright A. и соавт., 1993]. Для
подведения препарата непосредственно к спинному мозгу разработаны
специальные устройства, представляющие из себя помпу, которая вшивается
подкожно в область брюшной стенки, и катетер, который хирургическим
путем устанавливается в субарахноидальное пространство. Такой путь
введения позволяет уменьшить побочные эффекты, связанные с влиянием
лекарственного вещества на головной мозг. В зависимости от конструкции
помпы (механическая, компьютеризированная) подача препарата к спинному
мозгу может осуществляться в постоянном либо в запрограммированном
переменном режиме. Обычно первоначальная суточная доза составляет 25 мг,
затем ее постепенно повышают до той, которая способствует
удовлетворительному снижению мышечного тонуса (около 400-500 мг в
сутки). Повторные наполнения помпы лекарственным веществом проводят
путем транскутанных инъекций. К возможным осложнениям относятся
передозировка баклофена, инфекции, поломка помпы, закупорка либо
смещение катетера. Стоимость устройства очень велика (около 6.500
долларов США), еще около 3.000 долларов больной ежегодно тратит на
лекарственный препарат и хирургические вмешательства. Поэтому показания и
противопоказания к интратектальному введению препарата определяются
особенно тщательно. Этот путь введения баклофена показан больным со
спинальными формами спастических параличей ног (после спинальной травмы,
при рассеянном склерозе) при условии частичной сохранности движений в
нижних конечностях и способности больного к ходьбе. У пациента не должно
быть сопутствующих инфекционных заболеваний и пролежней, в особенности в
области спины; необходимо также убедиться в отсутствии ликворного блока
между уровнем предполагаемого введения катетера и уровнем очага
поражения в спинном мозге.
Сирдалуд (тизанидин)
— агонист центральных альфа2-адренорецепторов, избирательно действующий
на полисинаптические пути в спинном мозге. Механизм действия, вероятно,
связан со снижением выброса возбуждающих аминокислот из
пресинаптических терминалей спинальных интернейронов и с активизацией
глицина (ингибирующего нейротрансмиттера), в результате чего уменьшается
поток возбуждающих импульсов к альфа-мотонейронам спинного мозга. По
эффективности воздействия на повышенный мышечный тонус близок к
баклофену, но лучше переносится и эффективен при спастике как
спинального, так и церебрального генеза. Период полувыведения около 3- 5
часов. Взрослым назначают начиная с дозы 1-2 мг в сутки (в два-три
приема) с последующим постепенным повышением дозы до 12-14 мг (в
три-четыре приема, не более 36 мг в сутки). Основными побочными
действиями являются легкая артериальная гипотензия, слабость, сухость во
рту, диссомния. В связи с гипотензивным эффектом в случаях
одновременного приема антигипертонических средств дозу последних следует
пересмотреть.
Диазепам (валиум) облегчает
постсинаптическое действие гамма-аминомасляной кислоты, что в свою
очередь приводит к усилению пресинаптического торможения импульсов и
ингибированию спинальных рефлексов. Основным моментом, ограничивающим
широкое применение диазепама, является его выраженный седативный эффект и
отрицательное воздействие на когнитивные функции, особенно
нежелательное у больных с церебральными поражениями. Начинают с дозы 2
мг в день, очень постепенно повышая ее до 60 мг в сутки в несколько
приемов. У детей назначают в дозах от 0.12 до 0.8 мг/кг в сутки, дробно.
К миорелаксантам периферического механизма действия относится дантролен (дантриум).
Дантролен
ингибирует актинмиозиновый комплекс, который является субстратом
сократимости мышцы. Механизм действия связан с уменьшением высвобождения
кальция в саркоплазматический ретикулюм, что сопровождается снижением
контрактильности мышечных волокон. Препарат, таким образом, действует
непосредственно на уровне мышечной ткани, не влияя на спинальные
механизмы регуляции тонуса. В большей степени воздействует на белые
мышечные волокна, поэтому сильнее снижает активность фазических
рефлексов (в сравнении с тоническими). Метаболизируется в печени,
выводится почками и с желчью, период полувыведения составляет около 8-9
часов. Более эффективен при церебральном происхождении спастичности
(постинсультная гемиплегия, детский церебральный паралич), в отличие от
баклофена или диазепама слабо влияет на когнитивные функции. У взрослых
начальные дозы составляют 25-50 мг в сутки, суточную дозу постепенно
повышают до 100-125 мг. Существенного улучшения клинических результатов
при дальнейшем наращивании дозы обычно не наблюдается. У детей начинают с
дозы 0.5 мг/кг массы тела, максимальная доза — 3 мг/кг, не более 100 мг
в сутки. К побочным действиям относятся сонливость, тошнота,
головокружение, диарея. Примерно у 1% больных могут наблюдаться симптомы
поражения печени, в связи с этим препарат противопоказан при
сопутствующих заболеваниях печени. К противопоказаниям относятся также
явления сердечной недостаточности.
Таким образом, выбор
препарата определяется основным заболеванием, выраженностью мышечной
спастичности, а также побочными эффектами и особенностями действия
конкретного препарата. Например, сирдалуд и баклофен в большей степени
действуют на тонус мышц-разгибателей [Braddom R., 1996]. Поэтому в
случаях наличия значительного гипертонуса мышц-сгибателей руки и легкой
спастичностыо мышц ноги прием миорелаксантов не показан, поскольку
легкое повышение тонуса мышц-разгибателей ноги как бы компенсирует
мышечную слабость в ноге и стабилизирует походку больного. В таком
случае средством выбора являются методы физического воздействия на мышцы
верхней конечности [Кадыков А.С., 1997].
Ортезирование
Длительная
укладка конечности в таком положении, когда спастичные мышцы растянуты,
уменьшает тоническую (динамическую и статическую) рефлекторную
активность и способствует снижению мышечного гипертонуса [Booth В. и
соавт., 1983]. Наложение съемной гипсовой лонгеты или шины рекомендуется
при выраженном повышении мышечного тонуса, способном вызвать
формирование контрактуры. Шина должна фиксировать конечность или ее
сегмент в том положении, при котором спастичные мышцы находятся в
растянутом состоянии (например, разгибательная шина для пальцев кисти и
лучезапястного сустава при повышении тонуса в мышца-сгибателях кисти и
предплечья). Лечение положением осуществляется от одного до нескольких
часов в день, в зависимости от субъективных ощущений больного и
состояния мышечного тонуса. При появлении болей и усилении спастичности
процедуру прекращают.
Физиотерапевтические процедуры
Из
физиотерапевтических процедур назначают местное применение холода или,
наоборот, тепла, а также электростимуляцию периферических нервов.
Местное применение холода
(например, льда) способствует снижению повышенных сухожильных
рефлексов, увеличению объема движений в суставе, улучшению функции
мышц-антагонистов. После аппликации льда тонус снижается на очень
непродолжительное время, возможно, в результате снижения
чувствительности кожных рецепторов и замедления нервной проводимости.
Близкий эффект достигается при применении местных анестетиков. Для
достижения максимального эффекта пакеты со льдом рекомендуется
накладывать на 15-20 и более минут. Курс 15-20 процедур.
Местное применение тепла
также может способствовать временному снижению повышенного тонуса.
Лечение теплом осуществляется с помощью парафиновых или озокеритовых
аппликаций (салфетно-аппликационный и кюветно-аппликационный способы), в
виде широких полос, перчаток, носков в таком положении конечности,
когда спастичная мышца наиболее растянута. Температура аппликаций
составляет 48-50 градусов, длительность процедуры 15-20 минут, 15-20
процедур на курс. При выполнении тепловых процедур у больных с
сопутствующей артериальной гипертензией необходимо контролировать
артериальное давление.
Электрическая стимуляция была
впервые применена для лечения спастических параличей еще Дюшеном в 1871
г. С тех пор при терапии мышечного гипертонуса используется накожное,
подкожное, эпидуральное расположение электродов, а также их перонеальная
имплантация.
Электростимуляция периферических нервов
традиционно применяется у больных с нижней спастической параплегией при
стоянии, ходьбе, выполнении физических упражнений. Доказана
эффективность поверхностной электростимуляции у больных с постинсультной
спастической гемиплегией [Fakhri О. и соавт., 1994]. У больных с
поражением спинного мозга для снижения тонуса делаются попытки
использовать электростимуляцию спинного мозга (задних столбов) путем
эпидурального введения электродов [Gottlieb G., 1985]. Механизм влияния
электростимуляции на повышенный мышечный тонус связывают с
нейротрансмиттерной модуляцией на сегментарном уровне. Снижение
мышечного тонуса обычно временное, наблюдается в пределах нескольких
часов после проведения процедуры. Режимы воздействия, как и параметры
электростимулирующего тока зависят от этиологии и локализации паралича.
Электростимуляция
мышц при спастических параличах проводится главным образом с целью
создания целенаправленной интенсивной афферентации со стимулируемых
мышц, что способствует растормаживанию временно инактивированных нервных
элементов вблизи очага деструкции, а также помогает в тренировке новых
двигательных навыков, улучшает трофику мышечной ткани. При спастических
параличах рекомендуется стимуляция антагонистов спастичных мышц,
поскольку «электрогимнастика» гипертоничных мышц может вызвать
дополнительное повышение мышечного тонуса. Чаще всего стимуляцию
проводят токами повышенных частот, поскольку низкочастотные токи,
обладая значительным раздражающим действием на кожу, вызывают
болезненные ощущения, что может также способствовать усилению
гипертонуса. При использовании аппарата «Амплипульс» применяют II род
работы при режиме «посылка-пауза», частоте 50-100 гц и глубине модуляций
75-100%. Длительность серии колебаний устанавливается в 2 сек., а
длительность пауз в 5 сек. Продолжительность стимуляции каждой мышечной
группы постепенно увеличивается с 5 до 20 минут, курс лечения состоит из
18-30 процедур [Ткачева Г.Р. и соавт., 1975].
При лечении
спастических параличей в качестве стимулирующих сигналов могут быть
также использованы усиленные и видоизмененные биопотенциалы здоровых
мышечных групп, причем биостимуляция может быть многоканальной. Среди
аппаратов многоканальной электростимуляции с биоэлектрическим
управлением наиболее широкое применение нашло устройство «Миотон»,
разработанное в Киевском институте кибернетики. Принцип действия каждого
канала этого аппарата заключается в том, что усиленные и
интегрированные биопотенциалы донора, снятые с определенной мышечной
группы и выполняющие роль «алгоритма» движения, управляют сигналами от
генератора переменных высокочастотных токов, подаваемыми на определенную
мышечную группу реципиента. Запись сигналов от донора на магнитофон
позволяет многократно повторять заданную программу движения.
Массаж
Направлен
на расслабление спастичных мышц, поэтому среди приемов используют
поглаживание, крупное потряхивание, очень медленное и неглубокое
разминание, воздействие на сегментарные зоны. Грубые болезненные приемы
вызывают повышение тонуса. Используют также точечный массаж по тормозной
методике. Тормозной метод точечного массажа осуществляется путем
постепенного наращивания интенсивности давления кончиком пальца на
избранную точку, задержкой его на оптимальной глубине с последующим
постепенным снижением и прекращением давления. Воздействие на одну точку
продолжается от 30 секунд до полутора минут [Добровольский В.К. и
соавт., 1986]. Топография рекомендуемых точек воздействия для снижения
тонуса в мышцах конечностей представлены в таблице 1 и на рис. 3.
Таблица 1. Точки для снижения тонуса мышц конечностей, мышц плечевого и тазового пояса
(по В.К. Добровольскому и соавт., 1986)
| № точки | Название точки | Местонахождение точки | Мышцы, на которые оказывается расслабляющее воздействие |
| Плечевой пояс и верхняя конечность | |||
| 1 | Чжоу-жун | Во 2 межреберье по срединно-ключичной линии, на большой грудной мышце |
Большая грудная мышца (сгибает, приводит и пронирует руку в плечевом суставе) |
| 2 | Цзи-цюань | На уровне подмышечной складки во впадине у внутреннего края двуглавой мышцы плеча | Сгибатели и пронаторы плеча |
| 3 | Цзянь-чжень | Сзади и книзу от плечевого сустава по задней подмышечной линии, между плечевой костью и лопаткой | Широчайшая мышца спины (разгибает, приводит и пронирует руку в плечевом суставе) |
| 4 | Био-нао | На наружной поверхности плеча выше локтевого сгиба на 7 цуней, у заднего края дельтовидной мышцы и наружного края трехглавой мышцы плеча |
Общее расслабление мышц верхней конечности |
| 5 | Чи-цзе | На складке локтевого сгиба, у наружного края сухожилия двуглавой мышцы плеча | Двуглавая мышца плеча (сгибает плечо и предплечье, супинирует предплечье) |
| 6 | Шао-хай | На складке локтевого сгиба, спереди от внутреннего мыщелка локтевой кости | Мышцы-сгибатели предплечья |
| 7 | Нэй-гуань |
На ладонно-срединной линии предплечья, на 2 цуня выше лучезапястного сустава |
Мышцы-сгибатели кисти, квадратный пронатор |
| 8 | Да-лин | На ладонной поверхности в середине лучезапястного сустава | Мышцы-сгибатели кисти и пальцев |
| 9 | Лао-гун | В середине ладони, между 3 и 4 пястными костями | Мышцы-сгибатели пальцев кисти |
| 10 | Щи-сюань | На кончиках дистальных фаланг пальцев кисти | Мышцы-сгибатели пальцев кисти |
| 11 | Шоу-сань-ли |
На тыльно-лучевой линии предплечья на 2 цуня ниже локтевого сгиба |
Круглый пронатор |
| 12 | Хэ-гу | На тыльной поверхности кисти между 1 и 2 пястными костями | Мышцы-сгибатели кисти и пальцев, приводящая мышца большого пальца |
| Тазовый пояс и нижняя конечность | |||
| 13 | Хуань-тяо | Сзади от тазобедренного сустава на большой ягодичной мышце | Ягодичные мышцы (разгибают, супинируют и пронируют бедро) |
| 14 | Би-гуань |
На передней поверхности бедра на 13 цуней выше коленного сустава |
Четырехглавая мышца бедра (разгибает голень и сгибает бодро) |
| 15 | Фу-ту | На передней поверхности бедра выше верхнего края надколенника на 7 цуней | Тоже |
| 16 | Ду-би | Снаружи от нижнего полюса надколенника | Тоже |
| 17 | Чэн-шань | На задней поверхности голени у места перехода икроножной мышцы в ахиллово сухожилие | Икроножная и камбаловидная мышцы (сгибают голень и стопу, пронируют и супинируют голень при согнутом коленное суставе) |
| 18 | Чэн-цзинь | На 2 цуня выше точки чэн-шань | Тоже |
| 19 | Кунь-лунь | Сзади и снизу между наружной лодыжкой и ахилловым сухожилием | Мыщцы-сгибатели стопы и пальцев |
Примечание: цунь- это индивидуальная для каждого
человека единица измерения, равная расстоянию между двумя складками,
образующимися при сгибании 2 и 3-й фаланг среднего пальца на левой кисти
у мужчин и на правой кисти у женщин.
Рис. 3. Топография точек, рекомендуемых для расслабления мышц конечностей (по В.К.Добровольскому и соавт., 1986)
Лечебная гимнастика
Для
снижения спастичности назначают упражнения, направленные на
расслабление мышц, упражнения на подавление патологических синкинезий, а
также ежедневные упражнения на растяжение спастических мышц.
Дозированное растягивание мышцы позволяет на несколько часов снизить
мышечный тонус и увеличить объем движений в соответствующем суставе.
Механизм такого воздействия растягивающих упражнений не вполне ясен.
Возможно, он связан с изменением механических свойств
мышечно-сухожильного аппарата, а также с модуляцией синаптической
трансмиссии; так, в экспериментах было показано, что повторяющаяся
активизация рефлекторных механизмов приводит к уменьшению синаптической
трансмиссии в результате инактивации кальциевых каналов в
пресинаптических терминалях и уменьшению высвобождения
нейротрансмиттеров [Каtz R., 1996]. Снижение тонуса после таких
упражнений носит временный характер, и стратегия кинезотерапевта должна
быть направлена на максимально эффективное использование этого
промежутка времени для тренировки тех активных движений, которые на фоне
спастичности были затруднены.
Необходимо помнить о следующих особенностях лечебной гимнастики при спастических параличах [Коган О.Г., Найдин В.Л., 1988]:
- прекращение занятий при начинающемся повышении мышечного тонуса выше исходного;
- во избежании синкинезий сочетанные движения в двух и более
суставах применяются только после достижения четких движений в отдельно
взятых суставах (вначале в одном направлении и одной плоскости, затем — в
различных плоскостях и направлениях); - соблюдение правила «частичных» объемов — усиление мышцы вначале
проводится в диапазоне малых амплитуд, и лишь по мере укрепления мышцы
этот объем увеличивается вплоть до полного, физиологического; - необходимость достаточно раннего перехода от «абстрактных» гимнастических упражнений к тренировке простейших бытовых навыков;
- строгое соблюдение равномерного дыхания, недопустимость задержек дыхания на вдохе, натуживаний, одышки.
Увеличить эффект кинезотерапии позволяет также обучение больного
приемам аутогенной тренировки и включение ее элементов в урок лечебной
гимнастики [Демиденко Т.Д., 1989].
Медикаментозные блокады
Направлены на
временное или постоянное прерывание потока нервных импульсов к мышце
путем воздействия на нерв химическим веществом, механизм действия
основан на фармакологическом прерывании.
Так, при сгибательной
контрактуре в локтевом суставе (например, при постинсультной гемиплегии)
блокада лучевого нерва позволяет расслабить участвующую в сгибании
предплечья плечелучевую мышцу. Блокада срединного нерва помогает
уменьшить флексию в кистевом суставе и пальцах кисти. Блокада
запирательного нерва способствует снижению спастики в приводящих мышцах
бедра, улучшению вследствие этого походки и облегчению выполнения
процедур личной гигиены. Блокада большеберцового нерва может помочь
скорригировать эквино-варусное положение стопы, устранить болезненную
сгибательную контрактуру пальцев стопы.
В качестве препаратов
для химической перерезки нерва используют местные анестетики (например,
лидокаин), спирт, фенол, ботулотоксин.
Местные анестетики
вызывают временный (продолжительностью в несколько часов) блок
проведения путем воздействия на процессы деполяризации мембран нервных
клеток. Поскольку эффект таких блокад очень кратковременен, их применяют
в основном в качестве теста для определения потенциальной эффективности
блокад с использованием более длительнодействующих агентов, либо для
уточнения показаний к хирургическому вмешательству на нервных стволах.
В отечественной практике для химического невролиза наиболее часто используют спирт, в зарубежной — фенол и ботулотоксин.
Действие этилового спирта
связывают с избирательным блокированием волокон гиперакгивных
гамма-мотонейронов. Согласно рекомендациям Т.Д.Демиденко [1989], спирт
вводят в двигательные точки мышц (рис.4.4 и 4.5) в форме
спирт-новокаиновой смеси (0.25% раствор новокаина и 45% раствор
этилового спирта в равных частях), по 1-2 мл смеси на точку, 1-2 раза в
неделю, на курс от 3 до 15 процедур. Блокады обязательно сочетаются с
корригирующей гимнастикой. По М.О.Фридману [1954], успешно применявшему
метод закрытой перимускулярной алкоголизации для ослабления
спастического напряжения мышц, спирт-новокаиновая смесь готовится по
следующему рецепту:
Novocaini 1.0 (2.0)
Aq. destillatae 20.0
Spiritum vini rectificati 95% 80.0
Рис. 4. Двигательные точки нервов и мышц верхней конечности (по В.М.Боголюбову, 1985)
1
— трехглавая мышца плеча (длинная головка); 2 — трехглавая мышца плеча
(наружная головка); 3 — лучевой нерв; 4,14 -локтевой нерв; 5,15 —
срединный нерв; 6 — двуглавая мышца плеча; 7 — дельтовидная мышца; 8 —
плечелучевая мышца; 9 — лучевой сгибатель запястья; 10-поверхностный
сгибатель пальцев; 11 — длинный сгибатель большого пальца; 12 — глубокий
сгибатель пальцев; 13 — локтевой сгибатель запястья; 16 — короткая
ладонная мышца; 17 — мышца, отводящая мизинец; 18 — короткий сгибатель
мизинца; 19,24 — межкостные мышцы; 20 — мышца, приводящая большой палец;
21 — короткий сгибатель большого пальца; 22 — мышца, противоставляющая
большой палец; 23 — короткая мышца, отводящая большой палец; 25 —
длинный и короткий разгибатель большого пальца; 26-длинная мышца,
отводящая большой палей; 27 — разгибатель II пальца; 28 — разгибатель
пальцев; 29 — короткий лучевой разгибатель запястья; 30 — длинный
лучевой разгибатель запястья; 31 — локтевой разгибатель запястья; 32 —
супинатор предплечья
Рис. 5. Двигательные точки нервов и мышц нижней конечности (по В.М.Боголюбову, 1985)
1
— бедренный нерв; 2 — запирательный нерв; 3 — длинная приводящая мышца;
4 — тонкая мышца; 5 — большая приводящая мышца; 6 — портняжная мышца; 7
— четырехглавая мышца бедра; 8 — напрягатель широкой фасции; 9-прямая
мышца бедра; 10-медиальная широкая мышца бедра; 11 -латеральная широкая
мышца бедра; 13 — передняя большеберцовая мышца; 14 — длинный
разгибатель пальцев; 15,25,26 — икроножная мышца; 16 — длинный
разгибатель большого пальца; 17 — межкостные мышцы; 18 — большая
ягодичная мышца; 19 -седалищный нерв; 20 — двуглавая мышца бедра; 21 —
полусухожильная мышца; 22 — полуперепончатая мышца; 23 — малоберцовый
нерв; 24 — большеберцовый нерв; 27 — длинный сгибатель пальцев; 28 —
задняя большеберцовая мышца; 29 — длинный сгибатель большого пальца; 30 —
короткий разгибатель пальцев; 31 — короткая малоберцовая мышца; 32 —
короткий разгибатель большого пальца
Согласно
рекомендациям вышеуказанного автора, раствор вводят под фасцию мышцы в
дозах не свыше 30 мл раствора на сеанс для нижней конечности и 20 мл для
верхней конечности у взрослых и соответственно 15 и 10 мл у детей.
Расслабление мышц наступает через несколько минут и продолжается от
нескольких часов до нескольких дней. При недостаточном эффекте блокаду
повторяют через 5-10 дней.
Основным недостатком
спирт-новокаиновых блокад, помимо болезненности процедуры, является
кратковременность эффекта расслабления мышцы.
Действие фенола
основано на коагуляции белков и развитии вследствие этого некроза
аксонов. Фенол применяют в виде 2-6% раствора, вводя его в ствол нерва
либо в места разветвления его терминальных волокон (т.е. в двигательные
точки мышцы); последний способ менее эффективен и поэтому менее
предпочтителен. Средняя вводимая доза составляет около 20 мл 5%
раствора. При правильном выполнении блокады, предполагающем
использование иглы с тефлоновым покрытием и осуществление
электрофизиологического контроля в процессе процедуры, эффект от нее
сохраняется от 3 до 6 месяцев. Со временем разрушенные фенолом аксоны
регенерируют. Поскольку фенол повреждает не только двигательные, но и
чувствительные волокна, у 10% больных после блокады возникают дизестезии
(чувство жжения и дискомфорта) и каузалгии, о чем пациента надо
предупреждать заранее. Снизить вероятность этих осложнений можно при
открытом (т.е. в процессе хирургического вмешательства) выполнении
блокады, позволяющем избирательно блокировать двигательные волокна
непосредственно у места их вхождения в мышцу. К другим осложнениям
феноловых блокад относятся преходящая слабость в соответствующей мышце,
тромбозы вен, при передозировке препарата — судороги, угнетение функции
сердечно сосудистой и центральной нервной систем.
Эффект от
введения препарата проявляется обычно через 1-2 недели, сохраняется до 6
месяцев. Для профилактики вторичной резистентности к препарату между
сериями инъекций рекомендуют делать 12-недельные интервалы [O’Brien С.,
1995].
Начиная с 1980-х годов для снижения повышенного мышечного
тонуса стали применять местные инъекции ботулотоксина типа А.
Ботулотоксин типа А представлят собой один из восьми серотипов токсинов
(протеинов), продуцируемых Clostridium botulinum и ингибирующих
высвобождение ацетилхолина в нервномышечных синапсах [O’Brien С., 1995].
В настоящее время выпускается в виде препарата Botox (NОА) и Dysport
(Великобритания). Содержание токсинов в этих двух препаратах различно:
Ботокс содержит в 1 единице 0.4 нг токсина, Диспорт — 0.025 нг (одна
единица соответствует LD50 для самок- мышей Swiss-Webster весом 18-20
г). Токсичность (LD50) Для обезьян составляет при внутримышечном
введении 39 ед/кг, при внутривенном введении — 40 ед/кг.
Ботулотоксин,
в отличие от фенола, действует более диффузно, поэтому при его введении
не требуется точного попадания непосредственно в нервный ствол;
препарат вводят в проекции двигательных точек напряженной мышцы, по
30-50 единиц на точку. Желательно проведение процедуры под контролем
игольчатой ЭМГ для более точной локализации инъекции. Рекомендуемые для
инъекции мышцы и соответствующие им релаксирующие дозы препарата Диспорт
указаны в таблице 4.2. Эффект появляется через 4-14 дней и продолжается
2-6 месяцев.
Таблица 2. Рекомендуемые для инъекций ботулотоксина мышцы и релаксирующине дозы препарата Диспорт (по А. Langueny, 1995)
| Схема повышения мышечного тонуса | Мышцы | Дозы препарата Диспорт (в ед) в расчете на одну мышцу |
| ВЕРХНЯЯ КОНЕЧНОСТЬ | ||
| Приведение и внутренняя ротация плеча | Pectoralis major | 350 |
| Сгибание в локтевом суставе | Biceps brachii Brachioradialis Brachialis |
500 |
| Пронация предплечья | Pronators | 200 |
| Сгибание кисти | Flexor carpi radialis Flexor carpi ulnaris |
300 |
| Сгибание пальцев | Flexor digitorum superf. Flexor digitorum prof. |
250 |
| Приведение первого пальца | Opponens pollicis | 125 |
| НИЖНЯЯ КОНЕЧНОСТЬ | ||
| Приведение бедра | Adductors | 500 |
| Сгибание в коленном суставе | Hamstrings | 400 |
| Разгибание в коленном суставе | Quadriceps femoris | 1000 |
| Подошвенное сгибание стопы | Gastrocnemius | 1000 |
| Сгибание пальцев стопы | Flexor digitorum longus | 200 |
Следует избегать назначения более
чем 250-300 единиц в течение одной сессии инъекции. К настоящему времени
не выявлено серьезных побочных действий препаратов ботулотоксина при
применении его в рекомендуемых дозах. Возможно возникновение чрезмерной
мышечной слабости, однако со временем происходит восстановление мышечной
силы. Может наблюдаться также вторичная резистентность к препарату, для
профилактики которой рекомендуют делать интервал между сессиями
инъекциями не менее 12 недель. Не выявлено также эффекта взаимодействия
ботулотоксина и пероральных миорелаксантов типа баклофена.
Ограничивает
широкое применение ботулотоксина высокая стоимость препаратов,
выпускаемых на его основе. Для более обоснованного назначения препарата
O’Brien С. [1995] рекомендует придерживаться алгоритма, представленного
на схеме 4.1.
Схема 1. Алгоритм назначения препаратов ботулотоксина для снижения мышечного тонуса
(По С. O’Brien.1995)
Хирургические вмешательства
Применяют при
неэффективности консервативных мероприятий. При решении вопроса о
показаниях к ортопедической операции оценивают целый ряд факторов [Katz
R., 1996]:
- Давность поражения центральной нервной системы. Ортопедическое
вмешательство показано лишь тогда, когда исчерпаны возможности
восстановления нарушенных функций (не ранее чем через 6 месяцев после
инсульта и 12-24 месяцев после черепно-мозговой травмы). - Характер спастичности — динамический или статический. Под
динамическим характером спастики понимают усиление гипертонуса при
движениях (например, скрещивание ног, возникающее при ходьбе у детей,
страдающих детским церебральным параличом). Статический характер
спастики обычно является результатом довольно длительного повышения
мышечного тонуса, приведшего к формированию фиксированных контрактур,
выраженность которых одинакова как в покое, так и при движениях. В
некоторых случаях для определения характера гипертонуса приходится
прибегать к блокадам нервных стволов местными анестетиками типа
лидокаина. - Степень сохранности чувствительности конечности, резидуальных
двигательных функций, высших корковых функций. Так, восстановительная
операция на конечности может оказаться бессмысленной в отношении
улучшения способности больного к самообслуживанию при наличии грубых
нарушений праксиса и гнозиса либо при нарушении опорно-стабилизирующей
функции туловища и плечевого либо тазового пояса. - Сопутствующие повреждения опорно-двигательного аппарата
(переломы, вывихи, артриты, оссификации), поскольку несвоевременное
выявление этих поражений может полностью нивелировать успех грамотно
проведенной ортопедической операции.
Таким образом, отбор больных должен быть очень тщательным. При
положительном решении о показаниях к ортопедическому вмешательству четко
определяется его цель (улучшение походки, улучшение охвата кисти,
увеличение объема движения в суставе с целью облегчения самообслуживания
и т.д), а также тип в оперативного вмешательства (таблица 4.3 и 4.4).
Таблица 3. Типы ортопедических операций при спастических параличах верхней конечности
(по R. Braddom,1996)
| Характер нарушения | Тип вмешательства |
| Приведение и внутренняя ротация плеча |
Мобилизация сухожилий большой грудной и подлопаточной мышц с |
| Нижний подвывих плеча |
«Подтяжка» сухожилия двуглавой мышцы плеча путем перекидывания через клювовидный отросток лопатки |
| Сгибательная контрактура в локтевом суставе |
Поэтапное удлинение плечелучевой, двуглавой и плечевой мышц |
| Разгибательная контрактура в плечевом суставе |
V- или У-образное удлинение трехглавой мышцы плеча |
| Сгибательная контрактура в кистевом суставе и пальцах кисти |
При негрубой контрактуре — зигзагообразное удлинение сухожилий |
| Приведение большого пальца |
Мобилизация мышц тенара |
Таблица 4. Типы ортопедических операций при спастических параличах нижней конечности
(по R. Braddom,1996)
| Характер нарушения | Тип вмешательства |
| Функциональные нарушения | |
| Скрещивание ног при ходьбе (гипертонус мышц-аддукторов бедер) | При динамической спастике — неврэктомия запирательного нерва; при статической — мобилизация аддукторов бедра с последующей тренировкой ходьбы. |
| Походка «прячущегося» (гипертонус флексоров бедра, компенсаторное сгибание в коленном суставе и поясничный гиперлордоз) | Надрез повздошно-поясничной мышцы, постепенное удлинение сухожилий, ограничивающих дистально подколенную ямку. |
| Походка «на негнущихся ногах» (гипертонус четырехглавой мышцы бедра) | Мобилизация одной или двух головок четырехглавой мышцы с последующей 5-дневной иммобилизацией коленного сустава лонгетой, затем — тренировка ходьбы. |
| Эквиноварусная стопа (сгибание, приведение и супинация в голеностопном суставе, сгибание пальцев в результате гипертонуса передней большеберцовой мышцы) |
Удлинение ахиллова сухожилия. Расщепление сухожилия передней большеберцовой мышцы с перемещением дистального конца латерального фрагмента сухожилия на кубовидную и третью клиновидную кости. Мобилизация сгибателей пальцев. |
| Спастическая вальгусная стопа (гипертонус длинной малоберцовой мышцы) | Мобилизация и перемещение сухожилия длинной малоберцовой мышцы через тыл стопы на ладьевидную кость. |
| Статические нарушения | |
| Контрактура аддукторов бедра | Мобилизация длинного аддуктора и нежной мышцы с последующим 4-недельным наложением отводящей гипсовой лонгеты. |
| Контрактура сгибателей бедра | Мобилизация портняжной мышцы, прямой мышцы бедра, пояснично-повздошной мышцы, гребешковой мышцы и мышцы, натягивающей широкую фасцию бедра. |
| Контрактура разгибателей бедра | Мобилизация дистального отдела ахиллова сухожилия с последующим регулярным выполнением упражнений лечебной гимнастики. |
| Разгибательная контрактура в коленном суставе | Удлинение сухожилия четырехглавой мышцы бедра с последующим 3-недельным гипсованием коленного сустава в положении сгибания. |
| Сгибательная контрактура в коленном суставе | Мобилизация сухожилий, ограничивающих дистально подколенную ямку. |
| Контрактуры в голеностопном суставе | Те же вмешательства, что и при функциональных нарушениях, мобилизация подошвенной фасции, артродез голеностопного сустава. |
Нейрохирургические операции
В
тяжелых случаях можно решать вопрос о проведении ризотомии (перерезке
спинномозговых корешков). Ризотомия может быть открытой (требует
выполнения ламинэктомии) или закрытой (чрезкожной, осуществляемой под
флюороскопическим контролем с помощью специального инструментария),
полной или селективной, передней или задней. Поскольку передняя
ризотомия приводит к тяжелой дегенеративной атрофии всех мышц, имеющих
соответствующую иннервацию, предпочтение отдается задней селективной
ризотомии. Задняя (дорсальная) селективная ризотомия, или пересечение
определенной порции дорсальных корешков, выполняется наиболее часто на
пояснично-крестцовом уровне при спастическом параличе нижних конечностей
при частичной сохранности произвольных движений и существенной
ограничивающей роли спастики в реализации этих движений. Выбор тех
порций корешков, которые подлежат перерезке, определяется путем
предварительного проведения электрофизиологического исследования реакции
мышц при стимуляции соответствующих корешков и выяснения роли тех или
иных корешков в поддержании мышечного гипертонуса. Чаще всего патология
обнаруживается в L5 и S1 корешках. К основным побочным результатам
ризотомии относятся слабость и гипотония в нижних конечностях. Описаны
также случаи возникновения тазовых нарушений, чувствительных
расстройств, вывихов в тазобедренном суставе. Наибольший опыт применения
ризотомии накоплен при лечении детского церебрального паралича, однако
мнения специалистов об эффективности этой операции достаточно
противоречивы [Landaw W., 1990].
При обсуждении проблемы лечения
наиболее тяжелых форм спастики упоминается также такой метод, как
задняя продольная миелотомия [Kasdon D., 1986], однако ввиду тяжести
возможных осложнений этой операции она не нашла широкого распространения
в клинической практике.
Автор:
Белова А.Н.
Дата публикации:
31.01.2006
Источник:
sci-rus.com

Особенность двигательных нервных клеток в том, что их цитоплазма не окружает ядро равномерно, а образует два отростка. Один из них более короткий (дендрит) принимает нервный импульс, второй (аксон) передает его дальше.
Таким образом, двигательный периферический нейрон проводит нервный импульс от центральной нервной системы к мышце. В мышечной ткани его длинный отросток разветвляется и соединяется с десятками мышечных волокон.
Виды двигательных нейронов
По локализации моторные нейроны подразделяются на центральные и периферические. Центральные расположены в ткани головного мозга. Они отвечают за сознательные контролируемые мышечные сокращения.
Двигательные нейроны, идущие непосредственно к мышечным волокнам, называют соматическими.

Тела двигательных нейронов соматической нервной системы расположены в области передних рогов спинного мозга и располагаются группами, каждая из которых отвечает за сокращение строго определенной мускулатуры. К примеру, мотонейроны шейного отдела управляют мускулатурой рук, поясничного отдела отвечают за иннервацию ног.
Периферические нервные клетки, отвечающие за движения, классифицируются следующим образом:
- большие альфа-мотонейроны;
- малые альфа-мотонейроны;
- гамма-мотонейроны;
- клетки Реншо.
Большие альфа-клетки формируют крупные проводящие стволы. Малые альфа и гамма-нейроны имеют более тонкие аксоны. Клетки Реншо входят в состав крупных стволов и служат для коммутации сигналов.
Гамма-мотонейронная петля
Функции мотонейрона
Центральные и периферические двигательные нервные клетки работают согласовано. Совместно они обеспечивают сокращение определенных групп мышц и позволяют человеку выполнять какие-либо действия.
Для координированных движений конечностей необходимо одновременное сокращение сгибателей и разгибателей. При работе сгибателей первоначальный сигнал возбуждения возникает в области прецентральной извилины соответствующего полушария.
За это действие отвечают клетки, называемые пирамидными. Собранные вместе их отростки образуют так называемый пирамидный двигательный путь. Далее сигнал идет к передним рогам спинного мозга, откуда передается уже непосредственно в миофибриллы.
Активирующее влияние на мотонейроны мышц разгибателей оказывают специальные центры задних отделов больших полушарий. Они формируют дорсальный и вентральный пути. Таким образом, в формировании координированного движения участвуют две области головного мозга.

По характеру функции нервные клетки, задействованные в процессе мышечного сокращения, подразделяются на двигательные и вставочные нейроны. Первые ответственны за исполнительную функцию, в то время как для координации нервных импульсов служат вставочные. Эта особая разновидность имеет меньшие размеры и более многочисленна.
Для сравнения — в области передних рогов их в 30 раз больше чем двигательных. Когда возбуждение проводится по аксону двигательного нерва, оно переходит первоначально на вставочный нейрон. В зависимости от характера сигнала он может быть усилен либо ослаблен, после чего передается дальше.
Клетки вставочного типа имеют больше отростков и более чувствительны. Они обладают большим числом отростков и их еще называют мультиполярными.

Для оптимизации сигналов исходящих по аксонам и идущим к мышечным волокнам, служат специальные клетки Реншоу, которые передают возбуждение с одного отростка на другой. Такой механизм служит выравниванию интенсивности нервного сигнала.
По отростку мотонейрона импульс достигает мышечного волокна, которое сокращается. Каждая группа мотонейронов и иннервируемые ими мышечные волокна отвечают за определенные движения.
Нервные клетки, обеспечивающие двигательную функцию:
| Виды нейронов | Локализация | Функция |
|---|---|---|
| центральные иннервирующие сгибатели |
область прецентральной извилины | сокращение скелетных мышц сгибателей путем передачи импульса в область передних рогов |
| центральные иннервирующие разгибатели |
область заднего мозга | сокращение скелетных мышц разгибателей путем передачи импульса в область передних рогов |
| периферические альфа | передние рога спинного мозга | непосредственное сокращение скелетных мышц |
| периферические гамма | передние рога спинного мозга | регуляция тонуса |
| вставочные | все отделы ЦНС | коммуникация сигналов внутри ЦНС |
Большие альфа-нейроны, проводящие сильный импульс, вызывают сокращение миофибрилл. Малые проводят слабые сигналы и служат для поддержания тонуса мускулатуры.
Помимо волокон, отвечающих за сокращение, в мышечной ткани есть и специальные спиральные фибриллы, регулирующие силу напряжения мускулатуры.
Эти экстрафузальные мышечные волокна иннервируются гамма-нейронами.
Возбуждение гамма-мотонейрона приводит к увеличению растяжения миофибрилл и облегчает прохождение импульса сухожильных рефлексов. Примером может быть прохождение нервного сигнала по дуге коленного рефлекса.
Слаженной работой периферических мотонейронов достигается тонкая настройка мышечного тонуса, что позволяет выполнять точные координированные движения. При поражении периферических двигательных нейронов мышечный тонус исчезает и движения невозможны.

Как работает двигательный нейрон?
Для того чтобы возник биоэлектрический импульс, необходима разница потенциалов на оболочке нервной клетки. Это происходит в результате изменения концентрации ионов калия и натрия с наружной и внутренней поверхности мембраны.
В дальнейшем импульс проходит до конца длинного отростка ‒ аксона и достигает места соединения с другой клеткой. Место такого контакта называют синапс.

С другой стороны синапса к месту контакта прилежит короткий ветвящийся отросток ‒ дендрит. Передача сигнала через синапс обусловлена активными химическими веществами, так называемыми медиаторами.
Возникнув на дендрите, сигнал распространяется по его оболочке и переходит далее на аксон. Для сокращения скелетной мышцы сигнал зарождается в мотонейроне коры, проходит по пирамидному пути, переходит на вставочный нейрон и далее в область передних рогов спинного мозга. Заканчивается эта цепь в мышечной ткани.
Результатом возбуждения двигательного центра коры будет сокращение группы мышечных волокон.
Симптомы поражения центрального двигательного нейрона
Поражения центральных моторных нервных клеток возникают чаще всего при инсульте. При ишемии или кровоизлиянии в вещество больших полушарий участок ткани отмирает. Такие поражения почти всегда односторонние.
Вследствие этого при поражении центральных двигательных нейронов наблюдаются нарушения функции мускулатуры с одной стороны. Самый заметный признак ‒ это односторонний паралич, приводящий к невозможности активных движений в руке и ноге.
С этой же стороны снижается мышечный тонус в туловище и мимической мускулатуре лица. Поражение центральных моторных областей сопровождается рядом изменений рефлекторной деятельности.
Клинически это выражается в появлении разнообразных патологических рефлексов. Их совокупность, снижение тонуса мышц и нарушения чувствительности позволяют врачу установить диагноз.
Неврологический центр им. Б.М. Гехта ОАО «РЖД»;
НИИ общей патологии и патофизиологии РАМН
Меркулова Д.М.
Неврологический центр им. Б.М. Гехта ОАО «РЖД»;
НИИ общей патологии и патофизиологии РАМН
Иосифова О.А.
Научный центр неврологии РАМН, Москва
Завалишин И.А.
Научный центр неврологии РАМН, Москва
Аксонопатия в патогенезе рассеянного склероза, периферических диффузных и локальных моторных невропатий и болезни мотонейрона
Авторы:
Меркулов Ю.А., Меркулова Д.М., Иосифова О.А., Завалишин И.А.
Как цитировать:
Меркулов Ю.А., Меркулова Д.М., Иосифова О.А., Завалишин И.А. Аксонопатия в патогенезе рассеянного склероза, периферических диффузных и локальных моторных невропатий и болезни мотонейрона. Журнал неврологии и психиатрии им. С.С. Корсакова.
2010;110(8):4‑7.
Merkulov IuA, Merkulova DM, Iosifova OA, Zavalishin IA. Axonopathy in the pathogenesis of multiple sclerosis, peripheral diffuse and local motor neuropathies and motor neuron disease. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2010;110(8):4‑7. (In Russ.)

Актуальность изучения роли аксонопатии в патогенезе воспалительных и дегенеративных заболеваний центральной и периферической нервной системы (ЦНС и ПНС) связана с широкой распространенностью данной патологии среди лиц молодого трудоспособного возраста. Ремиттирующее или неуклонно прогредиентное течение этих болезней приводит к ранней инвалидизации и снижению продолжительности жизни данной категории пациентов.
Объективизация признаков аксональной дегенерации у больных с рассеянным склерозом (РС) при магнитно-резонансной томографии (МРТ) головного мозга в виде выявления гипоинтенсивных T1-очагов («черных дыр») получила развитие лишь со второй половины 90-х годов XX века [26, 28]. К настоящему времени доказана зависимость между объемом «черных дыр» на МРТ и степенью инвалидизации пациентов, оцениваемой при помощи шкалы EDSS [8, 13, 25]. В связи с этим большинством авторов [2, 6, 16] поднимается вопрос о том, не является ли РС дегенеративным, а не только демиелинизирующим заболеванием ЦНС. В свою очередь указания на наличие периферической демиелинизации и аксонопатии при РС [7, 11, 14] позволяют подойти к изучению единых процессов формирования иммунопатологии в ЦНС и ПНС.
Обращает на себя внимание противоречивость данных литературы о роли и времени присоединения аксональных расстройств в ПНС при формировании острой и хронической воспалительной демиелинизирующей полиневропатии (ОВДП и ХВДП) и влиянии аксонопатии на развитие клинической и нейрофизиологической картины данных заболеваний. Большинство авторов [15] придерживаются точки зрения о четкой зависимости вторичной аксонопатии и мышечной слабости от выраженности демиелинизирующего процесса в периферических нервах. Еще в 1994 г. было отмечено, что в ряде случаев значительная демиелинизация, например у больных с врожденными невропатиями, сопровождается относительно умеренным неврологическим дефицитом [29]. Наряду с этим в последние годы активно обсуждается проблема о первично аксональной форме синдрома Гийена-Барре с положительным эффектом от иммуномодулирующей терапии [1, 18].
В 1982 г. было установлено, что демиелинизация периферических нервов может носить как диффузный, так и локальный характер, проявляющийся развитием компрессионных «туннельных» синдромов, а также блоков проведения возбуждения (БПВ) по моторным волокнам периферических нервов [22, 24]. При этом патогенетические механизмы локальной демиелинизации носят персистирующий характер и вовлекают в патологический процесс осевой цилиндр нерва на самых ранних этапах формирования патологического процесса. На основании этого ряд авторов [5, 9, 17] выделяют особую форму демиелинизирующей полиневропатии — моторную мультифокальную невропатию (ММН) с БПВ, клинически имитирующую симптоматику поражения нижнего мотонейрона при боковом амиотрофическом склерозе (БАС).
В свою очередь при БАС выявляется феномен миелинопатии, в том числе и фокальной [21]. В связи с этим постановка правильного диагноза нередко вызывает большие сложности. Научно-практический поиск отправных моментов дифференциальной диагностики этих состояний очень актуален, поскольку ММН в отличие от БАС является курабельным заболеванием [27]. Ключом для разработки этих вопросов являются универсальные механизмы дизрегуляционной патологии, возникающей вследствие образования патологической интеграции поврежденных структур миелиновой оболочки и аксона и приводящей к формированию аксонально-демиелинизирующего невропатологического синдрома [4].
Целью работы явилось изучение единых механизмов развития аутоиммунных и дегенеративных заболеваний нервной системы.
Материал и методы
Обследовали 276 больных: 43 — с РС, 24 — с ОВДП, 144 — с ХВДП, 27 — с ММН, 38 — с БАС.
Диагноз в каждом отдельном случае устанавливали на основании типичной клинической картины в соответствии с общепринятыми критериями диагностики [1, 3, 15, 23, 30]. При клиническом неврологическом обследовании использовали шкалы оценки функционального состояния и различных проявлений неврологического дефицита: «Расширенная шкала инвалидизации» (Expanded Disability Status Scale), «Мера функциональной независимости» (Functional Independence Measure) [10], «Шкала выраженности утомляемости» (Fatigue Severity Scale, FSS) [20]. Отдельно оценивали симптоматику, характеризующую состояние моторной, сенсорной и рефлекторной сферы по 4-балльной шкале: 0 баллов — норма, 3 балла — наибольшая выраженность признака.
Для объективизации клинически выявленных синдромов поражения нейромоторного аппарата всем больным было проведено электромиографическое (ЭМГ) обследование, включавшее исследование характеристик потенциалов двигательных единиц (ПДЕ) при игольчатой ЭМГ с анализом уровня спонтанной активности (СА) ДЕ (потенциалов фасцикуляций, ПФЦ) и мышечных волокон (МВ) (потенциалов фибрилляций, ПФ, и положительных острых волн, ПОВ). Для изучения проводящей функции аксонов периферических нервов применяли стандартную методику стимуляционной ЭМГ с анализом амплитуды М-ответов, скорости распространения возбуждения (СРВ) на различных отрезках нервов, значений резидуальной латентности и характеристик F-волн, а также качественной и количественной оценкой БПВ по методике «inching» [19]. Для изучения проводящей функции наиболее проксимальных отрезков периферических нервов, моторных спинномозговых корешков и кортикоспинальных проводящих путей использовали методику транскраниальной магнитной стимуляции (ТМС). При этом анализировали показатели латентного времени вызванного суммарного потенциала действия дистальных мышц (ВСПДМ) верхних и нижних конечностей при стимуляции С7-С8 или L5-S1 спинномозговых корешков, а также в проекции соответствующих областей моторной зоны коры головного мозга (Cz и Fz). Вычисляли расчетные показатели времени центрального проведения (ВЦП), а также «корешковой задержки» — времени прохождения импульса по недоступному для непрямой стимуляции корешковому сегменту нервов. С целью объективизации клинических проявлений синдрома усталости у пациентов с РС проводили исследование феномена фасилитации амплитуды и латентного времени ВСПДМ. Одновременно для исключения патологии передачи импульса на синаптическом уровне у данной группы больных применяли стандартный декремент-тест с анализом отношения амплитуды 5-го М-ответа к 1-му в мышце кисти при стимуляции соответствующего нерва частотой 3 Гц. Исследовали силу мышцы до и после максимального произвольного тонического усилия, а также постактивационные феномены облегчения и истощения (ПАО и ПАИ).
Были обследованы повторно 148 пациентов после назначения соответствующей терапии, 64 — 3 раза и более на фоне лечения. Всего провели 424 комплексных клинико-электромиографических исследования, обследовали 264 скелетных мышцы, 698 периферических нервов, 245 спинномозговых корешков и кортикоспинальных трактов.
Всем пациентам с РС провели МРТ-исследование головного мозга в соответствии с общепринятыми протоколами, применяемыми при подозрении на органическую патологию ЦНС с оценкой количества, локализации гиперинтенсивных Т2-очагов демиелинизации и линейного размера максимальных очагов. Для объективизации аксонального поражения ЦНС анализировали состояние гипоинтенсивных Т1-очагов («черных дыр») и степень атрофических процессов (состояние субарахноидального пространства и желудочков головного мозга).
Были проведены диагностические люмбальные пункции 23 больным РС и 38 больным МНМ с последующим анализом уровня клеточно-белкового состава спинномозговой жидкости.
Статистическую обработку результатов проводили при помощи компьютерной программы STATISTICA.6.1 (США). Использовали параметрические и непараметрические методики: дисперсионный анализ и t-тест Стьюдента, критерии Вилкоксона, Манна-Уитни и Краскела-Уоллиса. Различия считали достоверными при достигнутом уровне значимости р<0,05.
Результаты и обсуждение
Во всех группах больных были выявлены признаки аксональной дегенерации, проявляющейся денервационными феноменами как клинически, так и по данным объективных методов обследования (ЭМГ, ТМС).
К настоящему времени анализ качественных и количественных характеристик аксонального повреждения ЦНС у пациентов с РС в основном сводится к оценке нейровизуализационных изменений. Среди обследованных больных РС наличие T1 «черных дыр» при МРТ было установлено в 28% случаев, регионарной атрофии коры головного мозга — в 46%. При этом получили статистически значимую корреляционную зависимость этих показателей от степени инвалидизации обследованных больных по шкале EDSS (т=0,38 и 0,43; p=0,038 и 0,021 соответственно).
Анализ феномена утомляемости позволил установить, что у 76% пациентов с РС значение суммарного балла по шкале FSS превышало 4, соответствуя наличию «синдрома усталости» [20]. Эти пациенты отличались статистически значимым снижением силы мышцы кисти по результатам тестирования максимального произвольного усилия (p=0,017), а также большей фасилитацией латентного времени и амплитуды ВСПДМ по результатам ТМС (p=0,024). Достоверное увеличение ВЦП на фоне истощения (p=0,032) наряду с отсутствием нарушения надежности нервно-мышечной передачи и отсутствием феноменов ПАО и ПАИ по результатам декремент-теста у данной категории больных позволило предположить преобладание центральных механизмов в формировании феномена усталости скелетных мышц при РС.
Вместе с тем в группе больных с РС в 34,7% случаев были выявлены признаки периферической демиелинизации, влияющие на паттерн типичной клинической и ЭМГ-картины заболевания. Из их числа в 29,2% случаев отмечались ЭМГ-признаки аксонального вовлечения в виде снижения амплитуды М-ответов при стимуляционной и увеличения амплитуды ПДЕ при игольчатой ЭМГ.
При снижении амплитуды М-ответов более 76% от нижней границы нормы у этих больных отмечалось появление клинических признаков невропатии (амиотрофия, снижение рефлексов и слабость), которые коррелировали с выявлением спонтанной активности МВ по данным игольчатой ЭМГ (т=0,31; p=0,027). Наряду с этим в клинико-электрофизиологической картине ММН в 12,3% случаев отмечено наличие признаков центральной демиелинизации, что свидетельствует об общности их патогенеза и подходов к лечению.
Наиболее частым механизмом формирования периферической аксонопатии было вторичное поражение осевого цилиндра нерва на фоне прогрессирования демиелинизирующего процесса, особенно характерное для больных ММН. Клинически это проявлялось развитием мышечной слабости и гипотрофий, достигая 80% при ОВДП и 67% при ХВДП. По данным ЭМГ-исследования, наряду со снижением СРВ отмечалось снижение амплитуды М-ответа в 35% случаев при ОВДП и 61% — при ХВДП, а также выявление спонтанной активности МВ по данным игольчатой ЭМГ в 41 и в 46% при ОВДП и ХВДП соответственно.
Взаимосвязь указанных клинических и нейрофизиологических феноменов у больных ДПНП подтверждалась наличием статистически значимой линейной корреляции степени мышечной гипотрофии и ПФ (r=0,26; p=0,024), гипотрофии и амплитуды М-ответов (r=–0,37; p=0,019). Наряду с этим было выявлено отсутствие корреляционной зависимости степени гипотрофии и СРВ (r=0,08; p=0,375).
По данным катамнеза, измененная СРВ сохранялась до 3 лет после клинического выздоровления. Следует подчеркнуть, что у 2,7% больных ОВДП снижение СРВ было выявлено даже на 3-й день болезни. Однако при тестировании больных ОВДП к 3-й неделе заболевания СРВ было снижено лишь в 22,8% случаев. У больных ХВДП снижение СРВ было отмечено в 100% случаев и имело диффузный и неравномерный по отношению к различным нервам тип распределения. Тщательное ЭМГ-обследование, проведенное в первые дни болезни, выявившее наличие спонтанной активности МВ и перестройки ПДЕ, наряду со снижением параметров СРВ и амплитуды М-ответов у 17,4% пациентов позволило диагностировать вариант ХВДП с острым началом и обосновать раннее присоединение глюкокортикоидной терапии.
Другим патофизиологическим механизмом развития аксонопатии явилось формирование БПВ, в первую очередь у больных ММН (100% — согласно критериям диагностики). БПВ выявлялись также и у пациентов с ОВДП (68%), ХВДП (72%) и даже БАС (71%). Однако в данных группах отмечена достоверно меньшая частота БПВ II степени (падение амплитуды проксимального М-ответа по отношению к дистальному на 50% и более) по сравнению с пациентами с ММН (χ2=137,5; p<0,001).
Выявление БПВ на раннем этапе развития ОВДП служило ЭМГ-подтверждением демиелинизирующей природы заболевания (с последующим присоединением снижения СРВ, белково-клеточной диссоциации в ликворе), что позволило своевременно начать патогенетическую терапию. При этом клиническая значимость БПВ была подтверждена наличием статистически значимой корреляции выраженности амиотрофического синдрома и БПВ II степени как у больных ММН, так и с другими формами демиелинизирующей полинейропатии (т=1,0 и 0,73; p=0,001 и 0,012 соответственно).
Особое внимание было уделено выявлению БПВ в проксимальных сегментах периферических нервов, корешках и участках нервных сплетений путем сопоставления результатов, полученных при анализе поздних ответов (F-волны) и магнитной стимуляции, поскольку традиционное исследование стимуляционной ЭМГ даже методом «inching» было неинформативным. У пациентов с ММН изолированные проксимальные БПВ были выявлены в 23% случаев, при ОВДП — в 28%, при ХВДП — в 20% и при БАС — в 22%. Срединная (по отношению к протяженности периферического нерва) локализация БПВ чаще располагалась вблизи зоны физиологических компрессий, что косвенно указывает на генерализованную «слабость» миелина при демиелинизирующем процессе. Дистальная локализация БПВ была менее характерна для всех групп больных.
Генез развития БПВ у больных с БАС до конца не ясен. Основными теориями являются вторичная деструкция миелина на фоне злокачественного нейронального процесса и присоединение вторичного аутоиммунного компонента [12, 24]. Вместе с тем только анализ БПВ у данной категории больных позволяет косвенно оценить качественный вклад аксонального повреждения в развитие заболевания, поскольку информативность остальных как клинических, так и электрофизиологических критериев снижена за счет процессов прогрессирующей нейрональной дегенерации. У обследованных больных с БАС аналогично отмеченным зависимостям при ММН и демиелинизирующей полинейропатии выявляли тенденцию к корреляции БПВ и клинических проявлений моторного дефицита: мышечных гипотрофий и слабости (т=0,36 и 0,49; р=0,089 и 0,082 соответственно). Особое внимание было уделено клинико-электрофизиологическим характеристикам БАС с преобладанием поражения нижнего мотонейрона (35,6%), который нуждается в тщательном проведении дифференциальной диагностики с ММН, имеющей в отличие от генерализованной болезни мотонейрона благоприятный прогноз.
Заключение
Выявленные аксональные нарушения у больных с РС, ММН и БАС позволили проследить общие закономерности развития патологического процесса при всех исследованных нозологиях. У всех больных преобладание аксональных нарушений способствовало выявлению особого паттерна клинических и электрофизиологических показателей, отличного от типичного распределения мышечной слабости, гипотрофий, клинически выявляемых фасцикуляций, характеристик амплитуды М-ответов, ПДЕ, спонтанной активности ДЕ и МВ. Демиелинизирующий процесс как в ЦНС, так и периферических нервах и моторных корешках на стадии развивающейся демиелинизации клинически проявляется минимально. Дебют клинической симптоматики обусловлен присоединением вторичной аксонопатии.
«Синдром усталости» у больных с РС наиболее вероятно является отражением нарушения центральных механизмов регуляции мышечных сокращений, что позволяет рассматривать его в качестве проявления вторичного аксонального поражения ЦНС.
Формирование БПВ является универсальным патофизиологическим механизмом развития аксонопатии при ОВДП, ХВДП, ММН и БАС. Высокая частота фокальной демиелинизации периферических нервов оказывает статистически значимое влияние на типичную клиническую и ЭМГ-картину при этих нозологиях. При этом подтверждено наличие особой формы демиелинизирующей полинейропатии — ММН с БПВ в 100% случаев, клинически имитирующей симптоматику поражения нижнего мотонейрона при БАС.
Признаки аксонопатии и периферической демиелинизации у больных с РС и БАС свидетельствуют о возможности распространения иммунопатологического процесса из ЦНС в ПНС. При этом у больных с РС имеются клинико-электрофизиологические признаки периферической демиелинизации диффузного характера, а у больных БАС — преимущественно локального (БПВ).