В теле человека бессчетное количество клеток, каждая из которых имеет собственную функцию. Среди них самые загадочные – нейроны, отвечающие за любое совершаемое нами действие. Попробуем разобраться как работают нейроны и в чем их предназначение.
Что такое нейрон (нейронные связи)
В переводе с греческого нейрон, или как его еще называют неврон, означает «волокно», «нерв». Нейрон – это специфическая структура в нашем организме, которая отвечает за передачу внутри него любой информации, в быту называемая нервной клеткой.
Нейроны работают при помощи электрических сигналов и способствуют обработке мозгом поступающей информации для дальнейшей координации производимых телом действий.
Эти клетки являются составляющей частью нервной системы человека, предназначение которой состоит в том, чтобы собрать все сигналы, поступающие из вне или от собственного организма и принять решение о необходимости того или иного действия. Именно нейроны помогают справиться с такой задачей.
Каждый из нейронов имеет связь с огромным количеством таких же клеток, создаётся своеобразная «паутина», которая называется нейронной сетью. Посредством данной связи в организме передаются электрические и химические импульсы, приводящие всю нервную систему в состояние покоя либо, наоборот, возбуждения.
К примеру, человек столкнулся с неким значимым событием. Возникает электрохимический толчок (импульс) нейронов, приводящий к возбуждению неровной системы. У человека начинает чаще биться сердце, потеют руки или возникают другие физиологические реакции.
Мы рождаемся с заданным количеством нейронов, но связи между ними еще не сформированы. Нейронная сеть строится постепенно в результате поступающих из вне импульсов. Новые толчки формируют новые нейронные пути, именно по ним в течение жизни побежит аналогичная информация. Мозг воспринимает индивидуальный опыт каждого человека и реагирует на него. К примеру, ребенок, схватился за горячий утюг и отдернул руку. Так у него появилась новая нейронная связь.
Стабильная нейронная сеть выстраивается у ребенка уже к двум годам. Удивительно, но уже с этого возраста те клетки, которые не используются, начинают ослабевать. Но это никак не мешает развитию интеллекта. Наоборот, ребенок познает мир через уже устоявшиеся нейронные связи, а не анализирует бесцельно все вокруг.
Даже у такого малыша есть практический опыт, позволяющий отсекать ненужные действия и стремиться к полезным. Поэтому, например, так сложно отучить ребенка от груди — у него сформировалась крепкая нейронная связь между приложением к материнскому молоку и удовольствию, безопасности, спокойствию.
Познание нового опыта на протяжении всей жизни приводит к отмиранию ненужных нейронных связей и формированию новых и полезных. Этот процесс оптимизирует головной мозг наиболее эффективным для нас образом. Например, люди, проживающие в жарких странах, учатся жить в определенном климате, а северянам нужен совсем другой опыт для выживания.
Сколько нейронов в мозге
Нервные клетки в составе головного мозга занимают порядка 10 процентов, остальные 90 процентов это астроциты и глиальные клетки, но их задача заключается лишь в обслуживании нейронов.
Подсчитать «вручную» численность клеток в головном мозге также сложно, как узнать количество звезд на небе.
Тем не менее ученые придумали сразу несколько способов для определения количества нейронов у человека:
- Рассчитывается число нервных клеток на небольшой части мозга, а затем, количество умножается пропорционально полному объему. Исследователи исходят из постулата о том, что нейроны равномерно распределены в нашем мозге.
- Происходит растворение всех мозговых клеток. В результате получается жидкость, в составе которой можно увидеть клеточные ядра. Их можно посчитать. При этом служебные клетки, о которых мы сказали выше, не учитываются.
В результате описанных экспериментов установлено, что число нейронов в головном мозге человека — 85 миллиардов единиц. Ранее, на протяжении многих веков считалось, что нервных клеток больше, порядка 100 миллиардов.
Строение нейрона
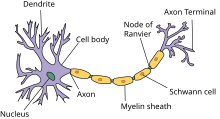
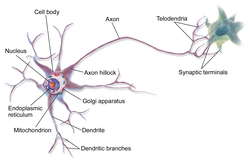
На рисунке приведено строение нейрона. Он состоит из основного тела и ядра. От клеточного тела идет ответвление многочисленных волокон, которые именуются дендритами.
Мощные и длинные дендриты называются аксонами, которые в действительности намного длиннее, чем на картинке. Их протяженность варьируется от нескольких миллиметров до более метра.
Аксоны играют ведущую роль в передаче информации между нейронами и обеспечивают работу всей нервной системы.
Место соединения дендрита (аксона) с другим нейроном называется синапсом. Дендриты при наличии раздражителей могут разрастись настолько сильно, что станут улавливать импульсы от других клеток, что приводит к образованию новых синаптических связей.
Синаптические связи играют существенную роль в формировании личности человека. Так, личность с устоявшимся позитивным опытом будет смотреть на жизнь с любовью и надеждой, человек, у которого нейронные связи с негативным зарядом, станет со временем пессимистом.
Виды нейронов и нейронных связей
Нейроны можно обнаружить в различных органах человека, а не исключительно в головном мозге. Большое их количество расположено в рецепторах (глаза, уши, язык, пальцы рук – органы чувств). Совокупность нервных клеток, которые пронизывают наш организм составляет основу периферической нервной системы. Выделим основные виды нейронов.
| Вид нейронной клетки | За что отвечает |
|---|---|
| Аффекторные | Являются переносчиками информации от органов чувств в головной мозг. У этого вида нейронов самые длинные аксоны. Импульс из вне поступает по аксонам строго в определенный участок головного мозга, звук — в слуховой «отсек», запах – в «обонятельный» и т.д. |
| Промежуточные | Промежуточные нервные клетки обрабатывают сведения, поступившие от аффекторных нейронов и передают ее периферическим органам и мышцам. |
| Эффекторные | На заключительном этапе в дело вступают эфференты, которые доводят команду промежуточных нейронов до мышц и других органов тела. |
Слаженная работа нейронов трех типов выглядит так: человек «слышит» запах шашлыка, нейрон передает информацию в соответствующий раздел мозга, мозг передает сигнал желудку, который выделяет желудочный сок, человек принимает решение «хочу есть» и бежит покупать шашлык. Упрощенно так это действует.
Самыми загадочными являются промежуточные нейроны. С одной стороны, их работа обуславливает наличие рефлекса: дотронулся до электричества – отдернул руку, полетела пыль –зажмурился. Однако, пока не объяснимо как обмен между волокнами рождает идеи, образы, мысли?
Единственное, что установили ученые, это тот факт, что любой вид мыслительной деятельности (чтение книг, рисование, решение математических задач) сопровождается особой активностью (вспышкой) нервных клеток определенного участка головного мозга.
Есть особая разновидность нейронов, которые именуются зеркальными. Их особенность заключается в том, что они не только приходят в возбуждение от внешних сигналов, но и начинают «шевелиться», наблюдая за действиями своих собратьев – других нейронов.
Функции нейронов
Без нейронов невозможна работа организма человека. Мы увидели, что эти наноклетки отвечают буквально за каждое наше движение, любой поступок. Выполняемые ими функции до настоящего времени в полной мере не изучены и не определены.
Существует несколько классификаций функций нейронов. Мы остановимся на общепринятой в научном мире.
Функция распространения информации
Данная функция:
- является основной;
- изучена лучше остальных.
Суть ее в том, что нейронами обрабатываются и переносятся в головной мозг все импульсы, которые поступают из окружающего мира или собственного тела. Далее происходит их обработка, подобно тому, как работает поисковик в браузере.
По результатам сканирования сведений из вне, головной мозг в форме обратной связи передает обработанную информацию к органам чувств или мышцам.
Мы не подозреваем, что в нашем теле происходит ежесекундная доставка и переработка информации, не только в голове и на уровне периферической нервной системы.
До настоящего времени создать искусственный интеллект, который бы приблизился к работе нейронных сетей человека, не удалось. У каждого из 85 миллиардов нейронов имеется, как минимум, 10 тысяч обусловленных опытом связей, и все они работают на передачу и обработку информации.
Функция аккумуляции знаний (сохранения опыта)
Человек обладает памятью, возможностью понимать суть вещей, явлений и действий, которые он единожды или многократно повторял. За формирование памяти отвечают именно нейронные клетки, точнее нейротрансмиттеры, связующие звенья между соседними нейронами.
Таким образом, за память отвечает не какая-то отдельная часть мозга, а маленькие белковые мостики между клетками. Человек может потерять память, когда произошло крушение этих нервных связей.
Функция интеграции
Данная функция позволяет взаимодействовать между собой отдельным долям головного мозга. Как мы уже сказали, сигналы от разных органов чувств поступают в разные отделы мозга.
Нейроны посредством «вспышек» активности передают и принимают импульсы в разных частях мозга. Так происходит процесс появления мыслей, эмоций и чувств. Чем больше таких разноплановых связей, тем эффективнее человек мыслит. Если человек способен к размышлениям и аналитике в определенном направлении, то он будет хорошо соображать и в другом вопросе.
Функция производства белков
Нейроны – настолько полезные клетки, что не ограничиваются только передаточными функциями. Нервные клетки вырабатывают необходимые для жизни человека белки. Опять же ключевую роль в производстве белков имеют нейротрансмиттеры, которые отвечают за память.
Всего в невронах индуцируется порядка 80 белков, вот основные из них, влияющие на самочувствие человека:
- Серотонин – вещество, вызывающее радость и удовольствие.
- Допамин – ведущий источник бодрости и счастья для человека. Активизирует физическую активность, помогает проснуться, переизбыток может привести к состоянию эйфории.
- Норадреналин – это «плохой» гормон, вызывающий приступы ярости и гнева. Наряду с кортизолом его называют гормоном стресса.
- Глутамат – вещество, отвечающие за хранение памяти.
Прекращение выработки белков или их выпуск в недостаточном количестве способны привести к тяжелым заболеваниям.
Восстанавливаются ли нервные клетки
При нормальном состоянии организма нейроны могут жить и функционировать очень долго. К сожалению, случается так, что они начинают массово погибать. Причин разрушения нервных волокон может быть много, но до конца механизм их деструкции не изучен.
Установлено, что нервные клетки погибают из-за гипоксии (кислородное голодание). Нейронные сети рушатся при отдельных травмах головного мозга, человек теряет память или утрачивает способность к хранению информации. В этом случае сами нейроны сохранены, но теряется их передаточная функция.
Отсутствие допамина ведет к развитию болезни Паркинсона, а его переизбыток является причиной шизофрении. Почему прекращается выработка белка не известно, спусковой механизм не выявлен.
Гибель нервных клеток происходит при алкоголизации личности. Алкоголик со временем может совершенно деградировать и утратить вкус к жизни.
Формирование нервных клеток происходит при рождении. Долгое время ученые полагали, что со временем нейроны отмирают. Поэтому с возрастом человек утрачивает способность накапливать информацию, хуже соображает. Нарушение функции по выработке допамина и серотонина связывается с наличием практически у всех пожилых людей депрессивных состояний.
Гибель нейронов, действительно неизбежна, в год исчезает примерно 1 процент от их количества. Но есть и хорошие новости. Последние исследования показали, что в коре головного мозга есть особенный участок, именуемый гипокаммом. Именно в нем генерируются новые чистые нейроны. Подсчитано примерное количество генерируемых ежедневно нервных клеток – 1400.
В науке обозначилось новое понятие «нейропластичность», обозначающее возможность мозга регенерироваться и перестраиваться. Но есть одна тонкость: новые нейроны еще не имеют никакого опыта и наработанных связей. Поэтому с возрастом или после заболевания мозг нужно тренировать, как и все иные мышцы тела: получать новые знания, анализировать происходящие события и явления.
Подобно тому, как мы усиливаем бицепс при помощи гантели, активизировать процесс включения новых нервных клеток можно следующими способами:
- изучение новых сфер знаний, которые ранее были не нужны или не интересны. К примеру, математику можно начать изучать живопись, а юристу – основы физики.
- через постановку сложных задач и поиск их решения;
- составлением планов деятельности, которые включают в себя множество исходных данных.
Механизм возрождения прост. У нас имеются совершенно не задействованные новые клетки, которые нужно заставить работать, а сделать это можно лишь путем постановки новых задач и изучения неизвестных предметных сфер.
Вся информация взята из открытых источников.
Если вы считаете, что ваши авторские права нарушены, пожалуйста,
напишите в чате на этом сайте, приложив скан документа подтверждающего ваше право.
Мы убедимся в этом и сразу снимем публикацию.
| Axon | |
|---|---|
An axon of a multipolar neuron |
|
| Identifiers | |
| MeSH | D001369 |
| FMA | 67308 |
| Anatomical terminology
[edit on Wikidata] |
An axon (from Greek ἄξων áxōn, axis), or nerve fiber (or nerve fibre: see spelling differences), is a long, slender projection of a nerve cell, or neuron, in vertebrates, that typically conducts electrical impulses known as action potentials away from the nerve cell body. The function of the axon is to transmit information to different neurons, muscles, and glands. In certain sensory neurons (pseudounipolar neurons), such as those for touch and warmth, the axons are called afferent nerve fibers and the electrical impulse travels along these from the periphery to the cell body and from the cell body to the spinal cord along another branch of the same axon. Axon dysfunction can be the cause of many inherited and acquired neurological disorders that affect both the peripheral and central neurons. Nerve fibers are classed into three types – group A nerve fibers, group B nerve fibers, and group C nerve fibers. Groups A and B are myelinated, and group C are unmyelinated. These groups include both sensory fibers and motor fibers. Another classification groups only the sensory fibers as Type I, Type II, Type III, and Type IV.
An axon is one of two types of cytoplasmic protrusions from the cell body of a neuron; the other type is a dendrite. Axons are distinguished from dendrites by several features, including shape (dendrites often taper while axons usually maintain a constant radius), length (dendrites are restricted to a small region around the cell body while axons can be much longer), and function (dendrites receive signals whereas axons transmit them). Some types of neurons have no axon and transmit signals from their dendrites. In some species, axons can emanate from dendrites known as axon-carrying dendrites.[1] No neuron ever has more than one axon; however in invertebrates such as insects or leeches the axon sometimes consists of several regions that function more or less independently of each other.[2]
Axons are covered by a membrane known as an axolemma; the cytoplasm of an axon is called axoplasm. Most axons branch, in some cases very profusely. The end branches of an axon are called telodendria. The swollen end of a telodendron is known as the axon terminal which joins the dendron or cell body of another neuron forming a synaptic connection. Axons make contact with other cells – usually other neurons but sometimes muscle or gland cells – at junctions called synapses. In some circumstances, the axon of one neuron may form a synapse with the dendrites of the same neuron, resulting in an autapse. At a synapse, the membrane of the axon closely adjoins the membrane of the target cell, and special molecular structures serve to transmit electrical or electrochemical signals across the gap. Some synaptic junctions appear along the length of an axon as it extends; these are called en passant («in passing») synapses and can be in the hundreds or even the thousands along one axon.[3] Other synapses appear as terminals at the ends of axonal branches.
A single axon, with all its branches taken together, can innervate multiple parts of the brain and generate thousands of synaptic terminals. A bundle of axons make a nerve tract in the central nervous system,[4] and a fascicle in the peripheral nervous system. In placental mammals the largest white matter tract in the brain is the corpus callosum, formed of some 200 million axons in the human brain.[4]
Anatomy[edit]
A typical myelinated axon
Axons are the primary transmission lines of the nervous system, and as bundles they form nerves. Some axons can extend up to one meter or more while others extend as little as one millimeter. The longest axons in the human body are those of the sciatic nerve, which run from the base of the spinal cord to the big toe of each foot. The diameter of axons is also variable. Most individual axons are microscopic in diameter (typically about one micrometer (µm) across). The largest mammalian axons can reach a diameter of up to 20 µm. The squid giant axon, which is specialized to conduct signals very rapidly, is close to 1 millimeter in diameter, the size of a small pencil lead. The numbers of axonal telodendria (the branching structures at the end of the axon) can also differ from one nerve fiber to the next. Axons in the central nervous system (CNS) typically show multiple telodendria, with many synaptic end points. In comparison, the cerebellar granule cell axon is characterized by a single T-shaped branch node from which two parallel fibers extend. Elaborate branching allows for the simultaneous transmission of messages to a large number of target neurons within a single region of the brain.
There are two types of axons in the nervous system: myelinated and unmyelinated axons.[5] Myelin is a layer of a fatty insulating substance, which is formed by two types of glial cells: Schwann cells and oligodendrocytes. In the peripheral nervous system Schwann cells form the myelin sheath of a myelinated axon. Oligodendrocytes form the insulating myelin in the CNS. Along myelinated nerve fibers, gaps in the myelin sheath known as nodes of Ranvier occur at evenly spaced intervals. The myelination enables an especially rapid mode of electrical impulse propagation called saltatory conduction.
The myelinated axons from the cortical neurons form the bulk of the neural tissue called white matter in the brain. The myelin gives the white appearance to the tissue in contrast to the grey matter of the cerebral cortex which contains the neuronal cell bodies. A similar arrangement is seen in the cerebellum. Bundles of myelinated axons make up the nerve tracts in the CNS. Where these tracts cross the midline of the brain to connect opposite regions they are called commissures. The largest of these is the corpus callosum that connects the two cerebral hemispheres, and this has around 20 million axons.[4]
The structure of a neuron is seen to consist of two separate functional regions, or compartments – the cell body together with the dendrites as one region, and the axonal region as the other.
Axonal region[edit]
The axonal region or compartment, includes the axon hillock, the initial segment, the rest of the axon, and the axon telodendria, and axon terminals. It also includes the myelin sheath. The Nissl bodies that produce the neuronal proteins are absent in the axonal region.[3] Proteins needed for the growth of the axon, and the removal of waste materials, need a framework for transport. This axonal transport is provided for in the axoplasm by arrangements of microtubules and intermediate filaments known as neurofilaments.
Axon hillock[edit]
Detail showing microtubules at axon hillock and initial segment.
The axon hillock is the area formed from the cell body of the neuron as it extends to become the axon. It precedes the initial segment. The received action potentials that are summed in the neuron are transmitted to the axon hillock for the generation of an action potential from the initial segment.
Axonal initial segment[edit]
The axonal initial segment (AIS) is a structurally and functionally separate microdomain of the axon.[6][7] One function of the initial segment is to separate the main part of an axon from the rest of the neuron; another function is to help initiate action potentials.[8] Both of these functions support neuron cell polarity, in which dendrites (and, in some cases the soma) of a neuron receive input signals at the basal region, and at the apical region the neuron’s axon provides output signals.[9]
The axon initial segment is unmyelinated and contains a specialized complex of proteins. It is between approximately 20 and 60 µm in length and functions as the site of action potential initiation.[10][11] Both the position on the axon and the length of the AIS can change showing a degree of plasticity that can fine-tune the neuronal output.[10][12] A longer AIS is associated with a greater excitability.[12] Plasticity is also seen in the ability of the AIS to change its distribution and to maintain the activity of neural circuitry at a constant level.[13]
The AIS is highly specialized for the fast conduction of nerve impulses. This is achieved by a high concentration of voltage-gated sodium channels in the initial segment where the action potential is initiated.[13] The ion channels are accompanied by a high number of cell adhesion molecules and scaffolding proteins that anchor them to the cytoskeleton.[10] Interactions with ankyrin G are important as it is the major organizer in the AIS.[10]
Axonal transport[edit]
The axoplasm is the equivalent of cytoplasm in the cell. Microtubules form in the axoplasm at the axon hillock. They are arranged along the length of the axon, in overlapping sections, and all point in the same direction – towards the axon terminals.[14] This is noted by the positive endings of the microtubules. This overlapping arrangement provides the routes for the transport of different materials from the cell body.[14] Studies on the axoplasm has shown the movement of numerous vesicles of all sizes to be seen along cytoskeletal filaments – the microtubules, and neurofilaments, in both directions between the axon and its terminals and the cell body.
Outgoing anterograde transport from the cell body along the axon, carries mitochondria and membrane proteins needed for growth to the axon terminal. Ingoing retrograde transport carries cell waste materials from the axon terminal to the cell body.[15] Outgoing and ingoing tracks use different sets of motor proteins.[14] Outgoing transport is provided by kinesin, and ingoing return traffic is provided by dynein. Dynein is minus-end directed.[15] There are many forms of kinesin and dynein motor proteins, and each is thought to carry a different cargo.[14] The studies on transport in the axon led to the naming of kinesin.[14]
Myelination[edit]
TEM of a myelinated axon in cross-section.
In the nervous system, axons may be myelinated, or unmyelinated. This is the provision of an insulating layer, called a myelin sheath. The myelin membrane is unique in its relatively high lipid to protein ratio.[16]
In the peripheral nervous system axons are myelinated by glial cells known as Schwann cells. In the central nervous system the myelin sheath is provided by another type of glial cell, the oligodendrocyte. Schwann cells myelinate a single axon. An oligodendrocyte can myelinate up to 50 axons.[17]
The composition of myelin is different in the two types. In the CNS the major myelin protein is proteolipid protein, and in the PNS it is myelin basic protein.
Nodes of Ranvier[edit]
Nodes of Ranvier (also known as myelin sheath gaps) are short unmyelinated segments of a myelinated axon, which are found periodically interspersed between segments of the myelin sheath. Therefore, at the point of the node of Ranvier, the axon is reduced in diameter.[18] These nodes are areas where action potentials can be generated. In saltatory conduction, electrical currents produced at each node of Ranvier are conducted with little attenuation to the next node in line, where they remain strong enough to generate another action potential. Thus in a myelinated axon, action potentials effectively «jump» from node to node, bypassing the myelinated stretches in between, resulting in a propagation speed much faster than even the fastest unmyelinated axon can sustain.
Axon terminals[edit]
An axon can divide into many branches called telodendria (Greek for ‘end of tree’). At the end of each telodendron is an axon terminal (also called a synaptic bouton, or terminal bouton). Axon terminals contain synaptic vesicles that store the neurotransmitter for release at the synapse. This makes multiple synaptic connections with other neurons possible. Sometimes the axon of a neuron may synapse onto dendrites of the same neuron, when it is known as an autapse.
Action potentials[edit]
| Structure of a typical chemical synapse |
|---|
|
Postsynaptic Voltage- Synaptic Neurotransmitter Receptor Neurotransmitter Axon terminal Synaptic cleft Dendrite |
Most axons carry signals in the form of action potentials, which are discrete electrochemical impulses that travel rapidly along an axon, starting at the cell body and terminating at points where the axon makes synaptic contact with target cells. The defining characteristic of an action potential is that it is «all-or-nothing» – every action potential that an axon generates has essentially the same size and shape. This all-or-nothing characteristic allows action potentials to be transmitted from one end of a long axon to the other without any reduction in size. There are, however, some types of neurons with short axons that carry graded electrochemical signals, of variable amplitude.
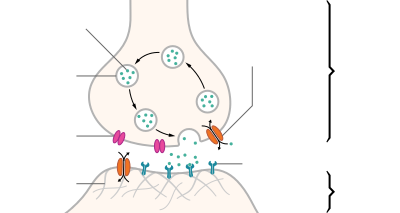
When an action potential reaches a presynaptic terminal, it activates the synaptic transmission process. The first step is rapid opening of calcium ion channels in the membrane of the axon, allowing calcium ions to flow inward across the membrane. The resulting increase in intracellular calcium concentration causes synaptic vesicles (tiny containers enclosed by a lipid membrane) filled with a neurotransmitter chemical to fuse with the axon’s membrane and empty their contents into the extracellular space. The neurotransmitter is released from the presynaptic nerve through exocytosis. The neurotransmitter chemical then diffuses across to receptors located on the membrane of the target cell. The neurotransmitter binds to these receptors and activates them. Depending on the type of receptors that are activated, the effect on the target cell can be to excite the target cell, inhibit it, or alter its metabolism in some way. This entire sequence of events often takes place in less than a thousandth of a second. Afterward, inside the presynaptic terminal, a new set of vesicles is moved into position next to the membrane, ready to be released when the next action potential arrives. The action potential is the final electrical step in the integration of synaptic messages at the scale of the neuron.[5]
(A) pyramidal cell, interneuron, and short durationwaveform (Axon), overlay of the three average waveforms;
(B) Average and standard error of peak-trough time for pyramidal cells interneurons, and putative axons;
(C) Scatter plot of signal to noise ratios for individual units againstpeak-trough time for axons, pyramidal cells (PYR) and interneurons (INT).
Extracellular recordings of action potential propagation in axons has been demonstrated in freely moving animals. While extracellular somatic action potentials have been used to study cellular activity in freely moving animals such as place cells, axonal activity in both white and gray matter can also be recorded. Extracellular recordings of axon action potential propagation is distinct from somatic action potentials in three ways: 1. The signal has a shorter peak-trough duration (~150μs) than of pyramidal cells (~500μs) or interneurons (~250μs). 2. The voltage change is triphasic. 3. Activity recorded on a tetrode is seen on only one of the four recording wires. In recordings from freely moving rats, axonal signals have been isolated in white matter tracts including the alveus and the corpus callosum as well hippocampal gray matter.[19]
In fact, the generation of action potentials in vivo is sequential in nature, and these sequential spikes constitute the digital codes in the neurons. Although previous studies indicate an axonal origin of a single spike evoked by short-term pulses, physiological signals in vivo trigger the initiation of sequential spikes at the cell bodies of the neurons.[20][21]
In addition to propagating action potentials to axonal terminals, the axon is able to amplify the action potentials, which makes sure a secure propagation of sequential action potentials toward the axonal terminal. In terms of molecular mechanisms, voltage-gated sodium channels in the axons possess lower threshold and shorter refractory period in response to short-term pulses.[22]
Development and growth[edit]
Development[edit]
The development of the axon to its target, is one of the six major stages in the overall development of the nervous system.[23] Studies done on cultured hippocampal neurons suggest that neurons initially produce multiple neurites that are equivalent, yet only one of these neurites is destined to become the axon.[24] It is unclear whether axon specification precedes axon elongation or vice versa,[25] although recent evidence points to the latter. If an axon that is not fully developed is cut, the polarity can change and other neurites can potentially become the axon. This alteration of polarity only occurs when the axon is cut at least 10 μm shorter than the other neurites. After the incision is made, the longest neurite will become the future axon and all the other neurites, including the original axon, will turn into dendrites.[26] Imposing an external force on a neurite, causing it to elongate, will make it become an axon.[27] Nonetheless, axonal development is achieved through a complex interplay between extracellular signaling, intracellular signaling and cytoskeletal dynamics.
[edit]
The extracellular signals that propagate through the extracellular matrix surrounding neurons play a prominent role in axonal development.[28] These signaling molecules include proteins, neurotrophic factors, and extracellular matrix and adhesion molecules.
Netrin (also known as UNC-6) a secreted protein, functions in axon formation. When the UNC-5 netrin receptor is mutated, several neurites are irregularly projected out of neurons and finally a single axon is extended anteriorly.[29][30][31][32] The neurotrophic factors – nerve growth factor (NGF), brain-derived neurotrophic factor (BDNF) and neurotrophin-3 (NTF3) are also involved in axon development and bind to Trk receptors.[33]
The ganglioside-converting enzyme plasma membrane ganglioside sialidase (PMGS), which is involved in the activation of TrkA at the tip of neutrites, is required for the elongation of axons. PMGS asymmetrically distributes to the tip of the neurite that is destined to become the future axon.[34]
Intracellular signaling[edit]
During axonal development, the activity of PI3K is increased at the tip of destined axon. Disrupting the activity of PI3K inhibits axonal development. Activation of PI3K results in the production of phosphatidylinositol (3,4,5)-trisphosphate (PtdIns) which can cause significant elongation of a neurite, converting it into an axon. As such, the overexpression of phosphatases that dephosphorylate PtdIns leads into the failure of polarization.[28]
Cytoskeletal dynamics[edit]
The neurite with the lowest actin filament content will become the axon. PGMS concentration and f-actin content are inversely correlated; when PGMS becomes enriched at the tip of a neurite, its f-actin content is substantially decreased.[34] In addition, exposure to actin-depolimerizing drugs and toxin B (which inactivates Rho-signaling) causes the formation of multiple axons. Consequently, the interruption of the actin network in a growth cone will promote its neurite to become the axon.[35]
Growth[edit]
Axon of nine-day-old mouse with growth cone visible
Growing axons move through their environment via the growth cone, which is at the tip of the axon. The growth cone has a broad sheet-like extension called a lamellipodium which contain protrusions called filopodia. The filopodia are the mechanism by which the entire process adheres to surfaces and explores the surrounding environment. Actin plays a major role in the mobility of this system. Environments with high levels of cell adhesion molecules (CAMs) create an ideal environment for axonal growth. This seems to provide a «sticky» surface for axons to grow along. Examples of CAMs specific to neural systems include N-CAM, TAG-1 – an axonal glycoprotein[36] – and MAG, all of which are part of the immunoglobulin superfamily. Another set of molecules called extracellular matrix-adhesion molecules also provide a sticky substrate for axons to grow along. Examples of these molecules include laminin, fibronectin, tenascin, and perlecan. Some of these are surface bound to cells and thus act as short range attractants or repellents. Others are difusible ligands and thus can have long range effects.
Cells called guidepost cells assist in the guidance of neuronal axon growth. These cells that help axon guidance, are typically other neurons that are sometimes immature. When the axon has completed its growth at its connection to the target, the diameter of the axon can increase by up to five times, depending on the speed of conduction required.[37]
It has also been discovered through research that if the axons of a neuron were damaged, as long as the soma (the cell body of a neuron) is not damaged, the axons would regenerate and remake the synaptic connections with neurons with the help of guidepost cells. This is also referred to as neuroregeneration.[38]
Nogo-A is a type of neurite outgrowth inhibitory component that is present in the central nervous system myelin membranes (found in an axon). It has a crucial role in restricting axonal regeneration in adult mammalian central nervous system. In recent studies, if Nogo-A is blocked and neutralized, it is possible to induce long-distance axonal regeneration which leads to enhancement of functional recovery in rats and mouse spinal cord. This has yet to be done on humans.[39] A recent study has also found that macrophages activated through a specific inflammatory pathway activated by the Dectin-1 receptor are capable of promoting axon recovery, also however causing neurotoxicity in the neuron.[40]
Length regulation[edit]
Axons vary largely in length from a few micrometers up to meters in some animals. This emphasizes that there must be a cellular length regulation mechanism allowing the neurons both to sense the length of their axons and to control their growth accordingly. It was discovered that motor proteins play an important role in regulating the length of axons.[41] Based on this observation, researchers developed an explicit model for axonal growth describing how motor proteins could affect the axon length on the molecular level.[42][43][44][45] These studies suggest that motor proteins carry signaling molecules from the soma to the growth cone and vice versa whose concentration oscillates in time with a length-dependent frequency.
Classification[edit]
The axons of neurons in the human peripheral nervous system can be classified based on their physical features and signal conduction properties. Axons were known to have different thicknesses (from 0.1 to 20 µm)[3] and these differences were thought to relate to the speed at which an action potential could travel along the axon – its conductance velocity. Erlanger and Gasser proved this hypothesis, and identified several types of nerve fiber, establishing a relationship between the diameter of an axon and its nerve conduction velocity. They published their findings in 1941 giving the first classification of axons.
Axons are classified in two systems. The first one introduced by Erlanger and Gasser, grouped the fibers into three main groups using the letters A, B, and C. These groups, group A, group B, and group C include both the sensory fibers (afferents) and the motor fibers (efferents). The first group A, was subdivided into alpha, beta, gamma, and delta fibers – Aα, Aβ, Aγ, and Aδ. The motor neurons of the different motor fibers, were the lower motor neurons – alpha motor neuron, beta motor neuron, and gamma motor neuron having the Aα, Aβ, and Aγ nerve fibers, respectively.
Later findings by other researchers identified two groups of Aa fibers that were sensory fibers. These were then introduced into a system that only included sensory fibers (though some of these were mixed nerves and were also motor fibers). This system refers to the sensory groups as Types and uses Roman numerals: Type Ia, Type Ib, Type II, Type III, and Type IV.
Motor[edit]
Lower motor neurons have two kind of fibers:
| Type | Erlanger-Gasser Classification |
Diameter (µm) |
Myelin | Conduction velocity (meters/second) |
Associated muscle fibers |
|---|---|---|---|---|---|
| Alpha (α) motor neuron | Aα | 13–20 | Yes | 80–120 | Extrafusal muscle fibers |
| Beta (β) motor neuron | Aβ | ||||
| Gamma (γ) motor neuron | Aγ | 5-8 | Yes | 4–24[46][47] | Intrafusal muscle fibers |
Sensory[edit]
Different sensory receptors innervate different types of nerve fibers. Proprioceptors are innervated by type Ia, Ib and II sensory fibers, mechanoreceptors by type II and III sensory fibers and nociceptors and thermoreceptors by type III and IV sensory fibers.
| Type | Erlanger-Gasser Classification |
Diameter (µm) |
Myelin | Conduction velocity (m/s) |
Associated sensory receptors | Proprioceptors | Mechanoceptors | Nociceptors and thermoreceptors |
|---|---|---|---|---|---|---|---|---|
| Ia | Aα | 13–20 | Yes | 80–120 | Primary receptors of muscle spindle (annulospiral ending) | ✔ | ||
| Ib | Aα | 13–20 | Yes | 80–120 | Golgi tendon organ | |||
| II | Aβ | 6–12 | Yes | 33–75 | Secondary receptors of muscle spindle (flower-spray ending). All cutaneous mechanoreceptors |
✔ | ||
| III | Aδ | 1–5 | Thin | 3–30 | Free nerve endings of touch and pressure Nociceptors of lateral spinothalamic tract Cold thermoreceptors |
✔ | ||
| IV | C | 0.2–1.5 | No | 0.5–2.0 | Nociceptors of anterior spinothalamic tract Warmth receptors |
Autonomic[edit]
The autonomic nervous system has two kinds of peripheral fibers:
| Type | Erlanger-Gasser Classification |
Diameter (µm) |
Myelin[48] | Conduction velocity (m/s) |
|---|---|---|---|---|
| preganglionic fibers | B | 1–5 | Yes | 3–15 |
| postganglionic fibers | C | 0.2–1.5 | No | 0.5–2.0 |
Clinical significance[edit]
In order of degree of severity, injury to a nerve can be described as neurapraxia, axonotmesis, or neurotmesis.
Concussion is considered a mild form of diffuse axonal injury.[49] Axonal injury can also cause central chromatolysis. The dysfunction of axons in the nervous system is one of the major causes of many inherited neurological disorders that affect both peripheral and central neurons.[5]
When an axon is crushed, an active process of axonal degeneration takes place at the part of the axon furthest from the cell body. This degeneration takes place quickly following the injury, with the part of the axon being sealed off at the membranes and broken down by macrophages. This is known as Wallerian degeneration.[50] Dying back of an axon can also take place in many neurodegenerative diseases, particularly when axonal transport is impaired, this is known as Wallerian-like degeneration.[51] Studies suggest that the degeneration happens as
a result of the axonal protein NMNAT2, being prevented from reaching all of the axon.[52]
Demyelination of axons causes the multitude of neurological symptoms found in the disease multiple sclerosis.
Dysmyelination is the abnormal formation of the myelin sheath. This is implicated in several leukodystrophies, and also in schizophrenia.[53][54][55]
A severe traumatic brain injury can result in widespread lesions to nerve tracts damaging the axons in a condition known as diffuse axonal injury. This can lead to a persistent vegetative state.[56] It has been shown in studies on the rat that axonal damage from a single mild traumatic brain injury, can leave a susceptibility to further damage, after repeated mild traumatic brain injuries.[57]
A nerve guidance conduit is an artificial means of guiding axon growth to enable neuroregeneration, and is one of the many treatments used for different kinds of nerve injury.
History[edit]
German anatomist Otto Friedrich Karl Deiters is generally credited with the discovery of the axon by distinguishing it from the dendrites.[5] Swiss Rüdolf Albert von Kölliker and German Robert Remak were the first to identify and characterize the axon initial segment. Kölliker named the axon in 1896.[58] Louis-Antoine Ranvier was the first to describe the gaps or nodes found on axons and for this contribution these axonal features are now commonly referred to as the nodes of Ranvier. Santiago Ramón y Cajal, a Spanish anatomist, proposed that axons were the output components of neurons, describing their functionality.[5] Joseph Erlanger and Herbert Gasser earlier developed the classification system for peripheral nerve fibers,[59] based on axonal conduction velocity, myelination, fiber size etc. Alan Hodgkin and Andrew Huxley also employed the squid giant axon (1939) and by 1952 they had obtained a full quantitative description of the ionic basis of the action potential, leading to the formulation of the Hodgkin–Huxley model. Hodgkin and Huxley were awarded jointly the Nobel Prize for this work in 1963. The formulae detailing axonal conductance were extended to vertebrates in the Frankenhaeuser–Huxley equations. The understanding of the biochemical basis for action potential propagation has advanced further, and includes many details about individual ion channels.
Other animals[edit]
The axons in invertebrates have been extensively studied. The longfin inshore squid, often used as a model organism has the longest known axon.[60] The giant squid has the largest axon known. Its size ranges from 0.5 (typically) to 1 mm in diameter and is used in the control of its jet propulsion system. The fastest recorded conduction speed of 210 m/s, is found in the ensheathed axons of some pelagic Penaeid shrimps[61] and the usual range is between 90 and 200 meters/s[62] (cf 100–120 m/s for the fastest myelinated vertebrate axon.)
In other cases as seen in rat studies an axon originates from a dendrite; such axons are said to have «dendritic origin». Some axons with dendritic origin similarly have a «proximal» initial segment that starts directly at the axon origin, while others have a «distal» initial segment, discernibly separated from the axon origin.[63] In many species some of the neurons have axons that emanate from the dendrite and not from the cell body, and these are known as axon-carrying dendrites.[1] In many cases, an axon originates at an axon hillock on the soma; such axons are said to have «somatic origin». Some axons with somatic origin have a «proximal» initial segment adjacent the axon hillock, while others have a «distal» initial segment, separated from the soma by an extended axon hillock.[63]
See also[edit]
- Electrophysiology
- Ganglionic eminence
- Giant axonal neuropathy
- Neuronal tracing
- Pioneer axon
References[edit]
- ^ a b Triarhou LC (2014). «Axons emanating from dendrites: phylogenetic repercussions with Cajalian hues». Frontiers in Neuroanatomy. 8: 133. doi:10.3389/fnana.2014.00133. PMC 4235383. PMID 25477788.
- ^ Yau KW (December 1976). «Receptive fields, geometry and conduction block of sensory neurones in the central nervous system of the leech». The Journal of Physiology. 263 (3): 513–38. doi:10.1113/jphysiol.1976.sp011643. PMC 1307715. PMID 1018277.
- ^ a b c Squire, Larry (2013). Fundamental neuroscience (4th ed.). Amsterdam: Elsevier/Academic Press. pp. 61–65. ISBN 978-0-12-385-870-2.
- ^ a b c Luders E, Thompson PM, Toga AW (August 2010). «The development of the corpus callosum in the healthy human brain». The Journal of Neuroscience. 30 (33): 10985–90. doi:10.1523/JNEUROSCI.5122-09.2010. PMC 3197828. PMID 20720105.
- ^ a b c d e Debanne D, Campanac E, Bialowas A, Carlier E, Alcaraz G (April 2011). «Axon physiology» (PDF). Physiological Reviews. 91 (2): 555–602. doi:10.1152/physrev.00048.2009. PMID 21527732. S2CID 13916255.
- ^ Nelson AD, Jenkins PM (2017). «Axonal Membranes and Their Domains: Assembly and Function of the Axon Initial Segment and Node of Ranvier». Frontiers in Cellular Neuroscience. 11: 136. doi:10.3389/fncel.2017.00136. PMC 5422562. PMID 28536506.
- ^ Leterrier C, Clerc N, Rueda-Boroni F, Montersino A, Dargent B, Castets F (2017). «Ankyrin G Membrane Partners Drive the Establishment and Maintenance of the Axon Initial Segment». Frontiers in Cellular Neuroscience. 11: 6. doi:10.3389/fncel.2017.00006. PMC 5266712. PMID 28184187.
- ^ Leterrier C (February 2018). «The Axon Initial Segment: An Updated Viewpoint». The Journal of Neuroscience. 38 (9): 2135–2145. doi:10.1523/jneurosci.1922-17.2018. PMC 6596274. PMID 29378864.
- ^ Rasband MN (August 2010). «The axon initial segment and the maintenance of neuronal polarity». Nature Reviews. Neuroscience. 11 (8): 552–62. doi:10.1038/nrn2852. PMID 20631711. S2CID 23996233.
- ^ a b c d Jones SL, Svitkina TM (2016). «Axon Initial Segment Cytoskeleton: Architecture, Development, and Role in Neuron Polarity». Neural Plasticity. 2016: 6808293. doi:10.1155/2016/6808293. PMC 4967436. PMID 27493806.
- ^ Clark BD, Goldberg EM, Rudy B (December 2009). «Electrogenic tuning of the axon initial segment». The Neuroscientist. 15 (6): 651–68. doi:10.1177/1073858409341973. PMC 2951114. PMID 20007821.
- ^ a b Yamada R, Kuba H (2016). «Structural and Functional Plasticity at the Axon Initial Segment». Frontiers in Cellular Neuroscience. 10: 250. doi:10.3389/fncel.2016.00250. PMC 5078684. PMID 27826229.
- ^ a b Susuki K, Kuba H (March 2016). «Activity-dependent regulation of excitable axonal domains». The Journal of Physiological Sciences. 66 (2): 99–104. doi:10.1007/s12576-015-0413-4. PMID 26464228. S2CID 18862030.
- ^ a b c d e Alberts B (2004). Essential cell biology: an introduction to the molecular biology of the cell (2nd ed.). New York: Garland. pp. 584–587. ISBN 978-0-8153-3481-1.
- ^ a b Alberts B (2002). Molecular biology of the cell (4th ed.). New York: Garland. pp. 979–981. ISBN 978-0-8153-4072-0.
- ^ Ozgen, H; Baron, W; Hoekstra, D; Kahya, N (September 2016). «Oligodendroglial membrane dynamics in relation to myelin biogenesis». Cellular and Molecular Life Sciences. 73 (17): 3291–310. doi:10.1007/s00018-016-2228-8. PMC 4967101. PMID 27141942.
- ^ Sadler, T. (2010). Langman’s medical embryology (11th ed.). Philadelphia: Lippincott William & Wilkins. p. 300. ISBN 978-0-7817-9069-7.
- ^ Hess A, Young JZ (November 1952). «The nodes of Ranvier». Proceedings of the Royal Society of London. Series B, Biological Sciences. Series B. 140 (900): 301–20. Bibcode:1952RSPSB.140..301H. doi:10.1098/rspb.1952.0063. JSTOR 82721. PMID 13003931. S2CID 11963512.
- ^ Robbins AA, Fox SE, Holmes GL, Scott RC, Barry JM (November 2013). «Short duration waveforms recorded extracellularly from freely moving rats are representative of axonal activity». Frontiers in Neural Circuits. 7 (181): 181. doi:10.3389/fncir.2013.00181. PMC 3831546. PMID 24348338.
- ^ Rongjing Ge, Hao Qian and Jin-Hui Wang* (2011) Molecular Brain 4(19), 1~11
- ^ Rongjing Ge, Hao Qian, Na Chen and Jin-Hui Wang* (2014) Molecular Brain 7(26):1-16
- ^ Chen N, Yu J, Qian H, Ge R, Wang JH (July 2010). «Axons amplify somatic incomplete spikes into uniform amplitudes in mouse cortical pyramidal neurons». PLOS ONE. 5 (7): e11868. Bibcode:2010PLoSO…511868C. doi:10.1371/journal.pone.0011868. PMC 2912328. PMID 20686619.
- ^ Wolpert, Lewis (2015). Principles of development (5th ed.). pp. 520–524. ISBN 978-0-19-967814-3.
- ^ Fletcher TL, Banker GA (December 1989). «The establishment of polarity by hippocampal neurons: the relationship between the stage of a cell’s development in situ and its subsequent development in culture». Developmental Biology. 136 (2): 446–54. doi:10.1016/0012-1606(89)90269-8. PMID 2583372.
- ^ Jiang H, Rao Y (May 2005). «Axon formation: fate versus growth». Nature Neuroscience. 8 (5): 544–6. doi:10.1038/nn0505-544. PMID 15856056. S2CID 27728967.
- ^ Goslin K, Banker G (April 1989). «Experimental observations on the development of polarity by hippocampal neurons in culture». The Journal of Cell Biology. 108 (4): 1507–16. doi:10.1083/jcb.108.4.1507. PMC 2115496. PMID 2925793.
- ^ Lamoureux P, Ruthel G, Buxbaum RE, Heidemann SR (November 2002). «Mechanical tension can specify axonal fate in hippocampal neurons». The Journal of Cell Biology. 159 (3): 499–508. doi:10.1083/jcb.200207174. PMC 2173080. PMID 12417580.
- ^ a b Arimura N, Kaibuchi K (March 2007). «Neuronal polarity: from extracellular signals to intracellular mechanisms». Nature Reviews. Neuroscience. 8 (3): 194–205. doi:10.1038/nrn2056. PMID 17311006. S2CID 15556921.
- ^ Neuroglia and pioneer neurons express UNC-6 to provide global and local netrin cues for guiding migrations in C. elegans
- ^ Serafini T, Kennedy TE, Galko MJ, Mirzayan C, Jessell TM, Tessier-Lavigne M (August 1994). «The netrins define a family of axon outgrowth-promoting proteins homologous to C. elegans UNC-6». Cell. 78 (3): 409–24. doi:10.1016/0092-8674(94)90420-0. PMID 8062384. S2CID 22666205.
- ^ Hong K, Hinck L, Nishiyama M, Poo MM, Tessier-Lavigne M, Stein E (June 1999). «A ligand-gated association between cytoplasmic domains of UNC5 and DCC family receptors converts netrin-induced growth cone attraction to repulsion». Cell. 97 (7): 927–41. doi:10.1016/S0092-8674(00)80804-1. PMID 10399920. S2CID 18043414.
- ^ Hedgecock EM, Culotti JG, Hall DH (January 1990). «The unc-5, unc-6, and unc-40 genes guide circumferential migrations of pioneer axons and mesodermal cells on the epidermis in C. elegans». Neuron. 4 (1): 61–85. doi:10.1016/0896-6273(90)90444-K. PMID 2310575. S2CID 23974242.
- ^ Huang EJ, Reichardt LF (2003). «Trk receptors: roles in neuronal signal transduction». Annual Review of Biochemistry. 72: 609–42. doi:10.1146/annurev.biochem.72.121801.161629. PMID 12676795. S2CID 10217268.
- ^ a b Da Silva JS, Hasegawa T, Miyagi T, Dotti CG, Abad-Rodriguez J (May 2005). «Asymmetric membrane ganglioside sialidase activity specifies axonal fate». Nature Neuroscience. 8 (5): 606–15. doi:10.1038/nn1442. PMID 15834419. S2CID 25227765.
- ^ Bradke F, Dotti CG (March 1999). «The role of local actin instability in axon formation». Science. 283 (5409): 1931–4. Bibcode:1999Sci…283.1931B. doi:10.1126/science.283.5409.1931. PMID 10082468.
- ^ Furley AJ, Morton SB, Manalo D, Karagogeos D, Dodd J, Jessell TM (April 1990). «The axonal glycoprotein TAG-1 is an immunoglobulin superfamily member with neurite outgrowth-promoting activity». Cell. 61 (1): 157–70. doi:10.1016/0092-8674(90)90223-2. PMID 2317872. S2CID 28813676.
- ^ Alberts, Bruce (2015). Molecular biology of the cell (Sixth ed.). p. 947. ISBN 9780815344643.
- ^ Kunik D, Dion C, Ozaki T, Levin LA, Costantino S (2011). «Laser-based single-axon transection for high-content axon injury and regeneration studies». PLOS ONE. 6 (11): e26832. Bibcode:2011PLoSO…626832K. doi:10.1371/journal.pone.0026832. PMC 3206876. PMID 22073205.
- ^ Schwab ME (February 2004). «Nogo and axon regeneration». Current Opinion in Neurobiology. 14 (1): 118–24. doi:10.1016/j.conb.2004.01.004. PMID 15018947. S2CID 9672315.
- ^ Gensel JC, Nakamura S, Guan Z, van Rooijen N, Ankeny DP, Popovich PG (March 2009). «Macrophages promote axon regeneration with concurrent neurotoxicity». The Journal of Neuroscience. 29 (12): 3956–68. doi:10.1523/JNEUROSCI.3992-08.2009. PMC 2693768. PMID 19321792.
- ^ Myers KA, Baas PW (September 2007). «Kinesin-5 regulates the growth of the axon by acting as a brake on its microtubule array». The Journal of Cell Biology. 178 (6): 1081–91. doi:10.1083/jcb.200702074. PMC 2064629. PMID 17846176.
- ^ Rishal I, Kam N, Perry RB, Shinder V, Fisher EM, Schiavo G, Fainzilber M (June 2012). «A motor-driven mechanism for cell-length sensing». Cell Reports. 1 (6): 608–16. doi:10.1016/j.celrep.2012.05.013. PMC 3389498. PMID 22773964.
- ^ Karamched BR, Bressloff PC (May 2015). «Delayed feedback model of axonal length sensing». Biophysical Journal. 108 (9): 2408–19. Bibcode:2015BpJ…108.2408K. doi:10.1016/j.bpj.2015.03.055. PMC 4423051. PMID 25954897.
- ^ Bressloff PC, Karamched BR (2015). «A frequency-dependent decoding mechanism for axonal length sensing». Frontiers in Cellular Neuroscience. 9: 281. doi:10.3389/fncel.2015.00281. PMC 4508512. PMID 26257607.
- ^ Folz F, Wettmann L, Morigi G, Kruse K (May 2019). «Sound of an axon’s growth». Physical Review E. 99 (5–1): 050401. arXiv:1807.04799. Bibcode:2019PhRvE..99e0401F. doi:10.1103/PhysRevE.99.050401. PMID 31212501. S2CID 118682719.
- ^ Andrew BL, Part NJ (April 1972). «Properties of fast and slow motor units in hind limb and tail muscles of the rat». Quarterly Journal of Experimental Physiology and Cognate Medical Sciences. 57 (2): 213–25. doi:10.1113/expphysiol.1972.sp002151. PMID 4482075.
- ^ Russell NJ (January 1980). «Axonal conduction velocity changes following muscle tenotomy or deafferentation during development in the rat». The Journal of Physiology. 298: 347–60. doi:10.1113/jphysiol.1980.sp013085. PMC 1279120. PMID 7359413.
- ^ Pocock G, Richards CD, et al. (2004). Human Physiology (2nd ed.). New York: Oxford University Press. pp. 187–189. ISBN 978-0-19-858527-5.
- ^ Dawodu ST (16 August 2017). «Traumatic Brain Injury (TBI) — Definition, Epidemiology, Pathophysiology». Medscape. Archived from the original on 12 June 2018. Retrieved 14 July 2018.
- ^ Trauma and Wallerian Degeneration Archived 2 May 2006 at the Wayback Machine, University of California, San Francisco
- ^ Coleman MP, Freeman MR (1 June 2010). «Wallerian degeneration, wld(s), and nmnat». Annual Review of Neuroscience. 33 (1): 245–67. doi:10.1146/annurev-neuro-060909-153248. PMC 5223592. PMID 20345246.
- ^ Gilley J, Coleman MP (January 2010). «Endogenous Nmnat2 is an essential survival factor for maintenance of healthy axons». PLOS Biology. 8 (1): e1000300. doi:10.1371/journal.pbio.1000300. PMC 2811159. PMID 20126265.
- ^ Krämer-Albers EM, Gehrig-Burger K, Thiele C, Trotter J, Nave KA (November 2006). «Perturbed interactions of mutant proteolipid protein/DM20 with cholesterol and lipid rafts in oligodendroglia: implications for dysmyelination in spastic paraplegia». The Journal of Neuroscience. 26 (45): 11743–52. doi:10.1523/JNEUROSCI.3581-06.2006. PMC 6674790. PMID 17093095.
- ^ Matalon R, Michals-Matalon K, Surendran S, Tyring SK (2006). «Canavan disease: studies on the knockout mouse». N-Acetylaspartate. Adv. Exp. Med. Biol. Advances in Experimental Medicine and Biology. Vol. 576. pp. 77–93, discussion 361–3. doi:10.1007/0-387-30172-0_6. ISBN 978-0-387-30171-6. PMID 16802706. S2CID 44405442.
- ^ Tkachev D, Mimmack ML, Huffaker SJ, Ryan M, Bahn S (August 2007). «Further evidence for altered myelin biosynthesis and glutamatergic dysfunction in schizophrenia». The International Journal of Neuropsychopharmacology. 10 (4): 557–63. doi:10.1017/S1461145706007334. PMID 17291371.
- ^ «Brain Injury, Traumatic». Medcyclopaedia. GE. Archived from the original on 26 May 2011. Retrieved 20 June 2018.
- ^ Wright DK, Brady RD, Kamnaksh A, Trezise J, Sun M, McDonald SJ, et al. (October 2019). «Repeated mild traumatic brain injuries induce persistent changes in plasma protein and magnetic resonance imaging biomarkers in the rat». Scientific Reports. 9 (1): 14626. Bibcode:2019NatSR…914626W. doi:10.1038/s41598-019-51267-w. PMC 6787341. PMID 31602002.
- ^ Finger S (1994). Origins of neuroscience: a history of explorations into brain function. Oxford University Press. p. 47. ISBN 9780195146943. OCLC 27151391.
Kölliker would give the «axon» its name in 1896.
- ^ Grant G (December 2006). «The 1932 and 1944 Nobel Prizes in physiology or medicine: rewards for ground-breaking studies in neurophysiology». Journal of the History of the Neurosciences. 15 (4): 341–57. doi:10.1080/09647040600638981. PMID 16997762. S2CID 37676544.
- ^ Hellier, Jennifer L. (16 December 2014). The Brain, the Nervous System, and Their Diseases [3 volumes]. ABC-CLIO. ISBN 9781610693387. Archived from the original on 14 March 2018.
- ^ Hsu K, Terakawa S (July 1996). «Fenestration in the myelin sheath of nerve fibers of the shrimp: a novel node of excitation for saltatory conduction». Journal of Neurobiology. 30 (3): 397–409. doi:10.1002/(SICI)1097-4695(199607)30:3<397::AID-NEU8>3.0.CO;2-#. PMID 8807532.
- ^ Salzer JL, Zalc B (October 2016). «Myelination». Current Biology. 26 (20): R971–R975. doi:10.1016/j.cub.2016.07.074. PMID 27780071.
- ^ a b Höfflin F, Jack A, Riedel C, Mack-Bucher J, Roos J, Corcelli C, et al. (2017). «Heterogeneity of the Axon Initial Segment in Interneurons and Pyramidal Cells of Rodent Visual Cortex». Frontiers in Cellular Neuroscience. 11: 332. doi:10.3389/fncel.2017.00332. PMC 5684645. PMID 29170630.
External links[edit]
- Histology image: 3_09 at the University of Oklahoma Health Sciences Center – «Slide 3 Spinal cord»
Статья на конкурс «био/мол/текст»: Мозг — довольно сложная штука: вроде бы, о нем много чего известно, но куда больше остается неизведанным. И если о клетках мозга (нейронах) накоплено знаний уже достаточно, то о том, что находится между клетками и непосредственно окружает их — куда меньше. В частности, тело и начальные участки дендритов снаружи клетки опоясывает сетчатая структура, называемая перинейрональной сетью (ПНС), которая практически не изучена! Известно лишь, что основная функция этой сети связана с ограничением синаптической пластичности. Научная группа, в которой я состою, сейчас занимается изучением микроструктуры ПНС. И в этой статье я постараюсь рассказать, что это за сети, чем они интересны, а также показать вклад нашей группы в их изучение.
Конкурс «био/мол/текст»-2017
Эта работа опубликована в номинации «Своя работа» конкурса «био/мол/текст»-2017.
Генеральный спонсор конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Спонсором приза зрительских симпатий и партнером номинации «Биомедицина сегодня и завтра» выступила фирма «Инвитро».
«Книжный» спонсор конкурса — «Альпина нон-фикшн»
Предыстория, или немного о себе
Я учусь в Казанском федеральном университете в Институте фундаментальной медицины и биологии на 5 курсе. А занимаюсь наукой с 1 курса. Попала в научную группу совершенно случайно, считаю это счастливым стечением обстоятельств. Я год отучилась на биологическом направлении, потому что после подачи заявления в университеты не могла понять, чего действительно хочу. Поэтому оставила все документы там, где прошла в первую волну, и это оказался КФУ. Отучилась на биофаке — тогда еще не было медицинских специальностей, открылись они только через год. За этот единственный свой биологический год я сдружилась с одногруппником — Никитой Арнстом. Мне хотелось переплюнуть его в чем-то на тот момент, потому что он очень умный, и шел на биофак осознанно, в отличие от меня. Ему нравилась наука — он много читал, и ему было легко учиться. Я вся такая пубертатная девочка, очень бесилась, когда у него что-то получалось лучше, чем у меня. Но в целом, отношения у нас с ним неплохие, дружеские. И вот, когда я на следующий год отчислилась, и поступила опять-таки в КФУ, только уже на медицинскую биохимию — получать специальность врача, — некоторые предметы зачли, так что свободного времени было побольше. В итоге Никита предложил мне заниматься наукой, а я подумала: «Почему бы и нет, не понравиться — уйду».
Мой научный руководитель — Михаил Николаевич Павельев — тогда работал в Центре нейронаук в Хельсинки и, в основном, общался со мной по скайпу. Провел собеседование, посмотрел мои оценки (я закончила школу с серебряной медалью, в университете экзамены сдавала и сдаю на «отлично»), задавал много вопросов, но на некоторые из них я ответа не знала, и отвечала неуверенно. Сейчас вспоминать это все забавно. Но спустя эти все годы обучения, я поняла, как выросла.
Наша научная группа тогда занималась травмой спинного мозга — в частности, моей темой было наблюдение за поведением животных при восстановлении после операции: контузионная травма спинного мозга. Затем мы переключились на перинейрональные сети. Моя роль в проекте была — съемка на конфокальном микроскопе и анализ изображений. Ну а потом Никите захотелось сменить тему, и мне пришлось взять всю работу на себя, долго учиться окрашиванию тканей головного мозга. Очень тяжело было. Еще Михаил Николаевич поставил задачу найти новых членов группы и обучить их. Теперь в нашей группе Арсений Расческов — студент уже 3 курса лечебного дела, и Анастасия Кочнева — студентка 2 курса биологического направления. Все вместе мы трудимся на благо нашего научного коллектива и университета.
С чего же все началось, или откуда взялись ПНС?
Все началось с итальянского ученого Камилло Гольджи [1]. Он впервые описал перинейрональные сети (ПНС) на поверхности нейронов коры головного мозга кролика. Он предположил, что это «своего рода корсет из нейрокератина, который препятствует прохождению тока от клетки к клетке». Как обычно бывает в науке, никто его находку особо не воспринял. Сантьяго Рамон-и-Кахаль вообще утверждал, что это всего лишь артефакт, полученный от коагуляции внеклеточной жидкости [2], [3]. В то время это был очень влиятельный ученый, и его мнение, прямо скажем, подавило интерес к этой структуре, и постепенно про нее забыли. Но биология развивалась, совершенствовались методики визуализации и окрашивания. Спустя годы интерес вновь вернулся. За несколько десятилетий накоплено внушительное количество данных о молекулах — компонентах ПНС, и их функциях. Но микроструктура остается неизученной [4].
Почему это важно — изучать микроструктуру ПНС?
Макроскопическая картина дает мало информации, и даже под большим увеличением можно лишь понять, стало ПНС больше или меньше, но более тонкие структурные эффекты, увы, увидеть не получается. Наша научная группа занимается анализом изображений, полученных после иммунофлуоресценции и конфокальной микроскопии [5], [6]. И такие изображения, особенно если сделаны на большом увеличении, дают очень много информации, главное — это извлечь ее и сделать выводы.
Итак, мы смотрим пространственную структуру ПНС. Уже известно, что она регулирует ряд функций синапса, и ее структура меняется при:
- Эпилепсии: разрушаются перинейрональные сети [7], [8].
- Посттравматическом синдроме: увеличивается экспрессия (синтез белка, считанного с ДНК) компонентов ПНС [9].
- Психиатрических заболеваниях (например, при шизофрении): возможно, уменьшается количество перинейрональных сетей в зонах, которые связаны с патофизиологией заболевания, и изменяется экспрессия компонентов ПНС [10], [11].
Итак, изучение структуры ПНС поможет понять механизмы этих патологий. Так что область эта очень перспективна и актуальна.
Что такое ПНС и «с чем их едят»
Рисунок 1. Схематическое изображение ПНС, окружающей тело нейрона, а также начальные сегменты дендритов и аксона.
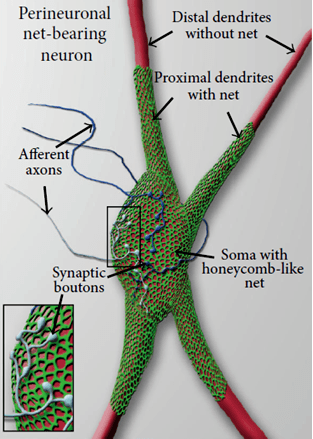
ПНС — это сетчатая структура, окружающая определенные нейроны в головном и спинном мозгах, плотно переплетенная с синаптическими контактами на теле и проксимальных дендритах нейронов [3] (рис. 1).
Перинейрональные сети находят в зрительной коре, соматосенсорной коре, в глубоких ядрах мозжечка, черной субстанции, гиппокампе, а также в спинном мозге [13], [14]. Почему именно там? Потому что ПНС, в основном, окружают тормозные ГАМК-ергические (ГАМК — γ-аминомасляная кислота, тормозной медиатор [15]) интернейроны, а они как раз содержатся в этих зонах. Но исследования по поводу того, какие именно нейроны, помимо ГАМК-ергических, окружены перинейрональными сетями, и в каких пропорциях они окружают нейроны во всех зонах мозга, еще ведутся.
Формируются эти сети во время раннего постнатального развития (период после рождения) ближе к концу критического периода (период, когда нервная система особенно чувствительна к определенным стимулам окружающей среды). Самый интересный факт про ПНС — это то, что они ограничивают синаптическую пластичность.
Синаптическая пластичность — способность нейронных связей перестраиваться в ответ на стимулы окружающей среды и сенсорный опыт (информация, воспринятая через органы чувств). Пластичность играет важную роль в уточнении связей во время развития. Во взрослом состоянии пластичность снижается, но способность не пропадает полностью, нейронные связи продолжают реагировать на опыт, возраст или травмы.
Есть такой фермент — хондроитиназа ABC, — который разрушает ПНС. Так вот, обнаружено, что такое ферментативное разрушение приводит к облегчению синаптической пластичности у взрослых животных [13]. К примеру, проводили исследования на линии мышей с болезнью Альцгеймера [16], у которых была стойкая потеря памяти об объекте в течение трех месяцев. Но после введения им этого фермента, память восстановилась до нормального уровня. А вот если генетически ослабить у таких мышей перинейрональные сети, то начало потери памяти задерживается на несколько недель [11].
Из чего же сделаны ПНС, или много страшных непонятных слов
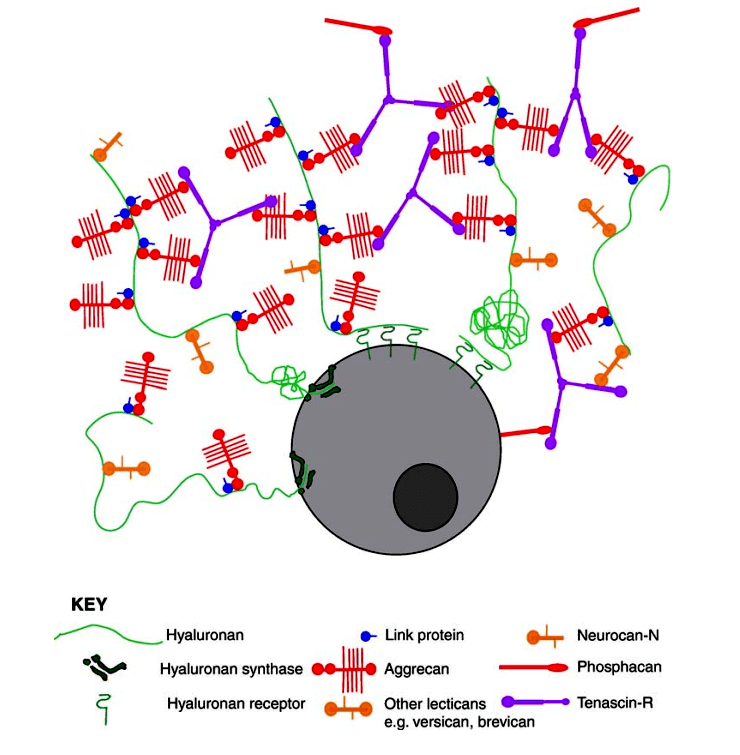
Вообще, ПНС — это всего лишь сочетание белков и протеогликанов, которые секретируются и нейронами, и глией (вспомогательными клетками нервной ткани) на протяжении раннего постнатального развития. И состоят они из четырех компонентов (рис. 2) [17]:
- гиалуроновая кислота — коровая часть;
- хондроитинсульфат протеогликаны (нейрокан, версикан, бревикан, аггрекан — коровые белки, к которым присоединяются цепочки полисахаридов, называемые хондроитинсульфатами) присоединены к коровой части;
- связывающие белки стабилизируют эти соединения;
- тенасцин-R формирует перекрестные связи между этими структурами [18].
Рисунок 2. Модель строения ПНС. Hyaluronan — гиалуроновая кислота (ГК) — каркас. Фермент гиалуронсинтаза (hyaluronan synthase) синтезирует ГК и, вероятно, заякоривает ее в клеточной мембране. С ГК взаимодействуют связывающие белки (link protein), а с ними связываются хондроитинсульфат протеогликаны (ХСПГ) (обозначены красным и оранжевым цветами). С ХСПГ связывается тенасцин-R (tenascin-R), что завершает формирование структуры.
Что же делала наша группа
На самом деле все довольно просто: нужно подготовить материал (в нашем случае головной мозг мыши), сделать срезы, покрасить их, отснять всё, что получилось, на конфокальном микроскопе и проанализировать снимки с помощью компьютера. Все просто, сделай — и сиди отдыхай. 
Но если отбросить шутки в сторону, процедура довольно длительная, сложная, требует концентрации внимания и сноровки. В случае провала на любом этапе нужно искать причину ошибки: что же могло пойти не так? Когда я только начала осваивать гистологическую часть работы, мне это жутко не нравилось. Я очень люблю животных, а тут нужно их забить, извлечь мозг и на все это смотреть беспристрастно… Смотреть было жутко даже со стороны, а уж когда делаешь всё это самостоятельно… Руки дрожат, и ты думаешь только о том, как это ужасно и как бы сделать так, чтобы животное ничего не почувствовало. Приходилось преодолевать страх, чтобы можно было продолжать работу. Сейчас я отношусь к этому более спокойно — рука набилась, все движения отточены. Процедуру забоя нужно проводить как можно быстрее, чтобы животное не успело очнуться и почувствовать невыносимую боль. А ведь оно может умереть раньше, чем нужно, от болевого шока, к тому же выпустив кучу медиаторов стресса типа адреналина, что может повлиять на конечный результат и дать нежелательные микроизменения в мозге. Вот почему всё нужно делать предельно быстро.
Рисунок 3. Вот так выглядит процедура нарезки
Затем нужно извлечь головной мозг из черепной коробки, не повредив его. Конечно, если фиксация прошла хорошо, то делать это намного проще, но все равно тут надо быть крайне внимательным. После подготовительных этапов — фиксации, криопротекции (это нужно для того, чтобы мозг «пережил» дальнейшее замораживание), заключения в среду и замораживания — можно приступать к нарезке материала.
Порезка на криотоме — еще один ужасно трудоемкий этап, где необходимы внимательность и сноровка в кубе, иначе всё насмарку. Нужно сделать очень тонкие срезы (18 мкм) очень острым лезвием (рис. 3). Казалось бы, что сложного? Но в процессе срезы скручиваются и рвутся, что, безусловно, портит препарат. Поэтому тут больше имеет значение опыт.
Очень нужный нам инструмент — беличья кисть, чтобы удерживать срез за край и сделать его ровным. А еще в состав криотома входит так называемая anti-roll plate — по сути, всего лишь прямоугольное стекло, предотвращающее скручивание срезов (рис. 4).
Рисунок 4. Anti-roll plate
И нет ничего лучше, когда процесс нарезки проходит быстро, и срезы получаются ровными, не порванными и просто шикарными. И ты такой радостный на подъеме идешь красить.
Но окрашивание (в нашем случае иммунофлюоресценция [6]) — это еще один этап, и один из самых важных, на котором можно всё испортить. Плохо покрасишь — ничего не увидишь, а значит, все твои старания получить суперкрутые ровные срезы пошли прахом. Этап этот длительный, и здесь тоже очень важны опыт, точное следование протоколу, проверка всех буферов на pH… В общем, очень много тонкостей, чтобы получить качественное окрашивание без высокого фона. Это значит, что те структуры, которые вы покрасили, будут хорошо и четко видны.
Здесь я лишь оговорюсь, что для окрашивания перинейрональных сетей используют биотинилированный лектин (лектин — это углеводсвязывающий белок [19], а слово «биотинилированный» говорит о том, что к этому лектину присоединен биотин) Wisteria floribunda (WFA) (глицинии обильноцветущей), который связывается с углеводным компонентом ПНС. А затем для визуализации применяют флуоресцентный краситель: стрептавидин-меченный AlexaFluor 633.
И вот после этого можно наконец смотреть в микроскоп, делать снимки и их анализировать. Как вы поняли, проще сказать, чем сделать. Поэтому квалифицированный гистолог в научном коллективе на вес золота. Ведь в такого рода исследованиях без гистологии никуда. За дополнительными подробностями о микроскопических методиках можно обратиться к статье «12 методов в картинках: микроскопия» [6].
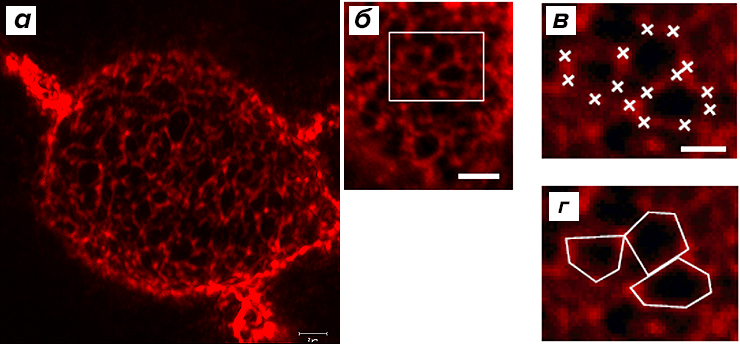
Итог: мы анализировали изображения гистологических срезов соматосенсорной коры взрослых мышей, окрашенных WFA. Получив эти изображения, с помощью специальной программы мы обводили ячейки как многоугольники. Далее у них определяли площадь, периметр и количество вершин. Этот анализ мы провели на телах 34 нейронов из коры мозга мыши (1274 ячейки, 3 мыши) (рис. 5).
Рисунок 5. Структура ПНС кортикальных нейронов взрослых мышей. а — WFA-позитивные ПНС, конфокальный снимок. б — Ячеистая структура ПНС на поверхности тел нейронов. в — Выбор координат вершин ячеек с помощью программы FIJI в области, отмеченной на б. Вершины каждой ячейки метились вручную. г — Результат мечения ячеек на в. Контуры каждой ячейки прорисованы программой, основываясь на координатах вершин.
Всё это мы делаем для того, чтобы копнуть глубже в структуру перинейрональных сетей. Некоторые ячейки окрасились ярче, что означает, что там отложилось больше углеводного компонента — ходроитинсульфат протеогликанов, про которые говорилось выше. Значит синапсы, которые находятся в тех ячейках, окружены более плотно, и им сложнее перестраиваться. Возможно, это является одним из механизмов долговременной памяти.
Обычно все останавливаются на количественном анализе ПНС, а качественно смотрят по компонентам на молекулярном уровне. Но такой анализ изображений поможет другим группам исследователей, занимающихся ПНС, более детально понять данные структуры, посмотреть на то, что происходит при влияниях различных веществ на мозг, при заболеваниях.
Ячейки, ячейки и еще раз ячейки
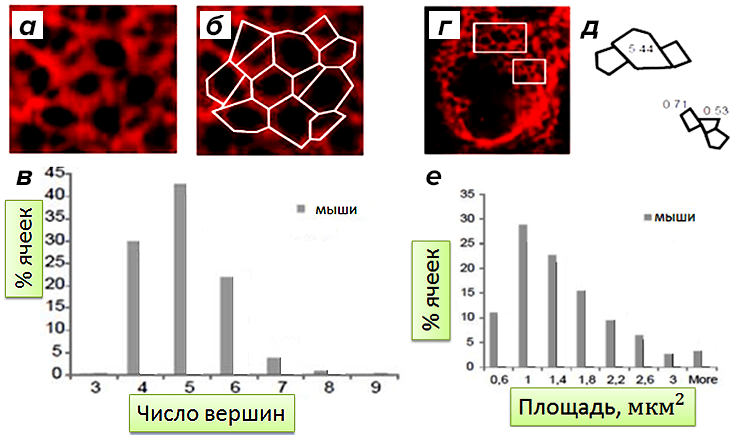
В основном, все ячейки имеют 4-, 5- (самая часто встречающаяся, 44%) или 6-угольную форму. В сумме они составляют 93% проанализированных нами ячеек. Площадь ячеек также варьирует в интервале 0,24–5,48 мкм2 (в среднем 1,29 ± 0,67 мкм2). Это предполагает возможный механизм для регуляции функции синапсов через морфологические ограничения размера ячейки (рис. 6).
Рисунок 6. Параметры ячеек перинейрональных сетей. а и б — Ячейки имеют треугольную, четырехугольную, пятиугольную, шестиугольную и многоугольную форму. в — Гистограмма распределения ячеек с различным числом углов для мышиных нейронов. г — Размер ячеек широко варьирует у отдельных нейронов. д — Контуры ячеек ПНС в двух зонах, отмеченных на г. Крайние значения площадей ячеек показаны в мкм2. е — Гистограмма распределения площадей ячеек для мышиных нейронов.
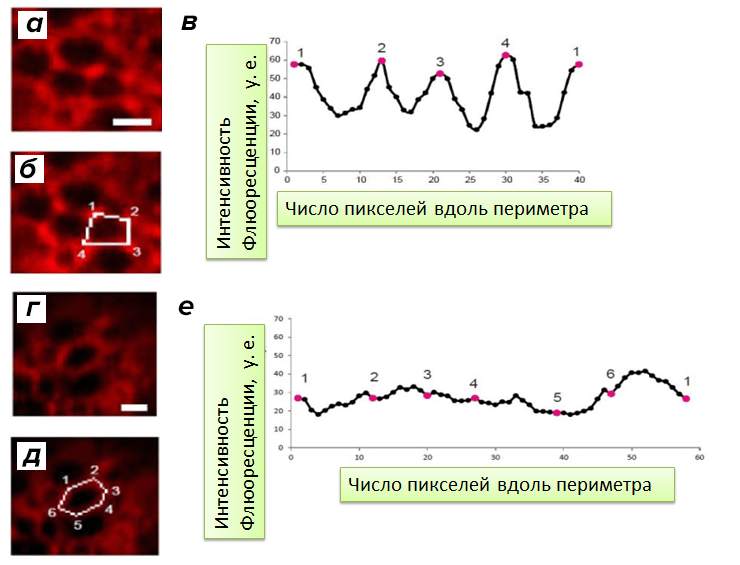
Еще мы обнаружили два варианта распределения интенсивности красителя по периметру ячеек. Первый мы назвали полярным: интенсивность сигнала выше в вершинах, чем в серединах ребер. Второй — неполярный — паттерн характеризуется относительно равномерным распределением интенсивности WFA по периметру ячейки. Все это наглядно показано на рисунке 7.
Рисунок 7. Паттерны распределения WFA вдоль периметра ячейки. а — Полярные ячейки. б — Показан контур ячейки и углы. в — Распределение интенсивности вдоль периметра ячейки, отмеченной на б. г — Неполярная ячейка. д — Контур неполярной ячейки и углы. е — Распределение интенсивности вдоль границы ячейки, отмеченной на д.
Чем важен этот уникальный результат — еще предстоит понять. Возможно, полярные и неполярные ячейки по-разному «окутывают» нейроны, что по-разному действует на синаптическую пластичность и процессы памяти и обучения…
Планы на будущее
Накопилось много данных о том, что же происходит в перинейрональных сетях при различных патологиях: посттравматический синдром, эпилепсия, шизофрения, а также при физиологических состояниях (например, при старении). И здесь очень важно понять, что же происходит на микроструктурном уровне, чтобы применить эти наблюдения при разгадке патогенеза заболеваний и разработке новых видов лечения.
- Окрасивший нейроны;
- Сотворивший нейробиологию: Сантьяго Рамон-и-Кахаль;
- Marco R Celio, Roberto Spreafico, Silvia De Biasi, Laura Vitellaro-Zuccarello. (1998). Perineuronal nets: past and present. Trends in Neurosciences. 21, 510-515;
- Nikita Arnst, Svetlana Kuznetsova, Nikita Lipachev, Nurislam Shaikhutdinov, Anastasiya Melnikova, et. al.. (2016). Spatial patterns and cell surface clusters in perineuronal nets. Brain Research. 1648, 214-223;
- Флуоресцентные репортеры и их молекулярные репортажи;
- 12 методов в картинках: микроскопия;
- Наука из первых рук: как гомеостаз хлора влияет на возникновение эпилепсии;
- Elyse K. Rankin-Gee, Paulette A. McRae, Esther Baranov, Stephanie Rogers, Luke Wandrey, Brenda E. Porter. (2015). Perineuronal net degradation in epilepsy. Epilepsia. 56, 1124-1133;
- Jessica C.F. Kwok, Gunnar Dick, Difei Wang, James W. Fawcett. (2011). Extracellular matrix and perineuronal nets in CNS repair. Devel Neurobio. 71, 1073-1089;
- Болезнь потерянных связей;
- Barbara A. Sorg, Sabina Berretta, Jordan M. Blacktop, James W. Fawcett, Hiroshi Kitagawa, et. al.. (2016). Casting a Wide Net: Role of Perineuronal Nets in Neural Plasticity. J. Neurosci.. 36, 11459-11468;
- F. de Winter, J. C. F. Kwok, J. W. Fawcett, T. T. Vo, D. Carulli, J. Verhaagen. (2016). The Chemorepulsive Protein Semaphorin 3A and Perineuronal Net-Mediated Plasticity. Neural Plasticity. 2016, 1-14;
- T. Pizzorusso. (2002). Reactivation of Ocular Dominance Plasticity in the Adult Visual Cortex. Unknown journal title.. 298, 1248-1251;
- P. A. McRae, M. M. Rocco, G. Kelly, J. C. Brumberg, R. T. Matthews. (2007). Sensory Deprivation Alters Aggrecan and Perineuronal Net Expression in the Mouse Barrel Cortex. Journal of Neuroscience. 27, 5405-5413;
- Спокоен как GABA;
- На руинах памяти: настоящее и будущее болезни Альцгеймера;
- Clare M. Galtrey, James W. Fawcett. (2007). The role of chondroitin sulfate proteoglycans in regeneration and plasticity in the central nervous system. Brain Research Reviews. 54, 1-18;
- Adrienne L. Mueller, Adam Davis, Samantha Sovich, Steven S. Carlson, Farrel R. Robinson. (2016). Distribution of N-Acetylgalactosamine-Positive Perineuronal Nets in the Macaque Brain: Anatomy and Implications. Neural Plasticity. 2016, 1-19;
- Лектины — новые инструменты в диагностике и терапии злокачественных опухолей.