Нервные импульсы распространяются при перемещении ионов через мембрану нервной клетки и передаются из одной нервной клетки в другую с помощью нейромедиаторов.
В результате эволюции нервной системы человека и других животных возникли сложные информационные сети, процессы в которых основаны на химических реакциях. Важнейшим элементом нервной системы являются специализированные клетки нейроны. Нейроны состоят из компактного тела клетки, содержащего ядро и другие органеллы. От этого тела отходит несколько разветвленных отростков. Большинство таких отростков, называемых дендритами, служат точками контакта для приема сигналов от других нейронов. Один отросток, как правило самый длинный, называется аксоном и передает сигналы на другие нейроны. Конец аксона может многократно ветвиться, и каждая из этих более мелких ветвей способна соединиться со следующим нейроном.
Во внешнем слое аксона находится сложная структура, образованная множеством молекул, выступающих в роли каналов, по которым могут поступать ионы — как внутрь, так и наружу клетки. Один конец этих молекул, отклоняясь, присоединяется к атому-мишени. После этого энергия других частей клетки используется на то, чтобы вытолкнуть этот атом за пределы клетки, тогда как процесс, действующий в обратном направлении, вводит внутрь клетки другую молекулу. Наибольшее значение имеет молекулярный насос, который выводит из клетки ионы натрия и вводит в нее ионы калия (натрий-калиевый насос).
Когда клетка находится в покое и не проводит нервных импульсов, натрий-калиевый насос перемещает ионы калия внутрь клетки и выводит ионы натрия наружу (представьте себе клетку, содержащую пресную воду и окруженную соленой водой). Из-за такого дисбаланса разность потенциалов на мембране аксона достигает 70 милливольт (приблизительно 5% от напряжения обычной батарейки АА).
Однако при изменении состояния клетки и стимуляции аксона электрическим импульсом равновесие на мембране нарушается, и натрий-калиевый насос на короткое время начинает работать в обратном направлении. Положительно заряженные ионы натрия проникают внутрь аксона, а ионы калия откачиваются наружу. На мгновение внутренняя среда аксона приобретает положительный заряд. При этом каналы натрий-калиевого насоса деформируются, блокируя дальнейший приток натрия, а ионы калия продолжают выходить наружу, и исходная разность потенциалов восстанавливается. Тем временем ионы натрия распространяются внутри аксона, изменяя мембрану в нижней части аксона. При этом состояние расположенных ниже насосов меняется, способствуя дальнейшему распространению импульса. Резкое изменение напряжения, вызванное стремительными перемещения ионов натрия и калия, называют потенциалом действия. При прохождении потенциала действия через определенную точку аксона, насосы включаются и восстанавливают состояние покоя.
Потенциал действия распространяется довольно медленно — не более доли дюйма за секунду. Для того чтобы увеличить скорость передачи импульса (поскольку, в конце концов, не годится, чтобы сигнал, посланный мозгом, достигал руки лишь через минуту), аксоны окружены оболочкой из миелина, препятствующей притоку и оттоку калия и натрия. Миелиновая оболочка не непрерывна — через определенные интервалы в ней есть разрывы, и нервный импульс перескакивает из одного «окна» в другое, за счет этого скорость передачи импульса возрастает.
Когда импульс достигает конца основной части тела аксона, его необходимо передать либо следующему нижележащему нейрону, либо, если речь идет о нейронах головного мозга, по многочисленным ответвлениям многим другим нейронам. Для такой передачи используется абсолютно иной процесс, нежели для передачи импульса вдоль аксона. Каждый нейрон отделен от своего соседа небольшой щелью, называемой синапсом. Потенциал действия не может перескочить через эту щель, поэтому нужно найти какой-то другой способ для передачи импульса следующему нейрону. В конце каждого отростка имеются крошечные мешочки, называющие (пресинаптическими) пузырьками, в каждом из которых находятся особые соединения — нейромедиаторы. При поступлении потенциала действия из этих пузырьков высвобождаются молекулы нейромедиаторов, пересекающие синапс и присоединяющиеся к специфичным молекулярным рецепторам на мембране нижележащих нейронов. При присоединении нейромедиатора равновесие на мембране нейрона нарушается. Сейчас мы рассмотрим, возникает ли при таком нарушении равновесия новый потенциал действия (нейрофизиологи продолжают искать ответ на этот важный вопрос до сих пор).
После того как нейромедиаторы передадут нервный импульс от одного нейрона на следующий, они могут просто диффундировать, или подвергнуться химическому расщеплению, или вернуться обратно в свои пузырьки (этот процесс нескладно называется обратным захватом). В конце XX века было сделано поразительное научное открытие — оказывается, лекарства, влияющие на выброс и обратный захват нейромедиаторов, могут коренным образом изменять психическое состояние человека. Прозак (Prozac*) и сходные с ним антидепрессанты блокируют обратный захват нейромедиатора серотонина. Складывается впечатление, что болезнь Паркинсона взаимосвязана с дефицитом нейромедиатора допамина в головном мозге. Исследователи, изучающие пограничные состояния в психиатрии, пытаются понять, как эти соединения влияют на человеческий рассудок.
По-прежнему нет ответа на фундаментальный вопрос о том, что же заставляет нейрон инициировать потенциал действия — выражаясь профессиональным языком нейрофизиологов, неясен механизм «запуска» нейрона. В этом отношении особенно интересны нейроны головного мозга, которые могут принимать нейромедиаторы, посланные тысячей соседей. Об обработке и интеграции этих импульсов почти ничего не известно, хотя над этой проблемой работают многие исследовательские группы. Нам известно лишь, что в нейроне осуществляется процесс интеграции поступающих импульсов и выносится решение, следует или нет инициировать потенциал действия и передавать импульс дальше. Этот фундаментальный процесс управляет функционированием всего головного мозга. Неудивительно, что эта величайшая загадка природы остается, по крайней мере сегодня, загадкой и для науки!
См. также:
Очень часто при описании нервной системы используются «электрические» термины: например, нервы сравниваются с проводами. Это потому, что по нервному волокну действительно перемещается электрический сигнал. Каждому из нас известно, что оголенный провод опасен, ведь он бьет током, и по этой причине люди пользуются изоляционными материалами, не проводящими электричество. Природе тоже не чужда техника безопасности, и нервные «провода» она обматывает своим собственным изолирующим материалом — миелином.
Сложная обёртка
Миелин окружает отростки нервных клеток, изолируя их от внешнего воздействия. Это необходимо для более надежной и быстрой передачи сигнала по нервной системе. Благодаря изоляции нервного волокна электрический сигнал не рассеивается и добирается до места назначения без помех. Скорость прохождения сигнала по миелиновым и безмиелиновым волокнам может отличаться на три порядка: от 70 до 140 м/с и от 0,3 до 0,5 м/с соответственно.
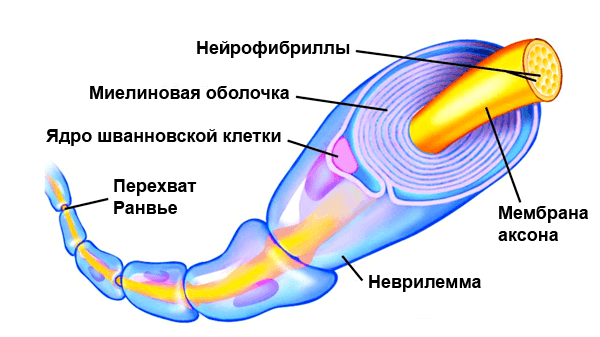
По сути миелин — это клеточная мембрана глиальных клеток, многократно обмотанная вокруг аксона. Сама мембрана на 70–75% состоит из липидов и на 25–30% — из белков. В периферической нервной системе донором мембран становятся шванновские клетки, а в центральной — олигодендроциты. Эти клетки бережно обматывают своими мембранами ценные каналы связи, чтобы обеспечить надежное взаимодействие нервной системы и периферических органов. Миелин покрывает нервное волокно не целиком: существуют промежутки между наслоениями миелина, называемые перехватами Ранвье (рис. 1). Есть прямая зависимость между расстоянием от одного промежутка до другого и скоростью распространения нервного импульса по волокну: чем больше расстояние между перехватами Ранвье, тем выше скорость передачи сигнала в нерве [1].
Рисунок 1. Нервное волокно, обернутое миелином. Видны ядра шванновских клеток (nucleus of Schwann cell) и перехваты Ранвье (nodes of Ranvier) — участки аксона, которые не покрыты миелиновой оболочкой.
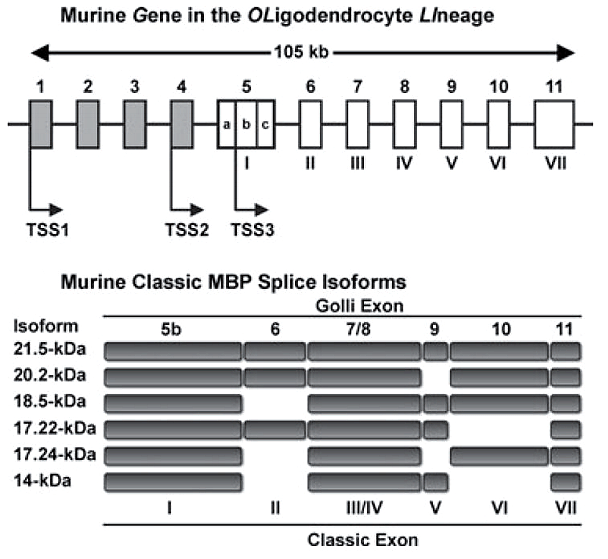
Если говорить о белках, входящих в состав миелина, то надо уточнить, что это не только простые белки. В миелине встречаются гликопротеины — белки, к которым присоединены короткие углеводные последовательности. Важной составляющей миелина является главный структурный белок миелина (myelin basic protein, MBP), впервые выделенный около 50 лет назад. MBP — это трансмембранный белок, который может многократно «прошивать» липидный слой клетки. Его различные изоформы (рис. 2) кодируются геном под названием Golli (gene in the oligodendrocyte lineage). Структурной основой миелина служит изоформа массой 18,5 килодальтон [2].
Рисунок 2. Различные изоформы основного белка миелина (MBP) создаются на основе одного и того же гена. Например, для синтеза изоформы массой 18,5 кДа используются все экзоны, кроме экзона II.
В состав миелина входят сложные липиды цереброзиды. Они представляют собой аминоспирт сфингозин, соединенный с жирной кислотой и остатком углевода. В синтезе липидов миелина принимают участие пероксисомы олигодендроцитов. Пероксисомы — это липидные пузырьки с различными ферментами (в общей сложности известно около 50 видов пероксисомных энзимов). Эти органеллы занимаются, в частности, β-окислением жирных кислот: жирных кислот с очень длинной цепью (very long chain fatty acids, VLCFA), некоторых эйкозаноидов и полиненасыщенных жирных кислот (ПНЖК, polyunsaturated fatty acids, PUFAs). Поскольку миелин может содержать до 70% липидов, пероксисомы крайне важны для нормального метаболизма этого вещества. Они используют N-ацетиласпартат, вырабатываемый нервной клеткой, для постоянного синтеза новых липидов миелина и поддержания его существования. Кроме этого, пероксисомы принимают участие в поддержании энергетического метаболизма аксонов [3].
Важная обёртка
Миелинизация (постепенная изоляция нервных волокон миелином) начинается у людей уже в эмбриональном периоде развития. Первыми этот путь проходят подкорковые структуры. В течение первого года жизни происходит миелинизация отделов периферической и центральной нервной системы, отвечающих за двигательную активность. Миелинизация участков головного мозга, регулирующих высшую нервную деятельность, заканчивается к 12–13 годам. Из этого видно, что миелинизация тесно связана со способностью отделов нервной системы осуществлять специфические для них функции. Вероятно, именно активная работа волокон до рождения запускает их миелинизацию.
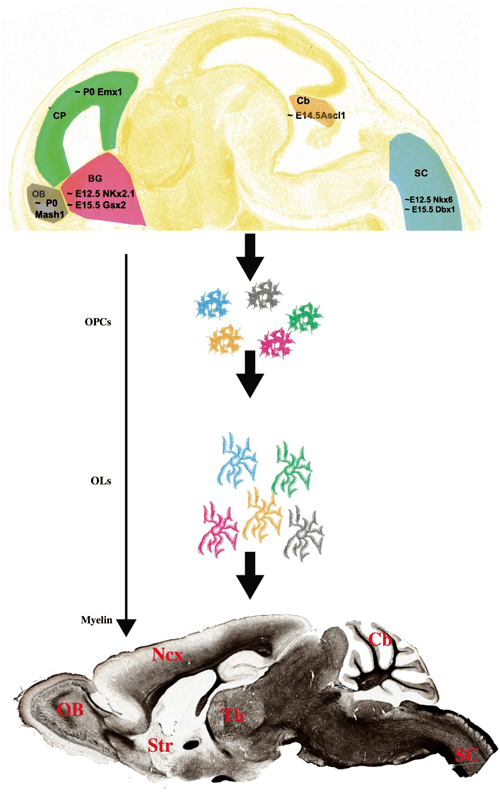
Дифференцировка клеток — предшественниц олигодендроцитов зависит от ряда факторов, связанных с работой нейронов. В частности, работающие отростки нейронов могут выделять белок нейролигин 3, который способствует пролиферации и дифференциации клеток-предшественниц [4]. В дальнейшем созревание олигодендроцитов происходит за счет ряда других факторов. В статье с характерным названием «Насколько велик миелинизирующий оркестр?» описывается происхождение олигодендроцитов в разных частях мозга [5]. Во-первых, в различных частях мозга олигодендроциты начинают созревать в разное время. Во-вторых, за их созревание отвечают разные клеточные факторы, что тоже зависит от региона нервной системы (рис. 3). У нас может возникнуть вопрос: а сходны ли между собой олигодендроциты, появившиеся с таким расхождением в стартовых данных? И насколько схож у них миелин? В целом, авторы статьи считают, что между популяциями олигодендроцитов из разных участков головного мозга действительно существуют различия, и обусловлены они во многом именно местом закладки клеток, воздействием на них окружающих нейронов. И всё же типы миелина, синтезируемые разными пулами олигодендроцитов, не имеют настолько больших отличий, чтобы они не были взаимозаменяемыми.
Рисунок 3. Различия во времени закладки олигодендроцитов в разных отделах головного мозга и в клеточных факторах, влияющих на их развитие.
Сам процесс миелинизации нервных волокон в центральной нервной системе происходит следующим образом (рис. 4). Олигодендроциты выпускают несколько отростков к аксонам разных нейронов. Входя с ними в контакт, отростки олигодендроцитов начинают оборачиваться вокруг них и расползаться по длине аксона. Количество оборотов постепенно увеличивается: в некоторых участках ЦНС их число доходит до 50. Мембраны олигодендроцитов становятся всё более тонкими, распространяясь по поверхности аксона и «выдавливая» из себя цитоплазму. Чем раньше слой миелина был обернут вокруг нервного окончания, тем более тонким он будет. Самый внутренний слой мембраны остается довольно толстым — для осуществления метаболической функции. Новые слои миелина наматываются поверх старых, перекрывая их так, как показано на рисунке 4 — не только сверху, но и увеличивая площадь аксона, покрытую миелином.
Рисунок 4. Миелинизация нервного волокна. Мембрана олигодендроцита наматывается на аксон, постепенно уплотняясь с каждым оборотом. Внутренний, прилегающий к аксону слой мембраны остается относительно толстым, что необходимо для выполнения метаболической функции. На разных частях рисунка (а-в) с разных ракурсов показано постепенное наматывание новых слоев миелина на аксон. Красным цветом выделен более толстый, метаболически активный слой, синим — новые уплотняющиеся слои. Внутренний слой миелина (inner tongue на части б) охватывается всё новыми и новыми слоями мембраны не только сверху, но и по бокам (в), вдоль аксона.
Миелинизация нервных волокон олигодендроцитами также значимо зависит от белка нейрегулина 1. Если он не воздействует на олигодендроциты, то в них запускается программа миелинизации, не учитывающая активность нервной клетки. Если же олигодендроциты получили сигнал от нейрегулина 1, то далее они начнут ориентироваться на работу аксона, и миелинизация будет зависеть от интенсивности выработки глутамата и активации им специфических NMDA-рецепторов на поверхности олигодендроцитов [6]. Нейрегулин 1 — ключевой фактор для запуска процессов миелинизации и в случае шванновских клеток [7].
Изменчивая обёртка
Миелин постоянно образуется и разрушается в человеческом организме. На синтез и распад миелина могут влиять факторы, связанные с особенностями внешней среды. Например, воспитание. С 1965 по 1989 год Румынией руководил Николае Чаушеску. Он установил жесткий контроль над репродуктивным здоровьем и институтом брака в своей стране: усложнил процедуру развода, запретил аборты и ввел ряд стимулов и льгот для женщин, имевших более пяти детей. Итогом этих мер стало ожидаемое повышение рождаемости. Вместе с рождаемостью увеличилось количество криминальных абортов, не добавивших здоровья румынкам, и возросло количество детей-отказников. Последние воспитывались в детских домах, где с ними не очень-то активно общался персонал. Румынские дети в полной мере ощутили на себе то, что называется социальной депривацией — лишение возможности полноценного общения с другими людьми. Если речь идет о маленьком ребенке, то следствиями социальной депривации станут нарушение формирования эмоциональных привязанностей и расстройство внимания. Когда режим Чаушеску пал, западным ученым предстояло в полной мере оценить результат социальной политики этого диктатора. Румынских детей, имеющих выраженные проблемы со вниманием и установкой социальных контактов, впоследствии стали называть детьми Чаушеску.
Кроме различий при выполнении нейропсихологических тестов, у детей Чаушеску по сравнению с детьми, не находившимися в таких условиях, отличалось даже строение головного мозга [8]. При оценке состояния белого вещества мозга ученые используют показатель фрактальной анизотропии. Он позволяет оценить плотность нервных волокон, диаметр аксонов и их миелинизацию. Чем больше фрактальная анизотропия, тем разнообразнее волокна, которые встречаются в этой области мозга. У детей Чаушеску отмечалось снижение фрактальной анизотропии в пучке белого вещества, соединяющего височную и лобную доли в левом полушарии, то есть связи в этом регионе были недостаточно сложными и разнообразными, с нарушениями миелинизации. Такое состояние связей мешает нормальному проведению сигналов между височной и лобной долями. В височной доле находятся центры эмоционального реагирования (миндалина, гиппокамп), а орбитофронтальная кора лобной доли также связана с эмоциями и принятием решений. Нарушение формирования связей между этими отделами мозга и проблемы в их работе в итоге приводили к тому, что выросшие в детдомах дети испытывали трудности в установлении нормальных отношений с другими людьми.
На миелинизацию также может влиять и состав еды, которую дают ребенку. При белково-энергетической недостаточности питания отмечается снижение образования миелина. Недостаток жирных кислот тоже отрицательно сказывается на синтезе этого ценного вещества, так как оно больше чем на 2/3 состоит из липидов. Дефицит железа, йода и витаминов группы В приводит к снижению образования миелина [9]. В основном эти данные были получены при изучении лабораторных животных, но история, к сожалению, дала людям возможность оценить влияние недостатка еды и на формирующийся мозг ребенка [10]. Голодная зима (голл. hongerwinter) 1944–1945 гг. в Нидерландах привела к тому, что родилось множество детей, чьи матери плохо питались. Оказалось, что в условиях голодания мозг этих детей формировался с нарушениями. В частности, наблюдалось большое количество нарушений именно в белом веществе, то есть возникали проблемы с формированием миелина. В итоге это приводило к разнообразным психическим расстройствам.
Поврежденная обёртка
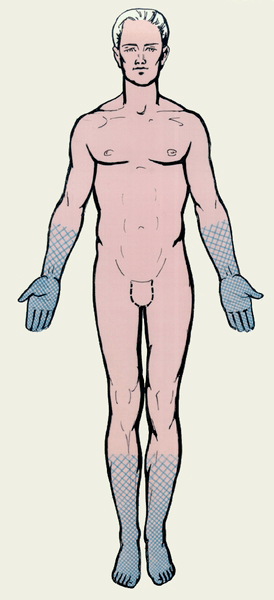
Рисунок 5. Нарушение чувствительности по полиневритическому типу. Название «носки — перчатки» связано с тем, что анатомические зоны, соответствующие поражению нервов, похожи на области, покрываемые этими предметами одежды.
Как мне кажется, для человеческого организма вполне подходит следующее правило: если есть орган, значит, к нему должна быть болезнь. В принципе, это правило можно расширить до молекулярных процессов: есть процесс — есть и болезни, связанные с нарушением этого процесса. В случае с миелином это демиелинизирующие заболевания. Их довольно много, но подробнее я расскажу о двух — синдроме Гийена-Барре и рассеянном склерозе. При этих расстройствах повреждение миелина приводит к нарушению адекватного проведения сигнала по нервам, что и обуславливает симптомы болезни.
Синдром Гийена-Барре (СГБ) — это заболевание периферической нервной системы, при котором происходит разрушение миелиновой оболочки, формируемой шванновскими клетками. СГБ является классическим аутоиммунным заболеванием. Как правило, ему предшествует инфекция (часто — вызванная микробом Campylobacter jejuni). Присутствие различных возбудителей в организме человека запускает аутоиммунное повреждение миелина нервных волокон T- и B-лимфоцитами. Клинически это проявляется мышечной слабостью, нарушением чувствительности по типу «носки — перчатки» (полиневритический тип) (рис. 5). В дальнейшем мышечная слабость может нарастать вплоть до полного паралича конечностей и поражения туловищной мускулатуры. Поражения чувствительной нервной системы также могут быть разнообразны: от снижения способности различать собственные движения (нарушение глубокой чувствительности) до выраженного болевого синдрома. При тяжелых формах СГБ главную опасность представляет потеря способности к самостоятельному дыханию, требующая подключения к аппарату искусственной вентиляции легких (ИВЛ). Для лечения СГБ в настоящее время используют плазмаферез (очистку плазмы от вредных антител) и внутривенные вливания препаратов человеческого иммуноглобулина для нормализации иммунного ответа. В большинстве случаев лечение приводит к стойкому выздоровлению.
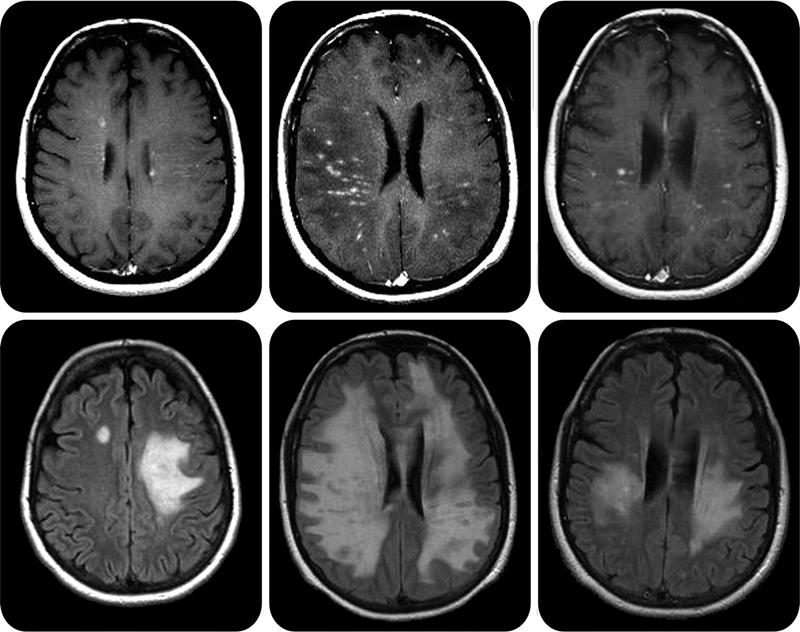
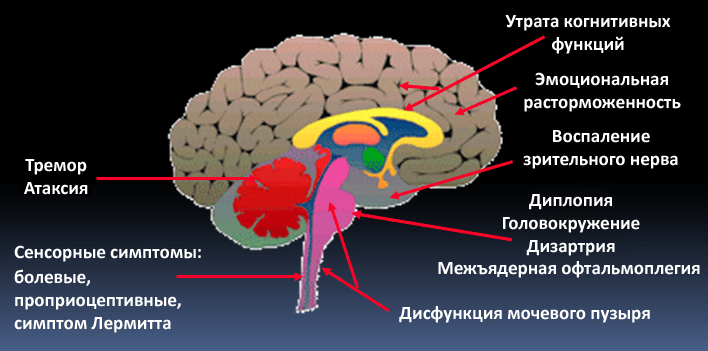
Рассеянный склероз (РС) заметно отличается от СГБ. Во-первых, это демиелинизирующее заболевание приводит к поражению центральной нервной системы, то есть затрагивает миелин, синтезируемый олигодендроцитами. Во-вторых, с причинами РС до сих пор много неясного: слишком большое разнообразие генетических и средовых факторов задействовано в патогенезе заболевания. Принципиальный момент в запуске РС — нарушение непроницаемости гематоэнцефалического барьера (ГЭБ) для иммунных клеток. В норме ткань мозга отгорожена от всего остального организма этим надежным фильтром, который не пропускает к ней множество веществ и клеток, в том числе иммунных. ГЭБ появляется уже в эмбриональном периоде развития, изолируя ткань мозга от формирующейся иммунной системы. В это время иммунная система человека «знакомится» со всеми существующими тканями, чтобы в дальнейшем, при взрослой жизни, не нападать на них. Мозг и ряд других органов остаются «не представленными» иммунной системе. При нарушении целостности ГЭБ иммунные клетки получают возможность для атаки незнакомых ей тканей мозга. В-третьих, РС отличается более тяжелыми симптомами, которые требуют других терапевтических подходов. Симптоматика зависит от того, где локализуются повреждения нервной системы (рис. 6 и 7). Это может быть шаткость походки, нарушения чувствительности, различные когнитивные симптомы. Для лечения РС используются высокие дозы глюкокортикоидов и цитостатики, а также препараты интерферона и специфические антитела (натализумаб). По-видимому, в дальнейшем будут развиваться новые методы лечения РС, основанные непосредственно на восстановлении миелиновой оболочки в поврежденных участках мозга. Ученые указывают на возможность трансплантации клеток — предшественниц олигодендроцитов или усиления их роста за счет введения инсулиноподобного фактора роста или тиреоидных гормонов [11]. Однако это еще впереди, а пока неврологам недоступны более «молекулярные» методы лечения.
Рисунок 6. Очаги поражения центральной нервной системы при рассеянном склерозе на МРТ выглядят как белые бляшки.
Рисунок 7. В зависимости от места поражения нервной системы при рассеянном склерозе может быть разная симптоматика: от тремора и атаксии при повреждении мозжечка до эмоциональных расстройств при локализации очагов в лобных долях.
- Wu L.M., Williams A., Delaney A., Sherman D.L., Brophy P.J. (2012). Increasing internodal distance in myelinated nerves accelerates nerve conduction to a flat maximum. Curr. Biol. 22, 1957–1961;
- Harauz G. and Boggs J.M. (2013). Myelin management by the 18.5-kDa and 21.5-kDa classic myelin basic protein isoforms. J. Neurochem. 125, 334–361;
- Kassmann C.M. (2014). Myelin peroxisomes — essential organelles for the maintenance of white matter in the nervous system. Biochemie. 98, 111–118;
- Venkatesh H.S., Johung T.B., Caretti V., Noll A., Tang Y., Nagaraja S. et al. (2015). Neuronal activity promotes glioma growth through neuroligin-3 secretion. Cell. 161, 803–816;
- Tomassy G.S. and Fossati V. (2014). How big is the myelinating orchestra? Cellular diversity within the oligodendrocyte lineage: facts and hypotheses. Front. Cell Neurosci. 8, 201;
- Michalski J.-P. and Kothary R. (2015). Oligodendrocytes in a nutshell. Front. Cell Neurosci. 9, 340;
- Salzer J.L. (2012). Axonal regulation of Schwann cell ensheathment and myelination. J. Peripher. Nerv. Syst. 17, 14–19;
- Eluvathingal T.J., Chugani H.T., Behen M.E., Juhász C., Muzik O., Maqbool M. et al. (2006). Abnormal brain connectivity in children after early severe socioemotional deprivation: a diffusion tensor imaging study. Pediatrics. 117, 2093–2100;
- Prado E.L. and Dewey K.G. (2014). Nutrition and brain development in early life. Nutr. Rev. 72, 267–284;
- Hulshoff Pol H.E., Hoek H.W., Susser E., Brown A.S., Dingemans A., Schnack H.G. et al. (2000). Prenatal exposure to famine and brain morphology in schizophrenia. Am. J. Psychiatry. 157, 1170–1172;
- Bhatt A., Fan L.W., Pang Y. (2014). Strategies for myelin regeneration: lessons learned from development. Neural. Regen. Res. 9, 1347–1350.
ФИЗИКА ЖИЗНЕННЫХ ПРОЦЕССОВ
АКСОН И НЕРВНЫЙ ИМПУЛЬС
Генерация и распространение нервного импульса в организмах животных, возбуждение нервных и мышечных клеток — важнейшие мембранные явления. Мембранная теория возбуждения была сформулирована Бернштейном еще в 1902 г. [1]. Согласно его теории, возбуждение определяется электрохимическими процессами, локализованными в мембранах нервных и мышечных клеток. Эти процессы сводятся к перемещению малых ионов. Позднее Лазарев опубликовал монографию об ионной природе нервного возбуждения [2]. Исследования, проведенные Ходжки- ном, Катцем, Хаксли, Тасаки и другими учеными [3—6], раскрыли принципиальные механизмы генерации нервного импульса и его распространения (см. также [7—9]).
Нервное возбуждение распространяется по нервным волокнам— аксонам. Принято разделять нервную систему высших организмов на центральную и периферическую. Периферическая система содержит аксоны, служащие для передачи сигналов, а также ганглии вегетативной нервной системы. Аксоны являются коммуникациями для афферентных сообщений от органов чувств, направляемых в центральную систему, и для эфферентных сигналов, направляющихся от центральной системы к мышцам. Аксоны представляют собой отростки центрально расположенных клеток. Нервная система беспозвоночных имеет иное строение, но она также содержит коммуникационные аксоны.
Исследование генерации нервного импульса и его распространения в аксоне — старая и традиционная проблема биофизики/ Уже Гельмгольц измерял скорость распространения нервного возбуждения/В настоящее время решены важные физические задачи, относящиеся к функции аксона. Напротив, современное состояние науки позволяет лишь формально моделировать работу центральной нервной системы и мы еще далеки от понимания физической природы высших ее функций — памяти и мышления.
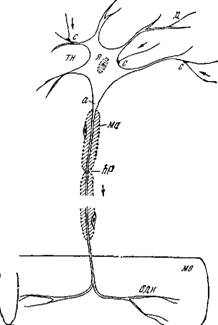
На рис. 4.1, заимствованном из [5], представлена схема строения нервной клетки, именуемой иначе нейроном. Нейрон полу
чает сообщения от многих других нейронов через их тонкие ответвления, образующие контакты — синапсы — с телом клетки и его короткими отростками — дендритами. Аксон имеет макроскопические протяженность и сечение. Длины аксонов в теле крупных животных достигают нескольких метров.
Контакты с другими клетками образуются не только в синапсах.^ Боль — шая часть поверхности нейрона покрыта прилегающими к нему глиальными, или иіванновскими, клетками^ роль которых пока не выяснена. С другой стороны^из мембран шванновских клеток образуется миелиновая оболочка миелинизирован — ных аксонов, показанная ^схематически на рис. 4.1. ^Оболочка прерывается через каждые 1—2 мм длины аксона перехватами Ранвье, имеющими протяженность /Т около 1 мкм. В области перехватов мембрана аксона непосредственно контактирует с окружающей средойЛ^
Немиелинизированные во — ЛОКНа могут быть объеди — Рис. 4.1. Схема строения нервной клетки нены одной шванновской (двигательный нейрон).
К-ТТР. ТКПЙ чтп ППКЯ1ЯНП R гр — і тн~тел0 нейрона,1Ца — аксои1Смо — миелиновая клеткой, ЧТО UOKdJdHU В се ~ оболочка, перехват Ранвье^д-дендрит,
ЧЄНИИ на рис. 4.2. Погру — X*— ядро,^с —синапсыЛодн—окончание двига о г — г тельного нерва,мв — мышечное волокно.
Женныи в шванНЬвскую 1
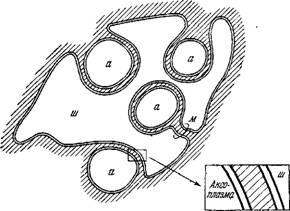
Клетку аксон создает глубокую инвагинацию мембраны шванновской клетки, причем образуется мезаксон — две шванновские мембраны, расположенные рядом^В правом нижнем углу схематически показана двойная мембрана, разделяющая цитоплазму шванновской клетки и цитоплазму аксона, аксоплазму [9].
Герен [10] установила, что миелиновая оболочка аксона образована многократным спиральным закручиванием мембраны шванновской клетки вокруг аксоиаГМиелин представляет собой, — т-а«им~ойразом,/многослойную (доЧїбО слоев) мембрану, строение которой наблюдается с помощью электронного микроскопа. Миелии защищает мембрану аксона от окружающей среды.
6 М. В. Волькеиштейн
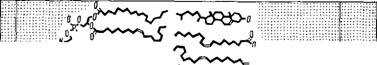
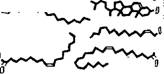
Структура миелина была детально изучена методом рентгенографии с разрешением 10 А [11]. Определены профили электронной плотности миелина седалищного нерва кролика и лягушки и миелина зрительного нерва кролика. На рнс. 4.3 показаны эти кривые для нервных волокон кролика и схема структуры миелина, соответствующая данным кривым. Миелин построен асимметрично, холестерин сосредоточен преимущественно на стороне
Рис. 4.2. Схема строения немиелинизированнного нервного волокна позвоночного.
А — аксон, м — мезаксон— шванновская клетка.
Миелина, соприкасающейся с мембраной аксона. Схема согласуется с липидным составом миелина млекопитающих, установленным ранее [12]. Белковые слои граничных областей миелина содержат йоду. Внутренняя область построена из гибких углевОдорОдных «хвостов» липидов.
/Уже давно установлено, что нервы и мышцы способны генерировать электродвижущие силы, биопотенциалы. Электрическая активность клеток проявляется в форме коротких разрядов, каждый из которых длится около 1 мс. Современная экспериментальная техника позволяет усиливать эти сигналы и регистрировать их с помощью осциллографа или другим путем. Установлено, что активность нерва всегда сопровождается электрическими явлениями — и при внешнем возбуждении и при посылке сигнала мозгом в соответствующем аксоне наблюдаются электрические импульсы. На рис. 4.4 показаны импульсы в зрительном нервном волокні краба Limulus, вызванные вспышкой света длительностью 1 с [13]. Частота и характер последовательности импульсов, имеющие несомненное информационное значе
ние, зависят от интенсивности и спектрального состава света [14, 15] (см. гл. 7) .1 Величина и длительность отдельного импульса не зависят отТгрироды и силы раздражения.»
О 20 40А
-J 1 1 1 1
0 0 .::•:
»w0#0
^ V J 1 O^^-v^.p..
Г У. Го 0
Внугрен^/7о/тярже=Стероид щ^Гибх/гя ^Стероид ^//плярная Внешний
Нийбеяоцт. группы^ +ягесткая цепь +жесткая белок
+еоЗа ‘— » цепь — цепь — —~ +вода углеводороды
Рис. 4.3. Схема миелиновой мембранной структуры.
Вверх* — профили электронной плотности для глазного (пунктир) н седалищного (сплошная
Лнння) нервов кролика.
Электрический сигнал, отвечающий отдельному импульсу, распространяющемуся вдоль аксона, называется потенциалом действия или спайком. Это — основная единица информации, передаваемой по нервному волокну.
Скорость распространения импульса по аксону равна по порядку величины 1—100 м/с, она меньше для немиелинизиро — ванных и больше для миелинизированных аксонов.
0,01
0,001
Рис. 4.4. Импульсы в зрительном нервном волокне Limulus, вызванные вспышкой света длительностью I с.
Цифры справа указывают относительную интенсивность вспышки. Период освещения указан разрывом верхней белой линии, отметка времени на нижней белой линии 0,2 с.
В табл. 4.1 [3] приведены некоторые данные. Проведение нервного возбуждения есть проведение электрического импульса. Несмотря на то, что аксоплазма представляет
Таблица 4.1
Скорость проведения возбуждения в нервном н мышечном волокнах
|
Волокно |
Температура, °С |
Диаметр волокна мкм |
Скорость проведения, м/с |
|
Миелинизированные нервные волок |
38 |
2-20 |
10-100 |
|
На кошки |
|||
|
Немиелинизированные нервные во |
38 |
0,3-1,3 |
0,7—2,3 |
|
Локна кошки |
|||
|
Миелинизированные нервные волок |
20 |
3-16 |
6-32 |
|
На лягушки |
35 |
||
|
Миелинизированные нервные во |
20 |
20 |
|
|
Локна креветки |
|||
|
Немиелинизированные нервные во |
20 |
30 |
5 |
|
Локна краба |
|||
|
Гигантский аксон кальмара (немие- |
20 |
500 |
Около 25 |
|
Линизированное волокно) |
|||
|
Мышечное волокно лягушки |
20 |
60 |
1,6 |
‘) Для миелинизированных волокон указаны значения наружного диа^ метра миелиновой оболочки.
Собой раствор электролитов, никоим образом нельзя считать, что ионный ток в ней определяет распространение импульса. («Удельное сопротивление аксоплазмы равно по порядку величины 10—100 Ом-см. Следовательно, сопротивление на единицу длины волокна диаметром 1 мкм составляет 109—Ю10Ом-см, т. е. превышает сопротивление медного провода того же диаметра в 108 раз. В таком проводнике очень велики потери и утечки. Между тем аксон передает первичный импульс на расстояния свыше метра б^а-затухания. и без иска^кения.^.
В нейрофизиологии и в биофизике нервнЪ’го»»возбуждения сыграло большую роль развитие методов работы на изолированных аксонах, техники введения микроэлектродов в аксон и метода перфузии, т. е. выдавливания аксоплазмы из волокна и ее замены искусственными растворамиДОсобенно удобна работа на гигантских аксонах кальмара, имеющих диаметр до 0,5 мм (см. табл. 4.1 ^Элементарный опыт состоит во введении в аксон двух микроэлектродов: первый служит для электрической стимуляции возбуждения, второй-^- для измерения генерируемого потенциала (рис. 4.5) [4]./Опыт показывает, что «»величина и временной ход токов действия совершенно не зависят от величины стимулирующего тока и что потенциал действия не возникает, если электрический стимул не достигает некоторого порогового потенциала. Тем самым, нервное волокно
Гл. 4. нервный импульс
Подчиняется закону «все или ничего». Иными словами, потенциал действия постоянной величины либо возникает, либо не возникает вовсе.
Для возбуждения аксона необходимо некоторое минимальное количество электричества.,’ Соответственно по мере уменьшения
Раздражение Осцилмерар
ЕЖЖ^,..»,, ,
Аксон
Рис. 4.5. Схема исследования нервного импульса при помощи двух микроэлектродов.
Длительности At подаваемого импульса необходимо увеличивать силу тока / — эти две величины обратно пропорциональны. Для длительных прямоугольных импульсов существует минимальная
Сила тока, достаточная для возбуждения; более слабый ток неэффективен при любой длительности.
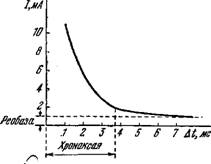
Fta рис. 3/S показана кривая зависимости силы порогового тока от длительности импульса. Кривая имеет гиперболическую форму. Было предложено описывать ее эмпирической формулой
/п = а/At — f b,
Где Іп— пороговый ток, At— длительность импульса, b — так называемая реобаза — минимальное значение возбуждающего тока при At-> оо. При очень коротких импульсах, т. е. при At—>-0 /п = а/At, т. е. произведение IaAt есть константа, характеризующая пороговое значение количества электричества при коротких импульсах. Из приведенной формулы следует, что при /п = 2b получим А^хр = а/Ь. В действительности, однако, оказалось, что при At = ajb /п~1,4Ь и простая эмпирическая формула несправедлива во всем интервале значений A^.j
166
Рисі 4.6. Зависимость силы порогового тока от длительности импульса.
Если сообщить волокну два последовательных стимула, разделенных некоторым интервалом времени, то возникающая ситуация зависит от этого интервала. Немедленно после генерации импульса данное место волокна находится в абсолютном
Рефрактерном состоянии, т. е. не может быть возбуждено вновь. Затем следует относительное рефрактерное состояние. В таком состоянии заметно увеличено значение порогового потенциала и может возникнуть лишь медленно распространяющийся импульс. Продолжительность всего рефрактерного состояния варьирует от одной до нескольких миллисекунд.
В состоянии покоя аксоплазма имеет отрицательный заряд по отношению к внешней среде, характеризуемый потенциалом покоя около 80 мВ. Пороговое возбуждение при этом имеет потенциал, примерно равный —50 мВ, а потенциал действия при надпороговом возбуждении равен потенциалу противоположного знака, составляющему около 40 мВ. Это изображено схематически на рис. 4.7 [4].
Прохождение импульса определяется изменением состояния мембраны аксона при ее стимуляции. Как уже говорилось, в состоянии покоя клеточной мембраны в результате активного транспорта ионов концентрация ионов К+ в цитоплазме (аксо — плазме) значительно превосходит их концентрацию во внешней среде, а для ионов Na+ ситуация противоположна^ В табл. 4.2 [3] приведен состав аксоплазми аксонов Loligo и состав плазмы крови, характерный для внешней среды, и близкий к нему состав морской воды.
Таблица 4.2 Концентрация нонов н других веществ в аксонах Loligo
Концентрация, ммоль на 1 кг НаО
|
Вещество |
Морская |
||
|
Аксоплазма |
Кровь |
Вода |
|
|
К+ |
400 |
20 |
10 |
|
Na+ |
50 |
440 |
460 |
|
Сг |
40—150 |
560 |
540 |
|
Са++ |
0,4 |
10 |
10 |
|
Mg++ |
10 |
54 |
53 |
|
Изэтионовая кислота |
250 |
— |
— |
|
Аспарагнновая кислота |
75 |
— |
— |
|
Глутаминовая кислота |
12 |
— |
— |
|
Янтарная н фумаровая кислоты |
17 |
— |
— |
|
Ортофосфат |
2,5-9 |
— |
— |
|
АТФ |
0,7—1,7 |
— |
— |
|
Аргннннфосфат |
1,8-5,7 865 г/кг |
— |
— |
|
Вода |
870 г/кг |
966 г/кг |
При наложении на мембрану стимулирующего потенциала вначале увеличивается ее проницаемость для ионов Na+, в состоянии покоя значительно меньшая проницаемости для ионов К+. Ионы Na+ входят в аксон, в результате чего внутренняя поверхность мембраны изменяет знак своего заряда с отрицательного на положительный. Иными словами, происходит деполяризация мембраныЛЕсли воспользоваться для выражения разности потенциалов на двух сторонах мембраны аксона формулой (3.105)
+ + (4.1)
^ РКСК + PNacNa + РС1сС ‘
То состояние покоя мембраны характеризуется следующим отношением ионных проницаемостей:
Рк ■ ^Na •’ Реї = 1 : 0,04:0,45.
В состоянии возбуждения, отвечающем генерации потенциала действия, имеем
Рк: Pnа: Ра = 1 :20: 0,45.
Подчеркнем, что истолкование возбуждения как результата изменения ионных проницаемостей является феноменологическим и не раскрывает молекулярный механизм процесса.
Наружная среда
Активный участок
+ + + — — — — + + + + +
Импульс Э-
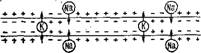
Электрические токи, возникающие при деполяризации мембраны аксона.
При деполяризации мембраны возникают токи, замыкающиеся через наружную проводящую среду (рис. 4.8) [5]. Они возбуждают следующий участок аксона.
Таким образом, согласно мембранной теории при генерации импульса в мембране аксона открывается некий «канал», сквозь который ионы Na+ проникают внутрь аксона, вызывая деполяризацию мембраны. Во время генерации импульса натриевый канал закрывается и открывается калиевый канал. Ионы К+ выходят наружу, что приводит к восстановлению нормального отрицательного заряда на внутренней стороне мембраны. Происходит реполяризация мембраны. После прохождения рефрактерного периода мембрана приобретает способность передавать новый импульс (рис. 4.9) (4].
+40 О
-за
3
Оотенциол действия
Птещиал пот
+ к — — у + + + + + + + + + + + +
Їфі TtII ‘МрЖ. 111111
+ T —+ + + + + + + + + + + ®
+40
О
+ + + + + + + + І » + + + + + + + + + + + + + + ї—+ + + + + +
+40 О
-ВО
Рис. 4.9. Распространение нервного импульса сопровождается изменениями нонной проницаемости мембранного аксона.
Наружный раствор
/ / і ±
А/гсоплаэма
Рнс. 4.10. Эквивалентная схема элемента возбудимой мембраны аксона.
Как видно из рис. 4.8, суммарный продольный ток через сечение аксона и окружающую среду равен нулю — в любом месте внутренние токи равны по силе и противоположны по направлению. Но плотность продольного тока и продольная разность потенциалов между двумя точками внутри аксона иные, чем снаружи.
Мембрана аксона имеет сопротивление 1000 Ом-см2, ее емкость равна 1 мкФ/см2, что соответствует бимолекулярному липидному слою толщиной 50 А с диэлектрической проницаемостью е=5 и удельным сопротивлением 2-Ю9 Ом-см. Во время генерации импульса проводимость мембраны увеличивается примерно в 1000 раз. Можно моделировать электрические свойства мембраны эквивалентной схемой, показанной на рис. 4.10 [3]. Рисунок изображает лишь один элемент мембраны, и следует представить себе длинную линейную последовательность таких элементов, моделирующих непрерывный кабель. Сопротивление R характеризует аксоплазму, наружный раствор имеется в большом избытке и изображается проводником без сопротивления. Натриевая и калиевая «батареи» и S’k,
Определяют генерацию импульса, добавочная «батарея» Sy ответственна за движение других ионов, не изменяющееся при возбуждении.
Таким образом, распространение импульса представляет собой самоподдерживающийся процесс, подобный горению бикфордова шнура. Очевидно, что процесс этот сводится к превращению химической энергии в электрическую.
Как уже сказано, распространение импульса в миелинизированном волокне происходит быстрее, чем в немиелинизированном. Доказано, что в миелинизированном аксоне проведение импульса является сальтаторным, т. е. происходит путем перескока импульса от одного перехвата Ранвье к другому. Калиевые и натриевые каналы открываются и закрываются только в перехватах Ранвье — миелинизированные участки хорошо изолированы. Миелин имеет малую емкость, чем и объясняется большая скорость проведения импульса. Схема сальтаторного проведения импульса показана на рис. 4.11. ^
РирГ 4.Т7Т^ Схема сальтаторного проведения импульса. пР—перехват Ранвье, л —миелин, а — аксо-
Прямые доказательства сальтаторной їеории, впервые предложенной Лилли [16], были получены в работах Кубо, Оно и Юге (см. [17]). В одиночном нервно-мышечном препарате, погруженном в раствор Рингера, пороговая величина стиму
лирующего тока зависит от расстояния между стимулирующим микрозлектродом и перехватом Ранвье. Она имеет наименьшее значение, если микрозлектрод помещен непосредственно в перехвате. Количественная теория этого эффекта была развита Та — саки (см. [6]).
Обозначим потенциалы трех последовательных перехватов — 1, 0 и 1 буквами ifi_i, if)0 и ij)j. Если миелин представляет собой идеальный изолятор, то ток, протекающий внутри аксона от 1 к 0, пропорционален if>i— if>o, от 0 к —1 — пропорционален ■ф-i — if>o. Через перехват 0 идет ток І, пропорциональный (грі — ij)0) — f (j)_i — %,). Имеем
‘ = І{(+-,-*о) + (+,-+о)}. (4.2)
Где R — сопротивление между двумя соседними перехватами (оно равно примерно 20 МОм).
Расстояния между микроэлектродом и перехватами 0, 1 и —1 равны Хо, Х, х-. Разность потенциалов, создаваемая микроэлектродом, дающим ток I, равна
Где р — удельное сопротивление среды (для раствора Рингера оно равно 100 Ом-см). Из (4.2) и (4.3) получаем
TOC o «1-3» h z i = Ч (4-4)
4яR х0 х х-1 ) 4 ‘
И если микроэлектрод очень близок к перехвату 0, т. е. Хи Х-1 » *0, то
= (4-5)
В опытах варьировалось расстояние х0 и при каждом значении Хо определялась величина /, отвечающая критическому значению і — іс. Опытные данные действительно согласуются с линейной зависимостью I от х0
І= — Ісх0. (4.6)
Установлено, что факторы, блокирующие распространение импульса (кокаин, уретан, ультрафиолетовое облучение), действуют именно на перехваты Ранвье, но не на участки между ними.
Прямые и строгие доказательства сальтаторной теории получены в работах Тасаки и его сотрудников [6, 18, 19]. Основной опыт ставился на одиночном волокне, лежащем в трех каплях раствора Рингера, разделенных двумя воздушными промежутками, расстояние между которыми равнялось приблизительно 1 мм (рис. 4.12) [3]. В первом опыте (рис. 4.12, а) в средней капле находилась только миелинизированная часть аксона, во втором (рис. 4.12,6)—в средней капле находился перехват Ранвье. Измерялся радиальный ток. Через сопротивление R проходит ток, равный il2— г23, где i2— ток, текущий в наружной цепи от капли 1 к капле 2, і23— от капли 2 к капле 3. Эта разность равна току, входящему в волокно из капли 2.
1ме 1ма
Рис. 4.12. Мембранный ток:
А—через участок аксона, расположенный между перехватами Раивье, б —через перехват Ранвье. Отклонение осциллограммы вверх соответствует выходящему току.
В первом опыте радиальный ток направлен наружу, что объясняется пассивным разрядом миелинизированного участка через перехват. Правый перехват разряжается позже левого, соответственно на осциллограмме видны два пика. Во втором опыте первая фаза тока направлена наружу, что означает пассивную деполяризацию перехвата. Во второй фазе ток направлен внутрь — перехват Ранвье находится в активном состоянии. Эти опыты однозначно подтверждают теорию (дальнейшие подробности см. в [3, 6, 18, 19]).
Мембранная теория в целом непосредственно подтверждается опытами с перфузией аксонов. Оказалось возможным выдавить аксоплазму из гигантского аксона Loligo без повреждения мембраны и заменить аксоплазму искусственными растворами (см. [3, 6, 20—22]). Перфузированные аксоны способны проводить до 105—106 импульсов в течение нескольких часов.
Потенциал покоя исчезает при равенстве наружной и внутренней концентраций калия. При замене в аксоплазме КС1 на NaCl потенциал покоя падает до нуля. В то же время потенциал покоя малочувствителен к концентрациям К+, меньшим 20 мМ (см. также § 3.6). Перфузионные опыты показывают, что потенциал покоя действительно регулируется ионами калия.
При указанной замене К. С1 на NaCl и значительном увеличении концентрации К (до 600 мМ) создается положение, обратное нормальному, и внутренняя часть волокна заряжается положительно, а не отрицательно по отношению к наружной среде. И в самом деле, при заполнении волокна, погруженного в изотонический раствор КС1, таким же раствором NaCl внутренний раствор заряжен положительно по отношению к наружному и <р составляет 50—60 мВ.
Прямые опыты с мечеными атомами показывают, что проведение импульса связано с возрастанием скорости движения калия и натрия по градиентам концентрации. В гигантском аксоне каракатицы Sepia при каждом импульсе наблюдается входящий поток Na+, равный 10,3-Ю-12 моль/см2, и выходящий поток 6,6-Ю-12 моль/см2. Чистый вход Na+ 3,7-Ю-12 моль/см2 за импульс примерно равен выходу К+. Действительно, для изменения напряжения конденсатора емкостью 1 мкФ на 120 мВ нужен заряд 0,12-Ю-6 Кл, что эквивалентно 1,3-Ю-12 моль/см2 одновалентного катиона. Таким образом, измеренный вход Na+ более чем достаточен для возникновения потенциала действия.
За один импульс в немиелинизированном аксоне через 1 мкм2 поверхности проходит около 20 000 ионов Na+. В миелинизиро — ванном аксоне за один импульс через каждый перехват Ранвье входит 6-Ю6 ионов Na+. Площадь мембраны в перехвате примерно равна 20 мкм2, следовательно, через 1 мкм2 проходит 300 000 ионов Na+. Плотность ионного тока в перехвате примерно в 10 раз больше, чем в немиелинизированных гигантских аксонах.
Мембранная теория встречается, однако, с трудностями при попытках объяснить тепловые явления в нерве. Согласно мембранной теории генерация импульса происходит за счет свободной энергии, определяемой градиентом концентрации ионов Na+. Если перенос ионов адиабатичен, то система, совершая электрическую работу, должна охлаждаться. Однако оказалось, что во время генерации импульса сначала происходит нагревание нерва, за которым следует охлаждение [23]. Аналогичное явление наблюдается при разряде электрического органа угря на внешнее сопротивление [24]. Эти тепловые явления до сих пор не объяснены. Несомненно, что мембрана аксона представляет собой диссипативную систему, и можно думать, что к рассмотрению генерации нервного импульса применима неравновесная термодинамика. Соответствующая теория еще не построена, она должна описать и теплопродукцию нерва. Подлинное объяснение этих явлений требует, однако, раскрытия их молекулярных механизмов.
В заключение приведем электрические характеристики мие- линизированного нервного волокна лягушки (табл. 4.3) [3].
Таблица 4.3
Электрические характеристики аксона
|
Диаметр волокна |
14 мкм |
|
Толщина миелиновой оболочки |
2 мкм |
|
Расстояние между перехватами Ранвье |
2 мм |
|
Площадь мембраны в перехвате Ранвье |
22 мкм2 |
|
Сопротивление на единицу длины осевого ци |
140 МОм/см |
|
Линдра |
110 Ом • см |
|
Удельное сопротивление аксоплазми |
|
|
Емкость на единицу длины миелиновой оболочки |
10—16 пФ/см |
|
Емкость на едниицу площади миелиновой обо |
0,0025—0,005 мкФ/см2 |
|
Лочки |
|
|
Диэлектрическая проницаемость миелиновой обо |
5-10 |
|
Лочки |
|
|
Удельное сопротивление миелиновой оболочки |
500—800 МОм/см |
|
Емкость перехвата Ранвье |
0,6-1,5 пФ |
|
Емкость на единицу площади перехвата Ранвье |
3—7 мкФ/см2 |
|
Сопротивление перехвата Ранвье в покое |
40—80 МОм |
|
Сопротивление, умноженное на единицу площади |
10-20 Ом-см2 |
|
Мембраны в перехвате Ранвье |
|
|
Потенциал действия |
116 мВ |
|
Потенциал покоя |
71 мВ |
|
Максимальная плотность входящего тока |
20 мА/см2 |
|
Скорость проведения |
23 м/с |
В биологии особое значение имеют автокаталитические химические системы. Достаточно указать, что авторепродукция КДеток и организмов эквивалентна автокатализу. Вернемся сначала к феноменологическому термодинамическому рассмотрению. Как мы видели, для химических процессов критерий …
Неотъемлемой особенностью биологических объектов — клеток и организмов — является их историчность, т. е. возникновение и развитие изучаемой системы в конечном интервале времени. Развитие биологической системы всегда необратимо, и в …
Самые общие соображения показывают, что перенос электрона, сдвиг электронной плотности в конденсированной ср. еде должны сопровождаться изменениями положений атомов, атомных ядер среды. Все степени свободы молекулярной системы, т. е. системы, …
Читательница журнала Л. Горбунова (деревня Цыбино, Московской области) пишет нам: «Меня интересует механизм, передачи сигналов по нервным, клеткам».
Лауреаты Нобелевской премии 1963 года (слева направо): А. Ходжкин, Э. Хаксли, Д. Экклс.
Представления ученых о механизме передачи нервного импульса претерпели в последнее время существенное изменение. До недавнего времени в науке господствовали взгляды Бернштейна.
‹
›
Мозг человека, без сомнения, высшее достижение природы. В килограмме нервной ткани заключена квинтэссенция всего человека, начиная от регуляции жизненных функций — работы сердца, легких, пищеварительного тракта, печени — и кончая его духовным миром. Здесь — наши мыслительные способности, всё наше мироощущение, память, разум, наше самосознание, наше «я». Познание механизмов работы мозга — это познание самого себя.
Велика и заманчива цель, но неимоверно сложен объект исследования. Шутка сказать, этот килограмм ткани представляет собой сложнейшую систему связи десятков миллиардов нервных клеток.
Однако первый существенный шаг к познанию работы мозга уже сделан. Может быть, он один из самых легких, но он чрезвычайно важен для всего дальнейшего.
Я имею в виду исследование механизма передачи нервных импульсов — сигналов, бегущих по нервам, как по проводам. Именно эти сигналы являются той азбукой мозга, с помощью которой органы чувств посылают в центральную нервную систему сведения-депеши о событиях во внешнем мире. Нервными импульсами зашифровывает мозг свои приказы мышцам и различным внутренним органам. Наконец, на языке этих сигналов говорят между собой отдельные нервные клетки и нервные центры.
Нервные клетки — основной элемент мозга — разнообразны по величине, по форме, но в принципе обладают единым строением. Каждая нервная клетка состоит из трех частей: из тела, длинного нервного волокна — аксона (длина его у человека от нескольких миллиметров до метра) и нескольких коротких ветвистых отростков — дендритов. Нервные клетки изолированы друг от друга оболочками. Но все же клетки взаимодействуют между собой. Происходит это в месте стыка клеток; этот стык называется «синапс». В синапсе встречаются аксон одной нервной клетки и тело или дендрит другой клетки. Причем интересно, что возбуждение может передаваться только и одном направлении: от аксона к телу или дендриту, но ни в коем случае не обратно. Синапс — это как бы кенотрон: он пропускает сигналы только в одном направлении.
В проблеме изучения механизма нервного импульса и его распространения можно выделить два основных вопроса: природа проведения нервного импульса или возбуждения в пределах одной клетки — по волокну и механизм передачи нервного импульса от клетки к клетке — через синапсы.
Какова природа сигналов, передающихся от клетки к клетка по нервным волокнам?
Этой проблемой человек интересовался уже давно, Декарт предполагал, что распространение сигнала связано с переливанием жидкости по нервам, как по трубкам. Ньютон думал, что это чисто механический процесс. Когда появилась электромагнитная теория, ученые решили, что нервный импульс аналогичен движению тока по проводнику со скоростью, близкой к скорости распространения электромагнитных колебаний. Наконец, с развитием биохимии появилась точка зрения, что движение нервного импульса — это распространение вдоль по нервному волокну особой биохимической реакции.
И всё же ни одно из этих представлений не оправдалось.
В настоящее время природа нервного импульса раскрыта: это удивительно тонкий электрохимический процесс, в основе которого лежит перемещение ионов через оболочку клетки.
Большой вклад в раскрытие этой природы внесли работы трех ученых: Алана Ходжкина, профессора биофизики Кембриджского университета; Эндрью Хаксли, профессора физиологии Лондонского университета, и Джона Экклса, профессора физиологии австралийского университета в Канберре. Им присуждена Нобелевская премия в области медицины за 1963 год,
Впервые предположение об электрохимической природе нервного импульса высказал известный немецкий физиолог Бернштейн в начале нашего столетия.
К началу двадцатого века было довольно многое известно о нервном возбуждении. Ученые уже знали, что нервное волокно можно возбудить электрическим током, причем возбуждение всегда возникает под катодом — под минусом. Было известно, что возбужденная область нерва заряжается отрицательно по отношению к невозбужденному участку. Было установлено, что нервный импульс в каждой точке длится всего 0,001—0,002 секунды, что величина возбуждения не зависит от силы раздражения, как громкость звонка в нашей квартире не зависит от того, как сильно мы нажимаем на кнопку. Наконец, ученые установили, что носителями электрического тока в живых тканях являются ионы; причем внутри клетки основной электролит — соли калия, а в тканевой жидкости — соли натрия. Внутри большинства клеток концентрация ионов калия в 30—50 раз больше, чем в крови и в межклеточной жидкости, омывающей клетки.
И вот на основании всех этих данных Бернштейн предположил, что оболочка нервных и мышечных клеток представляет собой особую полупроницаемую мембрану. Она проницаема только для ионов К+; для всех остальных ионов, в том числе и для находящихся внутри клетки отрицательно заряженных анионов, путь закрыт. Ясно, что калий по законам диффузии будет стремиться выйти из клетки, в клетке возникает избыток анионов, и по обе стороны мембраны появится разность потенциалов: снаружи — плюс (избыток катионов), внутри — минус (избыток анионов). Эта разность потенциалов получила название потенциала покоя. Таким образом, в покое, в невозбужденном состоянии внутренняя часть клетки всегда заряжена отрицательно по сравнению с наружным раствором.
Бернштейн предположил, что в момент возбуждения нервного волокна происходят структурные изменения поверхностной мембраны, ее поры как бы увеличиваются, и она становится проницаемой для всех ионов. При этом, естественно, разность потенциалов исчезает. Это и вызывает нервный сигнал.
Мембранная теория Бернштейма быстро завоевала признание и просуществовала свыше 40 лет, вплоть до середины нашего столетия.
Но уже в конце 30-х годов теория Бернштейна встретилась с непреодолимыми противоречиями. Сильный удар ей был нанесен в 1939 году тонкими экспериментами Ходжкина и Хаксли. Эти ученые впервые измерили абсолютные величины мембранного потенциала нервного волокна в покое и при возбуждении. Оказалось, что при возбуждении мембранный потенциал не просто уменьшался до нуля, а переходил через ноль на несколько десятков милливольт. То есть внутренняя часть волокна из отрицательной становилась положительной.
Но мало ниспровергнуть теорию, надо заменить ее другой: наука не терпит вакуума. И Ходжкин, Хаксли, Катц в 1949—1953 годах предлагают новую теорию. Она получает название натриевой.
Здесь читатель вправе удивиться: до сих пор о натрии не было речи. В этом все и дело. Ученые установили с помощью меченых атомов, что в передаче нервного импульса замешаны не только ионы калия и анионы, но и ионы натрия и хлора.
В организме достаточно ионов натрия и хлора, все знают, что кровь соленая на вкус. Причем натрия в межклеточной жидкости в 5—10 раз больше, чем внутри нервного волокна.
Что же это может означать? Ученые предположили, что при возбуждении в первый момент резко увеличивается проницаемость мембраны только для натрия. Проницаемость становится в десятки раз больше, чем для ионов калия. А так как натрия снаружи в 5—10 рез больше, чем внутри, то он будет стремиться войти в нервное волокно. И тогда внутренняя часть волокна станет положительной.
А через какое-то время — после возбуждения — равновесие восстанавливается: мембрана начинает пропускать и ионы калия. И они выходят наружу. Тем самым они компенсируют тот положительный заряд, который был внесен внутрь волокна ионами натрия.
Совсем нелегко было прийти к таким представлениям. И вот почему: диаметр иона натрия в растворе раза в полтора больше диаметра ионов калия и хлора. И совершенно непонятно, каким образом больший по размеру ион проходит там, где не может пройти меньший.
Нужно было решительно изменить взгляд на механизм перехода ионов через мембраны. Ясно, что только рассуждениями о порах в мембране здесь не обойтись. И тогда была высказана идея, что ионы могут пересекать мембрану совершенно другим способом, с помощью тайных до поры до времени союзников — особых органических молекул-переносчиков, спрятанных в самой мембране. С помощью такой молекулы ионы могут пересекать мембрану в любом месте, а не только через поры. Причем эти
молекулы-такси хорошо различают своих пассажиров, они не путают ионы натрия с ионами калия.
Тогда общая картина распространения нервного импульса будет иметь следующий вид. В покое молекулы-переносчики, заряженные отрицательно, мембранным потенциалом прижаты к наружной границе мембраны. Поэтому проницаемость для натрия очень мала: в 10—20 раз меньше, чем для ионов калия. Калий может пересекать мембрану через поры. При приближении волны возбуждения уменьшается давление электрического поля на молекулы-переносчики; они сбрасывают свои электростатические «оковы» и начинают переносить ионы натрия внутрь клетки. Это еще больше уменьшает мембранный потенциал. Идет как бы цепной процесс перезарядки мембраны. И этот процесс непрерывно распространяется вдоль нервного волокна.
Интересно, что нервные волокна тратят на свою основную работу — проведение нервных импульсов — всего около 15 минут в сутки. Однако готовы к этому волокна в любую секунду: все элементы нервного волокна работают без перерыва — 24 часа в сутки. Нервные волокна в этом смысле подобны самолетам-перехватчикам, у которых непрерывно работают моторы для мгновенного вылета, однако сам вылет может состояться лишь раз в несколько месяцев.
Мы познакомились сейчас с первой половиной таинственного акта прохождения нервного импульса — вдоль одного волокна. А как же передается возбуждение от клетки к клетке, через места стыков — синапсы. Этот вопрос был исследован в блестящих опытах третьего нобелевского лауреата, Джона Экклса.
Возбуждение не может непосредственно перейти с нервных окончаний одной клетки на тело или дендриты другой клетки. Практически весь ток вытекает через синаптическую щель в наружную жидкость, и в соседнюю клетку через синапс попадает ничтожная его доля, неспособная вызвать возбуждение. Таким образом, в области синапсов электрическая непрерывность в распространении нервного импульса нарушается. Здесь, на стыке двух клеток, в силу вступает совершенно другой механизм.
Когда возбуждение подходит к окончанию клетки, к месту синапса, в межклеточную жидкость выделяются физиологически активные вещества — медиаторы, или посредники. Они становятся связующим звеном в передаче информации от клетки к клетке. Медиатор химически взаимодействует со второй нервной клеткой, изменяет ионную проницаемость ее мембраны — как бы пробивает брешь, в которую устремляются многие ионы, в том числе и ионы натрия.
Итак, благодаря работам Ходжкина, Хаксли и Экклса важнейшие состояния нервной клетки — возбуждение и торможение — можно описать в терминах ионных процессов, в терминах структурно-химических перестроек поверхностных мембран. На основании этих работ уже можно делать предположения о возможных механизмах кратковременной и долговременной памяти, о пластических свойствах нервной ткани. Однако это разговор о механизмах в пределах одной или нескольких клеток. Это лишь, азбука мозга. По-видимому, следующий этап, возможно, гораздо более трудный, — вскрытие законов, по которым строится координирующая деятельность тысяч нервных клеток, распознание языка, на котором говорят между собой нервные центры.
Мы сейчас в познании работы мозга находимся на уровне ребенка, который узнал буквы алфавита, но не умеет связывать их в слова. Однако недалеко время, когда ученые с помощью кода — элементарных биохимических актов, происходящих в нервной клетке, прочтут увлекательнейший диалог между нервными центрами мозга.
Детальное описание иллюстраций
Представления ученых о механизме передачи нервного импульса претерпели в последнее время существенное изменение. До недавнего времени в науке господствовали взгляды Бернштейна. По его мнению, в состоянии покоя (1) нервное волокно заряжено положительно снаружи и отрицательно внутри. Это объяснялось тем, что сквозь поры в стенке волокна могут проходить только положительно заряженные ионы калия (К+); большие по размерам отрицательно наряженные анионы (А–) вынуждены оставаться внутри и создавать избыток отрицательных зарядов. Возбуждение (3) по Бернштейну сводится к исчезновению разности потенциалов, которое вызывается тем, что размер пор увеличивается, анионы выходят наружу и выравнивают ионный баланс: количество положительных ионов становится равным количеству отрицательных. Работа лауреатов Нобелевской премии 1963 года А. Ходжкпна, Э. Хаксли и Д. Экклса изменила наши прежние представления. Доказано, что в нервном возбуждении участвуют также положительные ионы натрия (Na+), отрицательные ноны хлора (Сl–) и отрицательно заряженные молекулы-переносчики. Покоящееся состояние (3) образуется в принципе так же, как и считалось раньше: избыток положительных ионов — снаружи нервного волокна, избыток отрицательных — внутри. Однако установлено, что при возбуждении (4) происходит не выравнивание зарядов, а перезарядка: снаружи образуется избыток отрицательных ионов, а внутри — избыток положительных. Объясняется это тем, что при возбуждении молекулы-переносчики начинают перевозить сквозь стенку положительные ионы натрия.
Таким образом, нервный импульс (5) — это перемещающаяся вдоль волокна перезарядка двойного электрического слоя. А от клетки к клетке возбуждение передается своеобразным химическим «тараном» (6) — молекулой ацетилхолина, которая помогает ионам прорываться сквозь стенку соседнего нервного волокна.