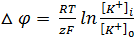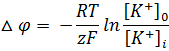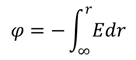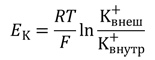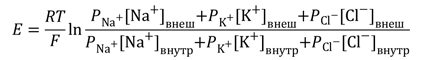Статья на конкурс «био/мол/текст»: Тайна того, каким образом «работает» человеческий мозг, мучила философов и естествоиспытателей с древнейших времен. Современные ученые постепенно подходят к ее разгадке, приближая тот час, когда мы сможем полностью понять, как и с помощью чего мы на самом деле думаем. Именно сейчас развитие вычислительной техники и последние достижения в нейробиологии сделали реальным то, что раньше казалось недостижимым. Появились компьютеры, способные понимать речь, ориентироваться в пространстве и даже писать научные статьи. Работа таких машин частично основана на принципах работы головного мозга. Каким образом они работают, что такое мышление и где оно происходит? Обо всем этом мы попытаемся рассказать.
Клетки-деревья
Общеизвестно, что наш мозг состоит из нейронов (по крайней мере, именно они отвечают за мыслительный процесс). Морфологически эти клетки похожи на деревья с корнями-дендритами и стволом-аксоном. На дендритах суммируются электрические сигналы, поступающие от других нейронов, и в зависимости от этого нейрон «принимает решение», формировать ли ему потенциал действия (т.е. нервный импульс). Потенциалом действия называется волна токов ионов натрия и калия, которая быстро проходит через мембрану и распространяется без затухания по аксону к другим нейронам. Именно это свойство позволяет нейронам передавать сигнал без потери информации на большие расстояния. Так, потенциал действия, сформированный в коре головного мозга, может достичь нейронов в позвоночнике, а затем в руке, за считанные миллисекунды. В окончании аксона находятся синапсы, из которых после прохождения потенциала действия высвобождаются особые вещества — нейромедиаторы. Именно они передают сигнал к следующему нейрону, и так далее, по цепочке [14].
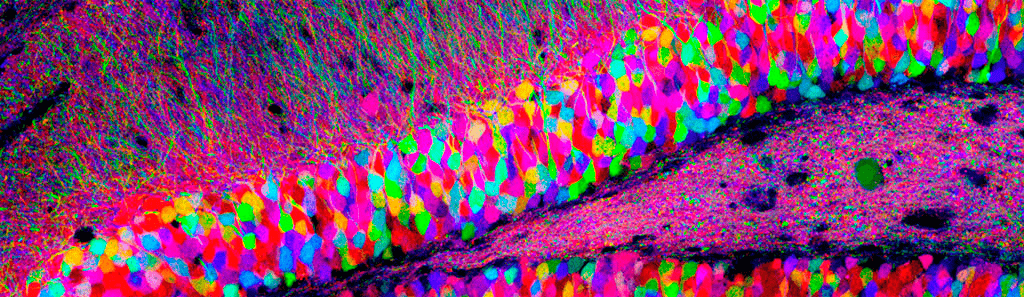
Однако один нейрон сам по себе не способен обеспечить сложное поведение, характерное для животных и тем более самого умного из них — человека. По оценкам ученых, в человеческом мозге около 100 миллиардов нервных клеток, которые соединены в сложнейшую сеть со 100 триллионами синаптических контактов между ними (рис. 1). При виде таких чисел в пору отчаяться и бросить попытки разобраться в том, как функционирует этот сложнейший природный объект. К счастью, ученые — люди не робкого десятка и продолжают упорно двигаться вперед.
Рисунок 1. Множество нейронов в срезе гиппокампа крысы. Клетки помечены различными флуоресцентными белками с помощью технологии Brainbow.
Моделирование вместо опыта
Один из главных вопросов изучения биологических нейронных сетей — каким образом при соединении нейронов относительно простое поведение отдельной единицы трансформируется в сложное поведение сети в целом. Однако полностью разобраться в этом мешают ограниченные возможности эксперимента: в настоящей нейронной сети практически невозможно измерить все сигналы со всех 100 миллиардов нейронов и отследить все процессы, происходящие в ней. Тут-то на помощь ученым и приходит компьютерное моделирование. Математические модели всегда помогали исследователям отвечать на подобного рода сложные вопросы. А после появления вычислительных машин возможности в этой области постоянно расширяются.
Одним из последних достижений в этой области является проект Blue Brain, возглавляемый Генри Маркромом [2], [3]. В рамках этой инициативы ученые пытаются воспроизвести поведение одной колонки кортекса, состоящей из сотен тысяч клеток, которые моделируются с максимальной степенью детализации. Колонки в новой коре являются ее важнейшим функциональным элементом, на уровне которых, по мнению многих ученых, происходят вычисления, которые являются основой высших психических функций, включая мышление. Именно поэтому детальное изучение этих структур является крайне важным.
Первая модель работы нейрона была создана еще в 1907 году французским физиологом Льюисом Лаписиком [4] — задолго до того, как был изучен механизм формирования нейроном потенциала действия [5]. Модель была очень простой: согласно ей нейрон как конденсатор накапливает напряжение до определенного порогового значения, после чего генерирует потенциал действия. Стоит отметить, что концепция работы нейрона как порогового интегратора почти не изменилась после публикации работы Льюиса Лаписика, но было выяснено множество важнейших деталей.
Нобелевская премия за кальмара
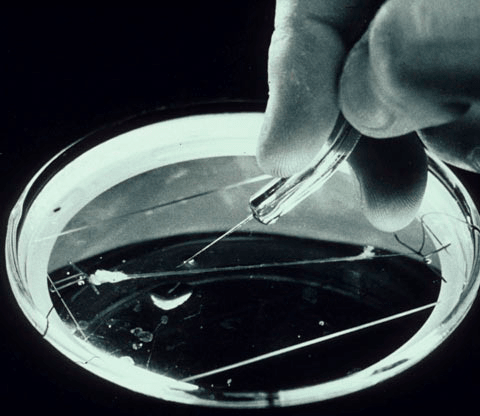
Однако наибольшее распространение получила модель Ходжкина-Хаксли, построенная на основе экспериментов с гигантским аксоном кальмара [5] (рис. 2). Тут мы позволим себе небольшое отступление, чтобы рассказать о том, почему нейроны именно этого живого организма оказались такими удобными для исследований.
Рисунок 2. Гигантский аксон кальмара в чашке Петри. Может быть, на первый взгляд он и не кажется таким уж большим, но по сравнению с аксонами нейронов головного мозга, которые невозможно увидеть невооруженным глазом, он просто огромен.
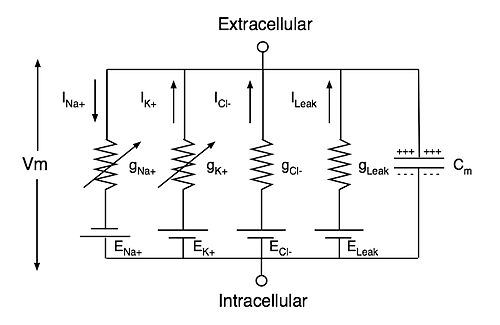
Модель Ходжкина-Хаксли (рис. 3) описывает поведение нейрона, представляя его в виде достаточно простой электрической цепи, где мембрана является конденсатором, ионные каналы — проводимостями (величина, обратная сопротивлению, измеряемая в Сименсах), градиенты ионов натрия, калия и хлора на мембране (то есть, разница между концентрацией ионов внутри и снаружи) — источниками напряжения. При этом активируемые каналы для ионов калия, натрия и хлора описываются нелинейными проводимостями gK, gNa и gCl, а каналы утечки, которые открыты всегда, — постоянной проводимостью gL (от англ. leak — «утечка»). Полученная модель работы нейрона оказалась применима не только для кальмара, но и для млекопитающих, в том числе для человека. Поэтому авторы исследования — британцы Алан Ходжкин и Эндрю Хаксли — получили в 1963 году Нобелевскую премию по физиологии и медицине.
Рисунок 3. Схема электрической цепи модели Ходжкина—Хаксли гигантского аксона кальмара, за которую была получена Нобелевская премия в 1963 году. Cm — емкость мембраны нейрона, ENa+, EK+, ECl− и ELeak — потенциалы реверсии токов натрия, калия, хлора и утечки, а gNa+, gK+, gCl− и gLeak — соответствующие проводимости ионных каналов. Vm — трансмембранный потенциал.
От подневольного труда к искусственному интеллекту
Первые упоминания об искусственных разумных существах можно обнаружить еще в греческой мифологии. Согласно легендам, Гефест по просьбе Зевса создал бронзового гиганта Талоса (рис. 4), который охранял Елену на острове Крит. В средние века появились предания о гомункулусах и Големе — созданных человеком разумных существах.
Рисунок 4. Бронзовый гигант Талос — пожалуй, первый робот в мифологическом фольклоре (кадр из фильма «Ясон и аргонавты», 1965 год).
С конца XIX века искусственные живые существа стали неотъемлемой частью культуры, начиная с «Франкенштейна» Мэри Шелли и пьесы Карела Чапека (рис. 5) «R.U.R.» («Россумские Универсальные Роботы»). Кстати, именно в этой пьесе Чапек впервые использовал придуманное с братом Йозефом слово «робот» (по-чешски robota означает «подневольный труд»).
Рисунок 5. Монстр Франкенштейна (а), Карел Чапек (б) и Алан Тьюринг (в)
До середины XX века разговоры о разумных машинах носили чисто теоретический характер, но уже в 1956 году разработка искусственного интеллекта приобрела статус научной дисциплины. Произошло это благодаря появлению электронных вычислительных машин, а также прорыву в нейробиологии. Наука о мозге помогла понять, что нервная система функционирует благодаря обмену нейронов электрическими импульсами, а вычислительные машины позволили описывать эти процессы с помощью программ.
Вскоре стало понятно, что создание искусственного интеллекта требует как минимум понимания значений слов «искусственный» и «интеллект». Алан Тьюринг нашел элегантный выход: вместо того, чтобы пытаться сформулировать, что же такое «интеллект», он предложил определять, есть он у машины или нет, способом, который получил название «Тест Тьюринга» [8].
Идея теста заключается в том, что экзаменатор общается в текстовом режиме с двумя испытуемыми, один из которых — машина, а другой — человек. Цель экзаменатора — определить, кто есть кто. Тест считается успешным, если машине удается обмануть эксперта. Несмотря на кажущуюся простоту, ни одной программе до сих пор не удалось его пройти.
Хотя настоящего думающего робота создать пока не удалось, различные современные подходы позволяют непрерывно расширять область задач, которые способны решать компьютеры, даже в тех сферах, которые всегда считались доступными лишь людям — например, работа с символами и написание научных статей.
Символьный подход
Первые достижения в создании искусственного интеллекта были связаны с использованием возможностей математической логики. Уже в 1956 году была создана программа с говорящим названием Logic Theorist, которая смогла доказать 38 из 52 теорем, описанных в книге Бертрана Рассела и Альберта Уайтхэда «Основания математики», причем для некоторых из них она смогла найти новые, более простые доказательства. В это же время были созданы программы, способные правдоподобно имитировать переписку с живым человеком (правда, недостаточно хорошо для прохождения теста Тьюринга), и многие другие.
Все эти программы основывались на предположении, что интеллект заключается в осуществлении операций над различными символами по законам логики. На этом принципе были основаны первые коммерчески успешные программы искусственного интеллекта — экспертные системы. Они позволяли частично заменить работу реального эксперта — например, оценить риск организации при предоставлении кредита клиенту. Такая программа работает с базой знаний (набором фактов и правил, формализующих работу экспертов в данной области) по определенным логическим законам. Но далеко не все проблемы могут быть решены в рамках строгой логики, поэтому зачастую в таких программах используется нечеткая или вероятностная логика. Ее особенностью является то, что вместо 0 и 1 — «да» или «нет» — в ней используются все значения между 0 и 1, — например, 0.2 или 0.7: «скорее да», «скорее нет».
Весьма ограниченный успех логического подхода продемонстрировал одну важную вещь: интеллект — это не только способность логически мыслить. Поэтому для решения сложно формализуемых задач (например, распознавания образов) пришлось отказаться от красоты и стройности формальной логики.
Нейронные сети
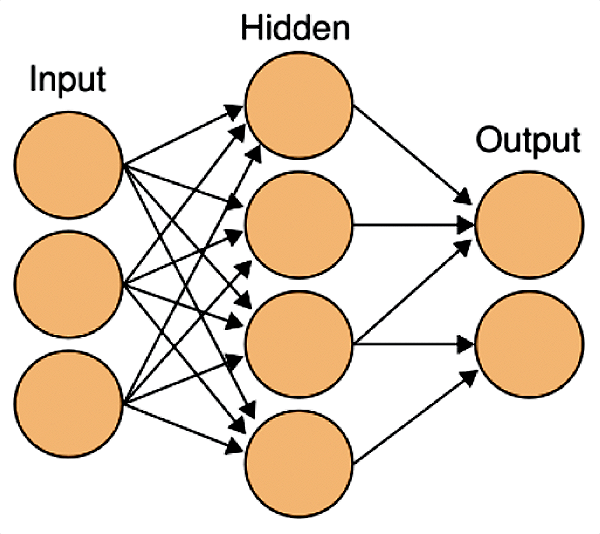
Разработчики искусственных нейронных сетей были вдохновлены работой настоящих нейронов в мозге. Только вместо реальных клеток в сетях используются уравнения, моделирующие их работу (рис. 6).
Рисунок 6. Схема искусственной нейронной сети. На входные нейроны подается стимул, затем он обрабатывается в нейронах скрытого слоя (таких слоев может быть несколько) и результаты предоставляются на выходных нейронах.
Первыми в нейронной сети получают информацию входные нейроны. Именно они получают сигналы от внешнего стимула, который может быть всем, чем угодно: изображения, отдельные звуки и даже человеческая речь. Но для того, чтобы передать полученную информацию, входным нейронам необходимо перевести сигнал стимула на их «язык». Это уже работа другого вида клеток — рецепторов, которые преобразуют информацию о стимуле в нервные импульсы. Биологическим примером таких рецепторов являются палочки и колбочки в сетчатке глаза. Подобные рецепторы есть и в искусственных нейронных сетях: при обработке изображений это фотоэлементы, звуков — микрофоны.
Конечным этапом обработки информации в нейросети являются выходные нейроны, активность которых интерпретируется как результат: преобразованный входными нейронами сигнал от рецепторов попадает в сеть, затем переходит к следующим нейронам и преобразуется за счет взаимодействий между ними через синапсы. Например, если сеть занимается распознаванием букв алфавита, то после успешного обучения на выходе будут активны нейроны, соответствующие этим буквам.
Для того чтобы сеть могла правильным образом классифицировать входной сигнал, связи между нейронами должны быть правильно подобраны. В 1943 году нейрофизиолог Фрэнк Розенблатт создал модель, которая называется перцептрон (от лат. perceptio — восприятие) [9]. Она работает следующим образом: в начале обучения связи между нейронами являются одинаковыми, затем сети предъявляются различные буквы по нескольку раз, и если буквы классифицируются на выходных нейронах правильно, то связи, приводящие к правильной классификации, усиливаются, а если нет, то ослабляются [13]. Таким образом, после предъявления большого количества стимулов сеть учится их распознавать. При этом, чем больше букв необходимо выучить сети, тем бóльшим должно быть количество нейронов. В качестве результата сеть может распознавать буквы, которые лишь отдаленно напоминают те, которые использовались при обучении. Более того, буквы могут быть повреждены или написаны другим шрифтом, но сеть все равно будет способна их распознать!
На самом деле многие программы в компьютере используют такой подход: например, программа Fine Reader, которая распознает изображение и переводит его в текст, использует в своей работе нейросети. По такому же принципу работает распознавание рукописного ввода на смартфонах и планшетах.
Генетические алгоритмы
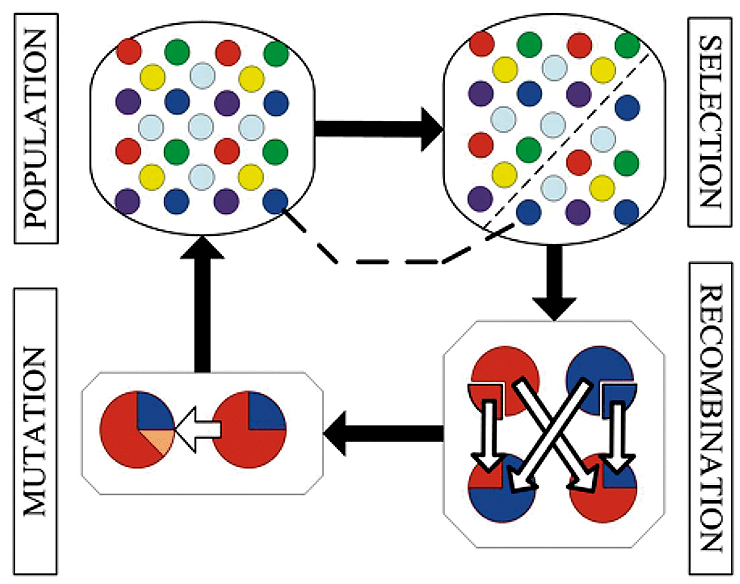
Еще одним подходом в программировании, вдохновленным биологией, являются эволюционные алгоритмы (рис. 7). В рамках этого подхода занимаются моделированием процесса биологической эволюции, только вместо живых организмов используются программы [10]. На первый взгляд у алгоритмов и животных мало общего, но, если присмотреться, можно увидеть похожее.
Под алгоритмом в общем случае подразумевают последовательный набор действий, который приводит к желаемому результату за конечное число ходов. Например, чтобы прийти в университет, необходимо: 1) проснуться, 2) умыться, 3) одеться, 4) позавтракать, 5) собраться, 6) пойти. Конечно, детали алгоритмов могут быть разными: например, кому-то не нужно собирать вещи, потому что они были собраны вчера. Но важным является то, что в любом случае выполняется последовательность действий, приводящая к нужному результату.
Рисунок 7. Принцип работы генетических алгоритмов. В начале рассматривается популяция алгоритмов, которые выполняют определенную задачу. Затем вводится правило, в соответствии с которым селективно выбираются только те из них, которые способны выполнить задачу лучше других. Затем алгоритмы обмениваются отдельными частями, чтобы получить новые на этапе рекомбинации. После этого на этапе мутаций в алгоритмы вносятся небольшие случайные изменения, чтобы увеличитель их разнообразие. Затем процедура выбора алгоритмов повторяется много раз, и на завершающем этапе остаются только те алгоритмы, которые выполняют задачу наилучшим образом.
Для того, чтобы алгоритмы могли эволюционировать, их разделяют на отдельные части, которые можно менять между собой. Например:
- проснуться—умыться—одеться—позавтракать—собраться—пойти;
- проснуться—собраться—одеться—позавтракать—умыться—пойти и т.д.
Также необходимо отказаться от невозможных вариантов: к примеру, алгоритм «одеться→позавтракать→проснуться→…» невозможен по понятным причинам.
После этого оценивают работу каждого алгоритма и выбирают наилучший. К примеру, в случае с походом в университет лучшим алгоритмом будет самый быстрый. Затем производится обмен их частей между собой и внесение мутаций (добавление и/или видоизменение действий), после чего появляются новые алгоритмы, которые снова оцениваются. Таким образом, через несколько поколений отбираются именно те, которые справляются с задачей лучше всего. Такие алгоритмы часто используют в биоинформатике, инженерном деле и многих других приложениях, чтобы находить наилучшие решения.
Во что играть против робота?
В 1994 году программа Chinook стала чемпионом мира по шашкам, впоследствии защитив этот титул в 1996 году. В 2007 году команда разработчиков Chinook закончила полный анализ всех возможных комбинаций этой игры, и Chinook стала непобедимой. На сегодняшний день шашки — самая сложная полностью проанализированная игра; в ней имеется 5×1020 возможных комбинаций фигур на игровом поле.
Но не стоит отчаиваться, потому что все еще существуют игры, в которых человек легко побеждает компьютер [11]. Например, к ним относится китайская игра го (рис. 8). Выглядит она достаточно просто: поле состоит из сетки 19×19 и двух видов шашек: черных и белых. Целью игры является захват территории — это чем-то напоминает игру в точки. Однако, несмотря на простоту правил, ней существует огромное количество возможных комбинаций. Если в шахматах после четвертого хода от начала партии может возникнуть несколько сотен тысяч различных вариантов, то в го их число превышает шестнадцать миллиардов. Так что пока человек все еще непобедимый соперник в некоторых играх против компьютера.
Рисунок 8. Игра го считается одной из наиболее сложных логических игр для освоения компьютером. Уже средние игроки легко побеждают любые существующие на данный момент компьютерные программы.
Заменят ли роботы ученых?
Казалось бы, кому, как не ученым, меньше всего стоит бояться того, что машины смогут конкурировать с ними? Не тут-то было: программисты из Массачусетского технологического института создали программу под названием SCIgen, способную «писать» тексты, посвященные разработке новых компьютерных алгоритмов, с иллюстрациями, графиками, ссылками и всеми остальными необходимыми атрибутами [12]! Правда, эти тексты похожи на научные статьи лишь по форме, а их осмысленность стремится к нулю.
Авторы создали эту программу для того, чтобы вывести на чистую воду конференции, которые публикуют присылаемые на них тезисы не глядя, и им это удалось. Тексты, сгенерированные программой, были приняты к публикации в сборниках тезисов сразу нескольких конференций. Группа российских ученых решила проверить, насколько тщательно подходят к отбору статей в отечественных журналах, и перевела текст, сгенерированный SCIgen, на русский язык. В итоге «статья» под названием «Корчеватель: Алгоритм типичной унификации точек доступа и избыточности» была опубликована в «Журнале научных публикаций аспирантов и докторантов»!
Разумные роботы уже рядом
Итак, полным ходом идет работа над созданием искусственного интеллекта — программ, обладающих, хотя бы частично, свойствами человеческого интеллекта. Пока что лучше всего ученым удается решение конкретных специализированных задач, таких как распознавание образов, автоматизированное написание финансовых отчетов или описание итогов спортивных игр на основе статистических данных о ходе игры.
Однако создание так называемого «сильного» искусственного интеллекта, то есть полноценного искусственного сознания, до сих пор представляется трудно достижимой целью. Тем не менее попытки его создания чрезвычайно полезны, так как позволяют лучше понять, что такое человеческий разум. Сегодня основная работа направлена на создание алгоритмов, позволяющих компьютерам осуществлять логические размышления, собирать, систематизировать и оперировать знаниями об окружающем мире, ставить цели и искать оптимальные пути их достижения, обучаться, распознавать речь и многое другое. «Сильный» искусственный интеллект должен объединять все эти алгоритмы и осуществлять взаимодействие между ними. При этом современные тенденции развития в этой области свидетельствуют о том, что, если «сильный» искусственный интеллект будет создан, большую роль в его создании будут играть нейронные сети, а значит, мы вряд ли будем знать в точности, как он работает. Стоит также отметить любопытное явление: многие успехи в развитии искусственного интеллекта, которые казались невозможными ранее, после их достижения не воспринимаются как «О, это же действительно искусственный разум!» Так что вполне возможно, что мы просто не заметим появление разумных роботов.
Статья написана в соавторстве с Антоном Сабанцевым. Частично материалы статьи были опубликованы в журнале «Я — Леонардо» (лето—осень 2013).
- Jean Livet, Tamily A. Weissman, Hyuno Kang, Ryan W. Draft, Ju Lu, et. al.. (2007). Transgenic strategies for combinatorial expression of fluorescent proteins in the nervous system. Nature. 450, 56-62;
- Henry Markram. (2006). The Blue Brain Project. Nat Rev Neurosci. 7, 153-160;
- Blue Brain Project: как все связано?;
- Nicolas Brunel, Mark C. W. van Rossum. (2007). Lapicque’s 1907 paper: from frogs to integrate-and-fire. Biol Cybern. 97, 337-339;
- A. L. Hodgkin, A. F. Huxley. (1952). A quantitative description of membrane current and its application to conduction and excitation in nerve. The Journal of Physiology. 117, 500-544;
- О чем не знал Гальвани: пространственная структура натриевого канала;
- Формирование мембранного потенциала покоя;
- Alan M. Turing. (2009). Computing Machinery and Intelligence. Parsing the Turing Test. 23-65;
- F. Rosenblatt. (1958). The perceptron: A probabilistic model for information storage and organization in the brain.. Psychological Review. 65, 386-408;
- Barricelli N.A. (1957). Symbiogenetic evolution processes realized by artificial methods. Methodos. 9, 143–182;
- Johnson G. (1997). To test a powerful computer, play an ancient game. The New York Times;
- Cyril Labbé, Dominique Labbé. (2013). Duplicate and fake publications in the scientific literature: how many SCIgen papers in computer science?. Scientometrics. 94, 379-396;
- Hebb D.O. The organization of behavior: A neuropsychological theory. Psychology Press, 2002;
- Kandel E.R. et al. Principles of neural science. NY: McGraw-Hill, 2000.
Все живые клетки при действии различных
раздражителей (химических, механических,
температурных и пр.) способны переходить
в возбужденное состояние. Опыт показывает,
что возбужденный участок становится
электроотрицательным по отношению к
покоящемуся, что является показателем
перераспределения ионных потоков в
возбужденном участке. Реверсия потенциала
при возбуждении кратковременна, и после
окончания возбуждения через некоторое
время вновь восстанавливается исходный
потенциал покоя. Общее изменение разности
потенциалов на мембране, происходящее
при возбуждении клеток, называется
потенциалом действия. На рис. 11.17
представлен потенциал действия
гигантского аксона кальмара, обозначены
отдельные стадии изменения потенциала.
В частности, для клетки характерен так
называемый запаздывающий потенциал,
когда в течение некоторого времени на
мембране существует даже меньший
потенциал, чем потенциал покоя.
Было показано, что возбуждение связано
с увеличением электропроводности
клеточной мембраны. При этом временная
зависимость электропроводимости
повторяла форму потенциала действия.
Чтобы решить вопрос, для каких ионов
изменяется проницаемость м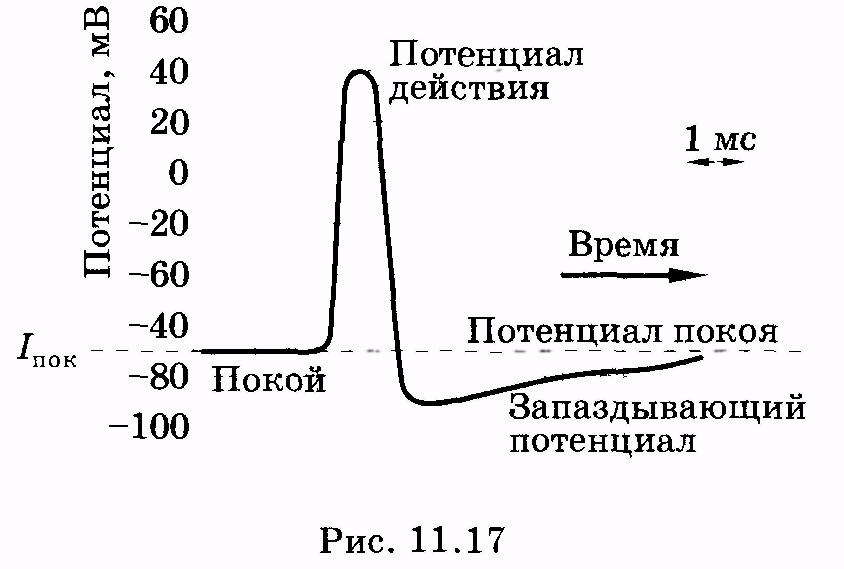
следует обратить внимание, что потенциал
действия приводит к кратковременному
возрастанию потенциала внутри клетки
(см. рис. 11.17). Отрицательный относительно
внешней среды потенциал становится
положительным. Если по уравнению Нернста
(11.38) вычислить равновесные потенциалы
на мембране аксона кальмара, то получим
соответственно для ионов К+, Na+ и Сl—величины -90, +46 и -29 мВ. Так как при
изменении проницаемости мембраны для
какого-либо иона этот ион будет проникать
через нее, стремясь создать равновесное
состояние, то числовые данные показывают,
что внутрь клетки проникают ионы Na+,
создавая там положительный потенциал.
Следовательно, при возбуждении клетки
в начальный период увеличивается
проницаемость мембран именно для ионов
натрия. «Натриевая теория» возникновения
потенциала действия была предложена,
разработана и экспериментально
подтверждена А. Ходжкином и А. Хаксли,
за что в 1963 г. они были удостоены
Нобелевской премии.
Измерить проницаемость мембран для
какого-либо иона (иначе говоря,
электропроводимость или сопротивление
мембраны для этого иона) можно, если на
основании закона Ома найти отношение
тока к напряжению, или наоборот.
Практическая реализация такой задачи
осложняется тем, что проницаемость
(электрическое сопротивление) мембраны
при возбуждении изменяется со временем.
Это приводит к перераспределению
электрического напряжения в цепи, и
разность потенциалов на мембране
изменяется. Ходжкин, Хаксли и Катц смогли
создать опыт с фиксацией определенного
значения разности потенциала на мембране.
Это позволило им провести измерение
ионных токов и, следовательно, проницаемости
(сопротивления) мембран для ионов.
Оказалось, что отношение проницаемостей
мембраны для ионов натрия и калия
практически повторяет форму потенциала
действия. Кроме того, были получены
кривые временной зависимости ионных
токов через мембрану (рис. 11.18). На этом
рисунке кривая1соответствует
временной зависимости суммарного
ионного тока через мембрану гигантского
аксона кальмара, полученного при
изменении потенциала на мембране до
+56 мВ (потенциал покоя равен60
мВ). Вначале направление тока отрицательно,
что соответствует прохождению
положительных ионов через мембрану
клетки. Было установлено, что ток этот
обусловлен прохождением ионов натрия
внутрь клетки, где концентрация их
значительно меньше, чем снаружи.
Естественно, что при таком нарушении
равновесия ионы калия начнут перемещаться
наружу, где их концентрация существенно
меньше. Для того чтобы выяснить, какая
часть тока «натриевая», а какая «калиевая»,
можно провести то же возбуждение, но в
искусственных условиях, когда в среде,
окружающей аксон, нет натрия. В этом
случае (см. кривую 2) ток обусловливается
только выходом ионов калия наружу из
клетки. Разница значений тока для двух
кривых показана на кривой3: кривая3есть разность кривых1и2.
Она дает зависимость от времени ионного
тока натрия. На этой кривой частьасоответствует открыванию натриевых
каналов, аб— их закрытию
(инактивации).
В целом
последовательность событий, происходящих
на клеточной мембране при возбуждении,
выглядит следующим образом. При
возбуждении в мембране открываются
каналы для ионов натрия (проницаемость
мембраны возрастает более чем в 5000 раз).
В результате отрицательный заряд с
внутренней стороны мембраны становится
положительным, что соответствует пику
мембранного потенциала (фаза деполяризации
мембраны). Затем поступление натрия из
внешней среды прекращается. В это время
натриевые каналы закрываются, но
открываются калиевые. Калий проходит
в соответствии с градиентом концентрации
из клетки до тех пор, пока не восстановится
первоначальный отрицательный заряд на
мембране и мембранный потенциал не
достигнет своего первоначального
значения (фаза реполяризации). На самом
деле выход ионов калия из клетки
продолжается дольше, чем это требуется
для восстановления потенциала покоя.
В результате за пиком потенциала действия
следует небольшой минимум (запаздывающий
потенциал).
Ионные
каналы имеют белковое происхождение
(см. рис. 11.3 и 11.13). Они селективно
(выборочно) пропускают ионы разного
вида. Канал может быть «закрыт»
(блокирован) молекулами ядов, его
пропускная способность зависит от
действия некоторых лекарственных
средств. Поэтому теория ионных каналов
в мембранах является важной частью
молекулярной фармакологии.
Механизм распространения потенциала
действия в деталях рассматривается в
курсе нормальной физиологии. Мы же
рассмотрим лишь некоторые основные
положения. Распространение потенциала
действия вдоль нервного волокна (аксона)
обусловлено возникновением так называемыхлокальных токов, образующихся
между возбужденным и невозбужденным
участками клетки. На рис. 11.19 схематично
указаны отдельные стадии возникновения
и распространения потенциала действия.
В состоянии покоя (рис. 11.19, а) внешняя
поверхность клеточной мембраны имеет
положительный потенциал, а внутренняя
— отрицательный. В момент возбуждения
полярность мембраны меняется на
противоположную (рис. 11.19,б). В
результате этого между возбужденным и
невозбужденным участками мембраны
возникает разность потенциалов. Наличие
разности потенциалов и приводит к
появлению между этими участкамилокальных
токов. На поверхности клетки локальный
ток течет от невозбужденного участка
к возбужденному; внутри клетки он течет
в обратном направлении (рис. 11.19, в).
Локальный ток, как и любой электрический
ток, раздражает соседние невозбужденные
участки и вызывает увеличение проницаемости
мембраны. Это приводит к возникновению
потенциалов действия в соседних участках.
В то же время в ранее возбужденном
участке происходят восстановительные
процессы реполяризации. Вновь возбужденный
участок в свою очередь становится
электроотрицательным и возникающий
локальный ток раздражает следующий
за ним участок. Этот процесс многократно
повторяется и обусловливает распространение
импульсов возбуждения по всей длине
клетки в обоих направлениях (рис. 11.19,г). В нервной системе импульсы
проходят лишь в определенном
направлении из-за наличия синапсов,
обладающих односторонней проводимостью.
По
электрическим свойствам аксон напоминает
кабель с проводящей сердцевиной и
изолирующей оболочкой. Однако для того
чтобы в кабеле не было значительных
потерь энергии при протекании
тока, сопротивление его должно быть
малым, а сопротивление
изоляции — очень большим. В аксоне
проводящим веществом
служит аксоплазма, т. е. раствор
электролита, удельноесопротивление
которого в миллионыраз
больше, чем у меди или алюминия,
из которых изготавливают обычные
кабели. Удельное сопротивление биомембран
достаточно велико, но вследствие их
малой толщины сопротивление изоляции
«аксонного кабеля» в сотни тысяч раз
меньше, чем у технического кабеля. По
этой причине однородное н
волокно не может проводить электрический
сигнал на далекое расстояние, интенсивность
сигнала быстро затухает. Расчеты
показывают, что напряжение на мембране
волокна будет экспоненциально уменьшаться
по мере удаления от места возбуждения
(рис. 11.20). Если величина потенциала
действия в месте возбуждения была равна mах,
то на расстоянии l
от этого места потенциал на мембране
будет равен:
(11.40)
где
—
постоянная
длины нервного
волокна, которая определяет степень
затухания сигнала в аксоне по
экспоненциальному закону. Эту величину
можно рассчитать по следующей приближеннойформуле:
(11.41)
где
d
— диаметр
волокна, R
— поверхностное
сопротивление мембраны
в Ом • м2
(т. е. сопротивление 1 м2
ее поверхности) и
— удельное сопротивление аксоплазмы
в Ом • м.
Расчеты,
проведенные для аксона кальмара,
показывают, что на
конце аксона величина сигнала должна
быть ничтожно малой. Однако
существование локальных токов приводит
к тому, что возбуждение
передается по нервному волокну без
затухания. Это объясняется тем, что
локальные токи лишь деполяризуют
мембрану до
критического уровня, а потенциалы
действия в каждом участке
мембраны поддерживаются независимыми
ионными потоками, перпендикулярными
к направлению распространения возбуждения.
Из
(11.40) видно, что с увеличением
степень затухания сигнала
уменьшается. Было показано, что при этом
возрастает скорость проведения импульса,
а это очень важно для жизнедеятельности
любого организма. Величины
и
примерно одинаковы
для всех животных
клеток, и поэтому увеличения постоянной
длины
можно добиться путем увеличения диаметра
d
аксона. Именно
поэтому у кальмаров аксоны достигают
«гигантских» размеров (диаметр до 0,5
мм), что обеспечивает кальмару достаточно
быстрое проведение нервного импульса
и, следовательно, быстроту реакции
на внешние раздражители.
У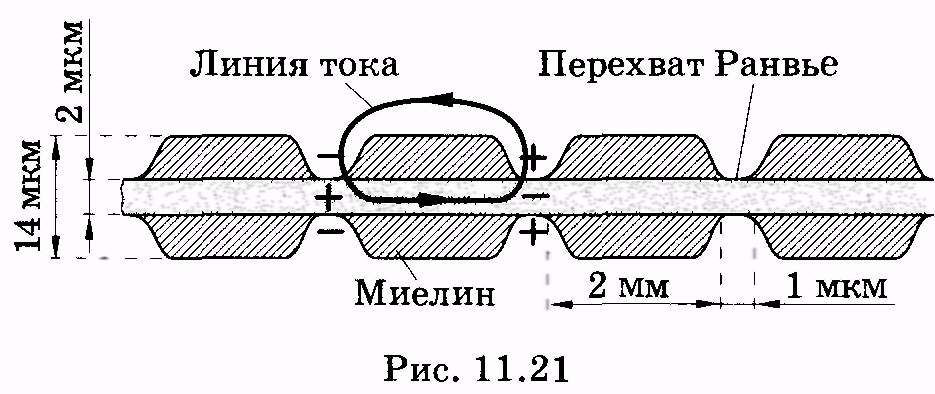
нервной системой
толстые волокна оказываются неэкономичными,
и затухание сигнала предотвращается
другим способом. Мембраны аксонов у них
покрытымиелином — веществом,
содержащим много холестерина и мало
белка (рис. 11.21). Удельное сопротивление
миелина значительно
выше удельного сопротивления других
биологических мембран. Помимо этого,
толщина миелиновой оболочки во много
раз больше толщины обычной мембраны,
что приводит к возрастанию диаметра
волокна и соответственно величины.
Как видно из рис. 11.21, миелиновая оболочка
не полностью покрывает
все волокно; оно разделено на отдельные
сегменты, между которыми на участках
длиной около 1 мкм мембрана аксона
непосредственно соприкасается с
внеклеточным раствором. Области, вкоторых мембрана
контактирует с раствором, называют
перехватами Ранвье. В связи с
большим сопротивлением миелиновой
оболочки по поверхности
аксона токи протекать не могут, и
затухание сигнала резко уменьшается.
При возбуждении одного узла возникают
токи между ним и другими узлами. Ток,
подошедший к другому узлу, возбуждает
его, вызывает появление в этом местепотенциала действия,
и процесс распространяется по всему
волокну. Затраты энергии на
распространение сигнала по волокну,покрытому миелином,
значительно меньше, чем по
немиелинизированному, так как общее
количество ионов натрия, проходящих
через мембрану
в области узлов, значительно меньше,
чем если бы они проходили через всю
поверхность мембраны. При некоторых
заболеваниях структура миелиновых
оболочек нарушается, и это
приводит к нарушению проведения нервного
возбуждения. При блокировании узлов
нервного волокна анестезирующими
средствами, например ядом кураре,
сопротивление аксона возрастает и
прохождение сигналов по нерву замедляется
или совсемпрекращается.
Поскольку
узлы замыкаются через аксоплазму и
внеклеточную
среду, то можно предположить, что при
увеличении сопротивления внешней среды
скорость проведения нервного импульса
уменьшится. Это предположение было
проверено на опыте. Нервные
волокна сначала помещали в морскую
воду, а затем в масло с большим удельным
сопротивлением. Скорость проведения
импульса во втором случае уменьшалась
в 1,5—2 раза (в зависимости от диаметра
волокна).
Существует
некоторая формальная аналогия между
распространением потенциала действия
по нервному волокну и электромагнитной
волной в двухпроводной линии или
коаксиальном кабеле. Однако между этими
процессами имеется существенное
различие.Электромагнитная
волна, распространяясь в среде, ослабевает,
так как растрачивает свою энергию.
Волна возбуждения, проходящая
по нервному волокну, не затухает, получая
энергию в самой
среде (энергию заряженной мембраны).
Волны, получающие энергию из среды
в процессе распространения, называютавтоволнами,
а среду —
активно-возбудимой
средой (ABC).
В § 11.9
будут рассмотрены более подробно
свойства авто волн, распространяющихся
в ABC.
Соседние файлы в папке лекции 2008-09
- #
- #
- #
- #
- #
- #
- #
Уравнение бернштейна для мембранного потенциала
Разность потенциалов, измеренная между внутренней и наружной поверхностями клеточной мембраны в состоянии физиологического покоя клетки, называется потенциалом покоя.
Потенциал покоя у разных клеток имеет величину от 50 до 100 мВ. Согласно современным взглядам, потенциал покоя по своей природе является мембранным потенциалом. Наличие мембраны приводит к возникновению потенциалов клеток, как в покое, так и при возбуждении. Причина их возникновения – неравномерное распределение ионов калия и натрия между содержимым клеток и межклеточной средой.Концентрация ионов калия внутри клеток в 20—40 раз превышает их содержание в окружающей клетку жидкости. Напротив, концентрация натрия в межклеточной жидкости в 10—20 раз выше, чем внутри клеток. Такое неравномерное распределение ионов обусловлено активным переносом ионов—работой натрий-калиевого насоса.
В 1905 г Бернштейн выдвинул гипотезу возникновения мембранного потенциала в покое. Он утверждал, что разность потенциалов на мембране обусловлена:
1. наличием разности концентраций ионов К + и Na + в цитоплазме клетки и снаружи.
2. В покое мембрана проницаема только для ионов К + .
В связи с этим был выведен равновесный калиевый потенциал, который определяется из уравнения Нернста
Исходя из гипотезы Бернштейна для мышечных волокон мембранный потенциал равен (-110) мВ, а экспериментальные данные давали (-90) мВ. Причина в расхождении в том, что гипотеза Бернштейна не учитывала проницаемость мембраны для других ионов, таких как Na + и Cl – .
Для более точного вычисления потенциала покоя необходимо учитывать не только диффузию ионов калия, но и диффузию натрия и хлора. Уравнение Нернста позволяет описывать мембранный потенциал только в первом приближении; для более точного определения потенциала применяют обобщенное уравнение Гольдмана-Ходжкина-Хаксли:
Е = (RT/ z F)·ln[( Рк·[K.]i + PNa·[Na]i + PCl·[Cl]e) / ( Рк·[K.]e + PNa·[Na]e + PCl·[Cl]i)
где Pk, PNa, PCl — коэффициенты проницаемости мембраны для ионов калия, натрия и хлора; [К], [Na], [Cl] — их активности внутри (i) и вне (е)клетки. Уравнение Гольдмана-Ходжкина-Хаксли позволяет определять мембранный потенциал не только в состоянии покоя, но и при возбуждении клетки. Для этого необходимо знание коэффициентов проницаемости для ионов. По данным Ходжкина и Катца (1949), для аксона кальмара в состоянии покоя отношение коэффициентов проницаемости Рк: Рnа : РCl= 1 : 0,04 : 0,45.
30. Потенциал действия. Изменение проницаемости мембраны для ионов Na+ и К+ при генерировании потенциала действия.
Потенциал действия – это скачкообразное изменение постоянного мембранного потенциала с отрицательной поляризации на положительную и обратно.
Потенциал действия — это возбуждение клетки, быстрое колебание мембранного потенциала вследствие диффузии ионов в клетку и из клетки.
В основе потенциала действия лежат последовательно развивающиеся во времени изменения ионной проницаемости клеточной мембраны.
Как отмечалось, в состоянии покоя проницаемость мембраны для калия превышает ее проницаемость для натрия. Вследствие этого поток К’+ из цитоплазмы во внешний раствор превышает противоположно направленный поток Na+ Поэтому наружная сторона мембраны в покое имеет положительный потенциал по отношению к внутренней.
При действии на клетку раздражителя проницаемость мембраны для Na+ резко повышается и в конечном итоге становится примерно в 20 раз больше проницаемости для К’+. Поэтому поток Na+ из внешнего раствора в цитоплазму начинает превышать направленный наружу калиевый ток. Это приводит к изменению знака (реверсии) мембранного потенциала: внутреннее содержимое клетки становится заряженным положительно по отношению к ее наружной поверхности. Указанное изменение мембранного потенциала соответствует восходящей фазе потенциала действия (фаза деполяризации).
Повышение проницаемости мембраны для Na + продолжается лишь очень короткое время. Вслед за этим проницаемость мембраны для Na + вновь понижается, а для К + возрастает.
Процесс, ведущий к понижению ранее увеличенной натриевой проницаемости мембраны, назван натриевой инактивацией. В результате инактивации поток Na + внутрь цитоплазмы резко ослабляется. Увеличение же калиевой проницаемости вызывает усиление потока К + из цитоплазмы во внешний раствор. В итоге этих двух процессов и происходит реполяризация мембраны: внутреннее содержимое клетки вновь приобретает отрицательный заряд по отношению к наружному раствору. Этому изменению потенциала соответствует нисходящая фаза потенциала действия (фаза реполяризации).
Одним из важных аргументов в пользу натриевой теории происхождения потенциалов действия был факт тесной зависимости его амплитуды от концентрации Na + во внешнем растворе. Опыты на гигантских нервных волокнах, перфузируемых изнутри солевыми растворами, позволили получить прямое подтверждение правильности натриевой теории. Установлено, что при замене аксоплазмы солевым раствором, богатым К + , мембрана волокна не только удерживает нормальный потенциал покоя, но в течение длительного времени сохраняет способность генерировать сотни тысяч потенциалов действия нормальной амплитуды. Если же К + во внутриклеточном растворе частично заменить на Na + и тем самым снизить градиент концентрации Nа + между наружной средой и внутренним раствором, амплитуда потенциала действия резко понижается. При полной замене К + на Na + волокно утрачивает способность генерировать потенциалы действия.
Эти опыты не оставляют сомнения в том, что поверхностная мембрана действительно является местом возникновения потенциала как в покое, так и при возбуждении. Становится очевидным, что разность концентраций Nа + и К + внутри и вне волокна является источником электродвижущей силы, обусловливающей возникновение потенциала покоя и потенциала действия.
На рис. 6 показаны изменения натриевой и калиевой проницаемости мембраны во время генерации потенциала действия в гигантском аксоне кальмара. Аналогичные отношения имеют место в других нервных волокнах, телах нервных клеток, а также в скелетных мышечных волокнах позвоночных животных. В скелетных мышцах ракообразных животных и гладких мышцах позвоночных в генезе восходящей фазы потенциала действия ведущую роль играют ионы Са 2+ . В клетках миокарда начальный подъем потенциала действия связан с повышением проницаемости мембраны для Nа + , а плато потенциала действия обусловлено повышением проницаемости мембраны и для ионов Са 2+
31. Потенциал-зависимые ионные каналы мембраны для К+ и Na+. Структура, особенности функционирования. Изменения проницаемости мембраны для К + и Na+ в различные фазы потенциала действия.
Состояние проницаемости клеточных мембран для различных веществ и, в частности, для минеральных ионов имеет исключительно важное значение в жизнедеятельности клетки и особенно в механизмах восприятия, преобразования, передачи сигналов от клетки к клетке и на внутриклеточные структуры.
Определяющую роль в состоянии проницаемости мембран клетки имеют их ионные каналы, которые формируются каналообразующими белками. Открытие и закрытие этих каналов могут контролироваться величиной разности потенциалов между наружной и внутренней поверхностями мембраны, множеством сигнальных молекул (гормонов, нейромедиаторов, сосудоактивных веществ) вторичными посредниками передачи внутриклеточных сигналов, минеральными ионами.
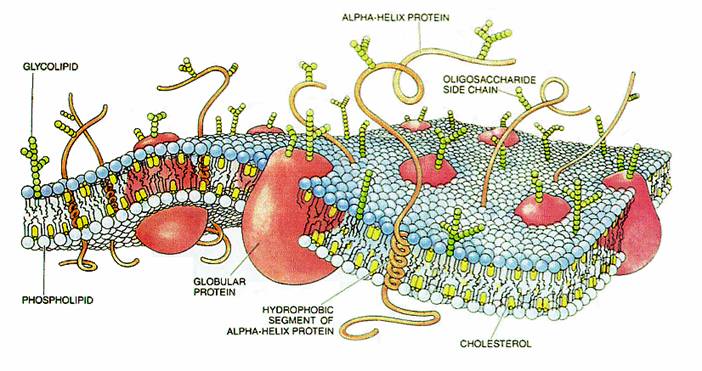
Ионный канал — несколько субъединиц (интегральных мембранных белков, содержащих трансмембранные сегменты, каждый из которых имеет а-спиральную конфигурацию), обеспечивающих перенос ионов через мембрану.
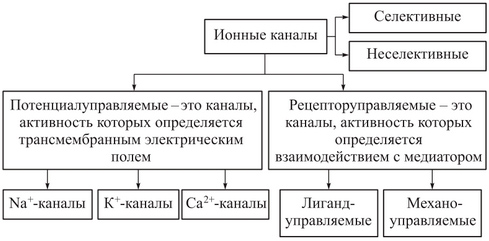
Рис. 1. Классификация ионных каналов
Современные представления о строении и функции ионных каналов стали возможными благодаря разработке методов регистрации электрических токов, протекающих через изолированный участок мембраны, содержащий одиночные ионные каналы, а также благодаря выделению и клонированию отдельных генов, контролирующих синтез белковых макромолекул, способных формировать ионные каналы. Это позволило искусственно модифицировать структуру таких молекул, встраивать их в мембраны клеток и изучать роль отдельных пептидных участков для выполнения функций каналов. Оказалось, что каналообразующие белковые молекулы всех ионных каналов имеют некоторые общие признаки строения и обычно представлены большими трансмембранными белками с молекулярными массами выше 250 кД.
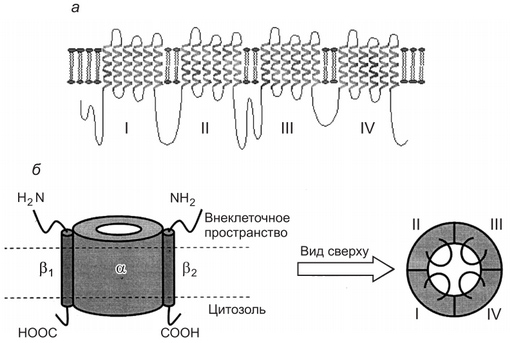
Они состоят из нескольких субъединиц. Обычно важнейшие свойства каналов определяются их а-субъединнней. Эта субъединица принимает участие в формировании ионоселективной норы, сенсорного механизма трансмембранной разности потенциалов — ворот канала и имеет места связывания для экзогенных и эндогенных лигандов. Другие субъединицы, входящие в структуру ионных каналов, играют вспомогательную роль, модулирующую свойства каналов (рис. 2).
Каналообразующая белковая молекула представлена внемембранными аминокислотными петлями и внутримембранными спирализованными участками-доменами, образующими субъединицы ионных каналов. Белковая молекула сворачивается в плоскости мембраны так, что между контактирующими друг с другом доменами и формируется собственно ионный канал (см. рис. 2, внизу справа).
Каналообразующая молекула белка располагается в цитоплазматической мембране так, что ее трехмерная пространственная структура формирует устья канала, обращенные к наружной и внутренней сторонам мемораны, пору, заполненную водой, и «ворота». Последние образуются участком пептидной цепи, который может легко изменять свою конформацию и определять открытое или закрытое состояние канала. От размеров поры и ее заряда зависят селективность и проницаемость ионного канала. Проницаемость канала для данного иона определяется также его размерами, величиной заряда и гидратной оболочкой.
Рис. 2. Строение Na+ -ионного канала клеточной мембраны: а — двухмерное строение а-еубъединицы ионного канала клеточной .мембраны; б — слева — натриевый канал, состоящий из а-субъединнцы и двух Р-субъединнн (вид сбоку); справа — вил натриевого канала сверху. Цифрами I. II. III. IV отмечены домены а-субъединицы
Типы ионных каналов
Описано более 100 разновидностей ионных каналов, для классификации которых используют различные подходы. Один из них основан на учете различий в строении каналов и в механизмах функционирования. При этом ионные каналы можно разделить на несколько типов:
§ пассивные ионные каналы, или каналы покоя;
§ каналы щелевых контактов;
§ каналы, состояние которых (открытое или закрытое) контролируется влиянием на их воротный механизм механических факторов (механочувствительные каналы), разности потенциалов на мембране (потенциалзависимые каналы) или лигандов, связывающихся с каналообразующим белком на внешней или внутренней стороне мембраны (лигандзависимые каналы).
Натриевые каналы
В клетках организма широко представлены потенциалзависимые, потенциалнезависимые (лигандзависимые, механочувствительные, пассивные и др.) натриевые каналы.
Формирование мембранного потенциала покоя
- 62855
- 36,8
- 30
- 30
Потенциал покоя. В мембране открыты калиевые ионные каналы постоянного тока, закрыты натриевые каналы, работает насос-обменник (Na + /K + -АТФаза).
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Потенциал покоя — это важное явление в жизни всех клеток организма, и важно знать, как он формируется. Однако это сложный динамический процесс, трудный для восприятия целиком, особенно для студентов младших курсов (биологических, медицинских и психологических специальностей) и неподготовленных читателей. Впрочем, при рассмотрении по пунктам, вполне возможно понять его основные детали и этапы. В работе вводится понятие потенциала покоя и выделяются основные этапы его формирования с использованием образных метафор, помогающих понять и запомнить молекулярные механизмы формирования потенциала покоя.
«Био/мол/текст»-2011
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2011 в номинации «Лучшая обзорная статья».
Мембранные транспортные структуры — натрий-калиевые насосы — создают предпосылки для возникновения потенциала покоя. Предпосылки эти — разность в концентрации ионов на внутренней и наружной сторонах клеточной мембраны. Отдельно проявляет себя разность концентрации по натрию и разность концентрации по калию. Попытка ионов калия (K + ) выровнять свою концентрацию по обе стороны мембраны приводит к его утечке из клетки и потере вместе с ними положительных электрических зарядов, за счёт чего значительно усиливается общий отрицательный заряд внутренней поверхности клетки. Эта «калиевая» отрицательность составляет бóльшую часть потенциала покоя (−60 мВ в среднем), а меньшую его часть (−10 мВ) составляет «обменная» отрицательность, вызванная электрогенностью самого ионного насоса-обменника.
Давайте разбираться подробнее.
Зачем нам нужно знать, что такое потенциал покоя и как он возникает?
Вы знаете, что такое «животное электричество»? Откуда в организме берутся «биотоки»? Как живая клетка, находящаяся в водной среде, может превратиться в «электрическую батарейку» и почему она моментально не разряжается?
На эти вопросы можно ответить только в том случае, если узнать, как клетка создаёт себе разность электрических потенциалов (потенциал покоя) на мембране.
Совершенно очевидно, что для понимания того, как работает нервная система, необходимо вначале разобраться, как работает её отдельная нервная клетка — нейрон. Главное, что лежит в основе работы нейрона — это перемещение электрических зарядов через его мембрану и появление вследствие этого на мембране электрических потенциалов. Можно сказать, что нейрон, готовясь к своей нервной работе, вначале запасает энергию в электрической форме, а затем использует ее в процессе проведения и передачи нервного возбуждения.
Таким образом, наш самый первый шаг к изучению работы нервной системы — это понять, каким образом появляется электрический потенциал на мембране нервных клеток. Этим мы и займёмся, и назовём этот процесс формированием потенциала покоя.
Определение понятия «потенциал покоя»
В норме, когда нервная клетка находится в физиологическом покое и готова к работе, у неё уже произошло перераспределение электрических зарядов между внутренней и наружной сторонами мембраны. За счёт этого возникло электрическое поле, и на мембране появился электрический потенциал — мембранный потенциал покоя.
Как известно из физики, электрические заряды (движущиеся и неподвижные) формируют в пространстве электромагнитное поле, которое влияет на тела, обладающие электрическим зарядом. С точки зрения электромагнетизма клеточную мембрану можно представить как плоский конденсатор, заполненный однородным диэлектриком из неполярных молекул. Если конденсатор заряжен, то внутри него возникает электрическое поле, обусловленное поверхностной плотностью заряда. На поверхности мембраны возникают некомпенсированные заряды: положительные у «отрицательной» поверхности и отрицательные — у «положительной» [6].
Таким образом, мембрана оказывается поляризованной. Это означает, что она имеет разный электрический потенциал наружной и внутренней поверхностей. Разность между этими потенциалами вполне возможно зарегистрировать.
В этом можно убедиться, если ввести внутрь клетки микроэлектрод, соединённый с регистрирующей установкой. Как только электрод попадает внутрь клетки, он мгновенно приобретает некоторый постоянный электроотрицательный потенциал по отношению к электроду, расположенному в окружающей клетку жидкости. Величина внутриклеточного электрического потенциала у нервных клеток и волокон, например, гигантских нервных волокон кальмара, в покое составляет около −70 мВ. Эту величину называют мембранным потенциалом покоя (МПП). Во всех точках аксоплазмы этот потенциал практически одинаков.
Ноздрачёв А.Д. и др. Начала физиологии [5].
Ещё немного физики. Макроскопические физические тела, как правило, электрически нейтральны, т.е. в них в равных количествах содержатся как положительные, так и отрицательные заряды. Зарядить тело можно, создав в нем избыток заряженных частиц одного вида, например, трением о другое тело, в котором при этом образуется избыток зарядов противоположного вида. Учитывая наличие элементарного заряда (e), полный электрический заряд любого тела можно представить как q = ±N×e, где N — целое число.
Потенциал электростатического поля φ определяется как отношение потенциальной энергии W пробного заряда q к величине этого заряда: φ = W/q, откуда следует, что потенциал численно равен потенциальной энергии, которой обладает в данной точке поля единичный положительный заряд. Единицей измерения потенциала служит вольт (1 В) [4]. В некоторых случаях потенциал электрического поля нагляднее определяется как физическая величина, численно равная работе внешних сил против сил электрического поля E при перемещении единичного положительного точечного заряда из бесконечности в данную точку. Последнее определение удобно записать следующим образом:
В электрофизиологии кроме потенциала покоя рассматриваются и другие электрические потенциалы: локальные постсинаптические и рецепторные потенциалы (возбуждающие и тормозные), электротонические и следовые потенциалы, миниатюрные потенциалы концевой пластинки, концентрационный потенциал и потенциал действия [5].
Потенциал покоя — это разность электрических потенциалов, имеющихся на внутренней и наружной сторонах мембраны, когда клетка находится в состоянии физиологического покоя. Его величина измеряется изнутри клетки, она отрицательна и составляет в среднем −70 мВ (милливольт), хотя в разных клетках может быть различной: от −35 мВ до −90 мВ.
Важно учитывать, что в нервной системе электрические заряды представлены не электронами, как в обычных металлических проводах, а ионами — химическими частицами, имеющими электрический заряд. И вообще в водных растворах в виде электрического тока перемещаются не электроны, а ионы. Поэтому все электрические токи в клетках и окружающей их среде — это ионные токи.
Итак, изнутри клетка в покое заряжена отрицательно, а снаружи — положительно. Это свойственно всем живым клеткам, за исключением, разве что, эритроцитов, которые, наоборот, заряжены отрицательно снаружи. Если говорить конкретнее, то получается, что снаружи вокруг клетки будут преобладать положительные ионы (катионы Na + и K + ), а внутри — отрицательные ионы (анионы органических кислот, не способные свободно перемещаться через мембрану, как Na + и K + ).
Теперь нам всего лишь осталось объяснить, каким же образом всё получилось именно так. Хотя, конечно, неприятно сознавать, что все наши клетки кроме эритроцитов только снаружи выглядят положительными, а внутри они — отрицательные.
Термин «отрицательность», который мы будем применять для характеристики электрического потенциала внутри клетки, пригодится нам для простоты объяснения изменений уровня потенциала покоя. В этом термине ценно то, что интуитивно понятно следующее: чем больше отрицательность внутри клетки — тем ниже в отрицательную сторону от нуля смещён потенциал, а чем меньше отрицательность — тем ближе отрицательный потенциал к нулю. Это намного проще понять, чем каждый раз разбираться в том, что же именно означает выражение «потенциал возрастает» — возрастание по абсолютному значению (или «по модулю») будет означать смещение потенциала покоя вниз от нуля, а просто «возрастание» — смещение потенциала вверх к нулю. Термин «отрицательность» не создаёт подобных проблем неоднозначности понимания.
Сущность формирования потенциала покоя
Попробуем разобраться, откуда берётся электрический заряд нервных клеток, хотя их никто не трёт, как это делают физики в своих опытах с электрическими зарядами.
Здесь исследователя и студента поджидает одна из логических ловушек: внутренняя отрицательность клетки возникает не из-за появления лишних отрицательных частиц (анионов), а, наоборот, из-за потери некоторого количества положительных частиц (катионов)!
Так куда же деваются из клетки положительно заряженные частицы? Напомню, что это покинувшие клетку и скопившиеся снаружи ионы натрия — Na + — и калия — K + .
Главный секрет появления отрицательности внутри клетки
Сразу откроем этот секрет и скажем, что клетка лишается части своих положительных частиц и заряжается отрицательно за счёт двух процессов:
- вначале она обменивает «свой» натрий на «чужой» калий (да-да, одни положительные ионы на другие, такие же положительные);
- потом из неё происходит утечка этих «наменянных» положительных ионов калия, вместе с которыми из клетки утекают положительные заряды.
Эти два процесса нам и надо объяснить.
Первый этап создания внутренней отрицательности: обмен Na + на K +
В мембране нервной клетки постоянно работают белковые насосы-обменники (аденозинтрифосфатазы, или Na + /K + -АТФазы), встроенные в мембрану. Они меняют «собственный» натрий клетки на наружный «чужой» калий.
Но ведь при обмене одного положительного заряда (Na + ) на другой такой же положительный заряд (K + ) никакого дефицита положительных зарядов в клетке возникать не может! Правильно. Но, тем не менее, из-за этого обмена в клетке остаётся очень мало ионов натрия, потому что они почти все ушли наружу. И в то же время клетка переполняется ионами калия, которые в неё накачали молекулярные насосы. Если бы мы могли попробовать на вкус цитоплазму клетки, мы бы заметили, что в результате работы насосов-обменников она превратилась из солёной в горько-солёно-кислую, потому что солёный вкус хлорида натрия сменился сложным вкусом довольно-таки концентрированного раствора хлорида калия. В клетке концентрация калия достигает 0,4 моль/л. Растворы хлорида калия в пределах 0,009–0,02 моль/л имеют сладкий вкус, 0,03–0,04 — горький, 0,05–0,1 — горько-солёный, а начиная с 0,2 и выше — сложный вкус, состоящий из солёного, горького и кислого [8].
Важно здесь то, что обмен натрия на калий — неравный. За каждые отданные клеткой три иона натрия она получает всего два иона калия. Это приводит к потере одного положительного заряда при каждом акте ионного обмена. Так что уже на этом этапе за счёт неравноценного обмена клетка теряет больше «плюсов», чем получает взамен. В электрическом выражении это составляет примерно −10 мВ отрицательности внутри клетки. (Но помните, что нам надо ещё найти объяснение для оставшихся −60 мВ!)
Чтобы легче было запомнить работу насосов-обменников, образно можно выразиться так: «Клетка любит калий!» Поэтому клетка и затаскивает калий к себе, несмотря на то, что его и так в ней полно. И поэтому она невыгодно обменивает его на натрий, отдавая 3 иона натрия за 2 иона калия. И поэтому она тратит на этот обмен энергию АТФ. И как тратит! До 70% всех энергозатрат нейрона может уходить на работу натрий-калиевых насосов. (Вот что делает любовь, пусть она даже и не настоящая!)
Кстати, интересно, что клетка не рождается с готовым потенциалом покоя. Ей его ещё надо создать. Например, при дифференцировке и слиянии миобластов потенциал их мембраны изменяется от −10 до −70 мВ, т.е. их мембрана становится более отрицательной — поляризуется в процессе дифференцировки. А в экспериментах на мультипотентных мезенхимальных стромальных клетках костного мозга человека искусственная деполяризация, противодействующая потенциалу покоя и уменьшающая отрицательность клеток, даже ингибировала (угнетала) дифференцировку клеток [1].
Образно говоря, можно выразиться так: Создавая потенциал покоя, клетка «заряжается любовью». Это любовь к двум вещам:
- любовь клетки к калию (поэтому клетка насильно затаскивает его к себе);
- любовь калия к свободе (поэтому калий покидает захватившую его клетку).
Механизм насыщения клетки калием мы уже объяснили (это работа насосов-обменников), а механизм ухода калия из клетки объясним ниже, когда перейдём к описанию второго этапа создания внутриклеточной отрицательности. Итак, результат деятельности мембранных ионных насосов-обменников на первом этапе формирования потенциала покоя таков:
- Дефицит натрия (Na + ) в клетке.
- Избыток калия (K + ) в клетке.
- Появление на мембране слабого электрического потенциала (−10 мВ).
Можно сказать так: на первом этапе ионные насосы мембраны создают разность концентраций ионов, или градиент (перепад) концентрации, между внутриклеточной и внеклеточной средой.
Второй этап создания отрицательности: утечка ионов K + из клетки
Итак, что начинается в клетке после того, как с ионами поработают её мембранные натрий-калиевые насосы-обменники?
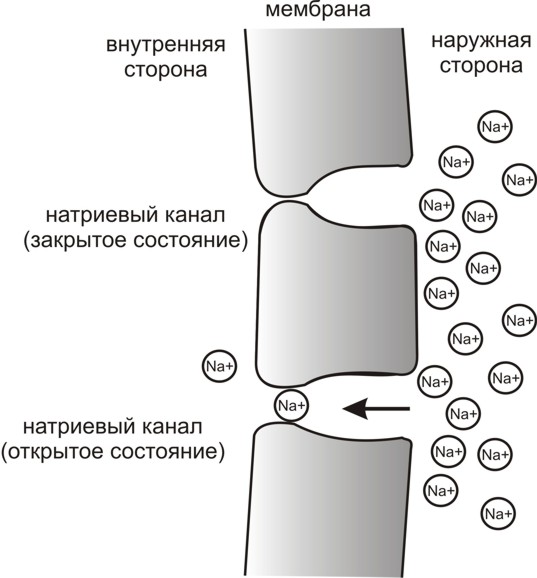
Из-за образовавшегося дефицита натрия внутри клетки этот ион при каждом удобном случае норовит устремиться внутрь: растворённые вещества всегда стремятся выровнять свою концентрацию во всём объёме раствора. Но это у натрия получается плохо, поскольку ионные натриевые каналы обычно закрыты и открываются только при определённых условиях: под воздействием специальных веществ (трансмиттеров) или при уменьшении отрицательности в клетке (деполяризации мембраны).
В то же время в клетке имеется избыток ионов калия по сравнению с наружной средой — потому что насосы мембраны насильно накачали его в клетку. И он, тоже стремясь уравнять свою концентрацию внутри и снаружи, норовит, напротив, выйти из клетки. И это у него получается!
Ионы калия K + покидают клетку под действием химического градиента их концентрации по разные стороны мембраны (мембрана значительно более проницаема для K + , чем для Na + ) и уносят с собой положительные заряды. Из-за этого внутри клетки нарастает отрицательность.
Тут ещё важно понять то, что ионы натрия и калия как бы «не замечают» друг друга, они реагируют только «на самих себя». Т.е. натрий реагирует на концентрацию натрия же, но «не обращает внимания» на то, сколько вокруг калия. И наоборот, калий реагирует только на концентрацию калия и «не замечает» натрий. Получается, что для понимания поведения ионов надо по отдельности рассматривать концентрации ионов натрия и калия. Т.е. надо отдельно сравнить концентрацию по натрию внутри и снаружи клетки и отдельно — концентрацию по калию внутри и снаружи клетки, но не имеет смысла сравнивать натрий с калием, как это, бывает, делается в учебниках.
По закону выравнивания химических концентраций, который действует в растворах, натрий «хочет» снаружи войти в клетку; туда же его влечёт и электрическая сила (как мы помним, цитоплазма заряжена отрицательно). Хотеть-то он хочет, но не может, так как мембрана в обычном состоянии плохо его пропускает. Натриевые ионные каналы, имеющиеся в мембране, в норме закрыты. Если все же его заходит немножко, то клетка сразу же обменивает его на наружный калий с помощью своих натрий-калиевых насосов-обменников. Получается, что ионы натрия проходят через клетку как бы транзитом и не задерживаются в ней. Поэтому натрий в нейронах всегда в дефиците.
А вот калий как раз может легко выходить из клетки наружу! В клетке его полно, и она его удержать не может. Он выходит наружу через особые каналы в мембране — «калиевые каналы утечки», которые в норме открыты и выпускают калий [5, 7].
К + -каналы утечки постоянно открыты при нормальных значениях мембранного потенциала покоя и проявляют взрывы активности при сдвигах мембранного потенциала, которые длятся несколько минут и наблюдаются при всех значениях потенциала. Усиление К + -токов утечки ведёт к гиперполяризации мембраны, тогда как их подавление — к деполяризации. . Однако, существование канального механизма, ответственного за токи утечки, долгое время оставалось под вопросом. Только сейчас стало ясно, что калиевая утечка — это ток через специальные калиевые каналы.
Зефиров А.Л. и Ситдикова Г.Ф. Ионные каналы возбудимой клетки (структура, функция, патология) [7].
От химического — к электрическому
А теперь — ещё раз самое главное. Мы должны осознанно перейти от движения химических частиц к движению электрических зарядов.
Калий (K + ) положительно заряжен, и поэтому он, когда выходит из клетки, выносит из неё не только самого себя, но и положительный заряд. За ним изнутри клетки к мембране тянутся «минусы» — отрицательные заряды. Но они не могут просочиться через мембрану — в отличие от ионов калия — т.к. для них нет подходящих ионных каналов, и мембрана их не пропускает. Помните про оставшиеся необъяснёнными нами −60 мВ отрицательности? Это и есть та самая часть мембранного потенциала покоя, которую создаёт утечка ионов калия из клетки! И это — большая часть потенциала покоя.
Для этой составной части потенциала покоя есть даже специальное название — концентрационный потенциал [5]. Концентрационный потенциал — это часть потенциала покоя, созданная дефицитом положительных зарядов внутри клетки, образовавшимся за счёт утечки из неё положительных ионов калия.
Ну, а теперь немного физики, химии и математики для любителей точности.
Электрические силы связаны с химическими по уравнению Гольдмана. Его частным случаем является более простое уравнение Нернста, по формуле которого можно рассчитать трансмембранную диффузионную разность потенциалов на основе различной концентрации ионов одного вида по разные стороны мембраны. Так, зная концентрацию ионов калия снаружи и внутри клетки, можно рассчитать калиевый равновесный потенциал EK:
где Ек — равновесный потенциал, R — газовая постоянная, Т — абсолютная температура, F — постоянная Фарадея, К + внеш и K + внутр — концентрации ионов К + снаружи и внутри клетки, соответственно. По формуле видно, что для расчёта потенциала между собой сравниваются концентрации ионов одного вида — K + .
Более точно итоговая величина суммарного диффузионного потенциала, который создаётся утечкой нескольких видов ионов, рассчитывается по формуле Гольдмана-Ходжкина-Катца. В ней учтено, что потенциал покоя зависит от трех факторов: (1) полярности электрического заряда каждого иона; (2) проницаемости мембраны Р для каждого иона; (3) [концентраций соответствующих ионов] внутри (внутр) и снаружи мембраны (внеш). Для мембраны аксона кальмара в покое отношение проводимостей РK : PNa :PCl = 1 : 0,04 : 0,45 [5].
Заключение
Итак, поте нциал покоя состоит из двух частей:
- −10 мВ, которые получаются от «несимметричной» работы мембранного насоса-обменника (ведь он больше выкачивает из клетки положительных зарядов (Na + ), чем закачивает обратно с калием).
- Вторая часть — это всё время утекающий из клетки калий, уносящий положительные заряды. Его вклад — основной: −60 мВ. В сумме это и дает искомые −70 мВ.
Что интересно, калий перестанет выходить из клетки (точнее, его вход и выход уравниваются) только при уровне отрицательности клетки −90 мВ. В этом случае сравняются химические и электрические силы, проталкивающие калий через мембрану, но направляющие его в противоположные стороны. Но этому мешает постоянно подтекающий в клетку натрий, который несёт с собой положительные заряды и уменьшает отрицательность, за которую «борется» калий. И в итоге в клетке поддерживается равновесное состояние на уровне −70 мВ.
Вот теперь мембранный потенциал покоя окончательно сформирован.
Схема работы Na + /K + -АТФазы наглядно иллюстрирует «несимметричный» обмен Na + на K + : выкачивание избыточного «плюса» в каждом цикле работы фермента приводит к отрицательному заряжению внутренней поверхности мембраны. Чего в этом ролике не сказано, так это того, что АТФаза ответственна за менее чем 20% потенциала покоя (−10 мВ): оставшаяся «отрицательность» (−60 мВ) появляется за счет выхода из клетки через «калиевые каналы утечки» ионов K + , стремящихся выровнять свою концентрацию внутри клетки и вне нее.
Потенциал покоя. Уравнение Нернста. Уравнение Гольдмана-Ходжкина-Катца
Потенциал покоя (ПП, мембранный потенциал покоя). ПП называется разность потенциалов между внутренней и наружной сторонами клеточной мембраны, возникающей в состоянии покоя клетки. У живых клеток в покое между внутренним содержимым клетки и наружным раствором существует отрицательная разность потенциалов (ПП) порядка 60—90 мВ, которая локализована на поверхностной мембране. Внутренняя сторона мембраны заряжена электроотрицательно по отношению к наружной. ПП обусловлен избирательной проницаемостью покоящейся мембраны для ионов К + (Ю. Бернштейн, 1902, 1912. А. Ходжкин и Б. Катц, 1947).
Предположим, что клетку с мембраной, проницаемой только для ионов калия, поместили в электролит, где их концентрация меньше, чем внутри клетки. Сразу после соприкосновения мембраны с раствором ионы калия начнут выходить из клетки наружу, как выходит газ из надутого шара. Но каждый ион несет с собой положительный электрический заряд, и чем больше ионов калия покинет клетку, тем более электроотрицательным станет ее содержимое. Поэтому на каждый ион калия, выходящий из клетки, будет действовать электрическая сила, препятствующая его движению наружу. В конце концов, установится равновесие, при котором электрическая сила, действующая на ион калия в канале мембраны, будет равна силе, обусловленной различием концентраций ионов калия внутри и вне клетки. Очевидно, что в результате такого равновесия между внутренним и наружным растворами появится разность потенциалов. При этом, если за нуль потенциала принять потенциал внешнего раствора, то потенциал внутри клетки будет отрицательным. Эта разность потенциалов – самое простое из наблюдаемых биоэлектрических явлений – носит название «потенциал покоя» клетки. В первом приближении величину ПП можно рассчитать с помощью формулы Нернста:

где 

Подставляя численные значения в формулу Нернста, получим значение ПП порядка -87 мВ, что весьма близко к экспериментально измеренному значению ПП. Дальнейшие исследования показали, что вклад в формирование ПП вносят не только ионы калия, но и ионы натрия и хлора.
Концентрация К + в протоплазме примерно в 50 раз выше, чем во внеклеточной жидкости, поэтому, диффундируя из клетки, ионы выносят на наружную сторону мембраны положительные заряды, при этом внутренняя сторона мембраны, практически не проницаемой для крупных органических анионов, приобретает отрицательный потенциал. Поскольку проницаемость мембраны в покое для Na + примерно в 100 раз ниже, чем для К + , диффузия натрия из внеклеточной жидкости (где он является основным катионом) в протоплазму мала и лишь незначительно снижает ПП, обусловленный ионами К + .
В скелетных мышечных волокнах в возникновении потенциала покоя важную роль играют также ионы Cl – , диффундирующие внутрь клетки. Следствием ПП является ток покоя, регистрируемый между поврежденным и интактным участками нерва или мышцы при приложении отводящих электродов. Мембраны нервных и мышечных клеток (волокон) способны изменять ионную проницаемость в ответ на сдвиги мембранного потенциала. При увеличении ПП (гиперполяризация мембраны) проницаемость поверхностных клеточных мембран для Na + и К + падает, а при уменьшении ПП (деполяризация) она возрастает, причём скорость изменений проницаемости для Na + значительно превышает скорость увеличения проницаемости мембраны для К + . Более точные значения для ПП вычисляются по формуле Гольдмана-Ходжкина-Катца (ГХК), которая учитывает проницаемость КМ в покое не только для ионов калия, но и для ионов натрия и хлора:

где PK, PNa, PCl – проницаемость КМ для ионов калия, натрия и хлора, выражения […]i и […]0 обозначают концентрации соответствующих молекул внутри и вне клетки.
В качестве примера вычислим величину ПП для гигантского аксона кальмара. Концентрации ионов внутри и вне аксона приведены ниже (см. таблицу).
| Ион | Концентрация (моль на 1 кг воды) |
| Внутри (i) | Вне (0) |
| Na + | |
| K + | |
| Cl – |
В состоянии покоя при физиологических условиях соотношение коэффициентов проницаемости равно:
Диффузия ионов калия и хлора идет через КМ в обе стороны. Натрий за счет механизма пассивного транспорта проникает внутрь аксона и за счет активного транспорта выносится из клетки. Следовательно, основной вклад в формирование ПП вносят ионы калия и хлора. Подставив численные значения проницаемостей и концентраций для ионов калия хлора в формулу Гольдмана-Ходжкина-Катца для температуры t=30 0 C вычислим:
Значение ПП, вычисленное по формуле Нернста, равно:
Формула Нернста дает несколько заниженное значение потенциала покоя, а формула ГХК приводит к более реалистичным значениям ПП, измеренным экспериментально на крупных клетках.
Следует также отметить, что ни формула Нернста, ни формула ГХК не учитывают механизма активного транспорта.
Формула Томаса для ПП учитывает работу электрогенных ионных Na-K- насосов и имеет вид:

где m – отношение количества ионов натрия к количеству ионов калия, переносимых натрий-калиевым насосом через КМ. Наиболее распространенный режим работы Na + -K + -АТФ-азы наблюдается при m=3/2. В уравнении Томаса отсутствуют члены PCl[Cl – ], так как нет активного транспорта для ионов хлора через КМ.
Численное значение ПП по формуле Томаса равно:

Коэффициент m, применяемый в уравнении Томаса, усиливает вклад градиента концентрации ионов калия в формирование ПП. Поэтому ПП, рассчитанный по формуле Томаса, по абсолютному значению меньше ПП, рассчитанного по формуле ГХК. Значение ПП, полученное с помощью формулы Томаса, хорошо совпадает со значениями ПП, измеренными экспериментально на мелких клетках.
источники:
http://biomolecula.ru/articles/formirovanie-membrannogo-potentsiala-pokoia
http://megalektsii.ru/s23176t4.html
Потенциал действия — волна возбуждения, перемещающаяся по мембране живой клетки в процессе передачи нервного сигнала. По сути своей представляет электрический разряд — быстрое кратковременное изменение потенциала на небольшом участке мембраны возбудимой клетки (нейрона, мышечного волокна или железистой клетки), в результате которого наружная поверхность этого участка становится отрицательно заряженной по отношению к соседним участкам мембраны, тогда как его внутренняя поверхность становится положительно заряженной по отношению к соседним участкам мембраны. Потенциал действия является физической основой нервного или мышечногоимпульса, играющего сигнальную (регуляторную) роль.
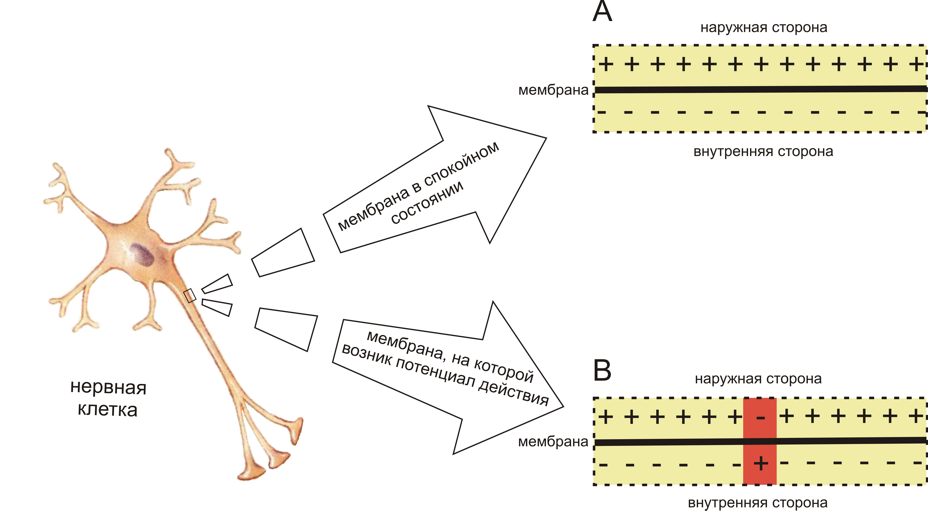
Рис. 1. Схема распределения зарядов по разные стороны мембраны возбудимой клетки в спокойном состоянии (A) и при возникновении потенциала действия (B) (см. объяснения в тексте)
Потенциалы действия могут различаться по своим параметрам в зависимости от типа клетки и даже на различных участках мембраны одной и той же клетки. Наиболее характерный пример различий: потенциал действия сердечной мышцыи потенциал действия большинства нейронов. Тем не менее, в основе любого потенциала действия лежат следующие явления:
- Мембрана живой клетки поляризована — её внутренняя поверхность заряжена отрицательно по отношению к внешней благодаря тому, что в растворе возле её внешней поверхности находится бо́льшее количество положительно заряженных частиц (катионов), а возле внутренней поверхности — бо́льшее количество отрицательно заряженных частиц (анионов).
- Мембрана обладает избирательной проницаемостью — её проницаемость для различных частиц (атомов или молекул) зависит от их размеров, электрического заряда и химических свойств.
- Мембрана возбудимой клетки способна быстро менять свою проницаемостъ для определённого вида катионов, вызывая переход положительного заряда с внешней стороны на внутреннюю (Рис.1).
Первые два свойства характерны для всех живых клеток. Третье же является особенностью клеток возбудимых тканей и причиной, по которой их мембраны способны генерировать и проводить потенциалы действия.
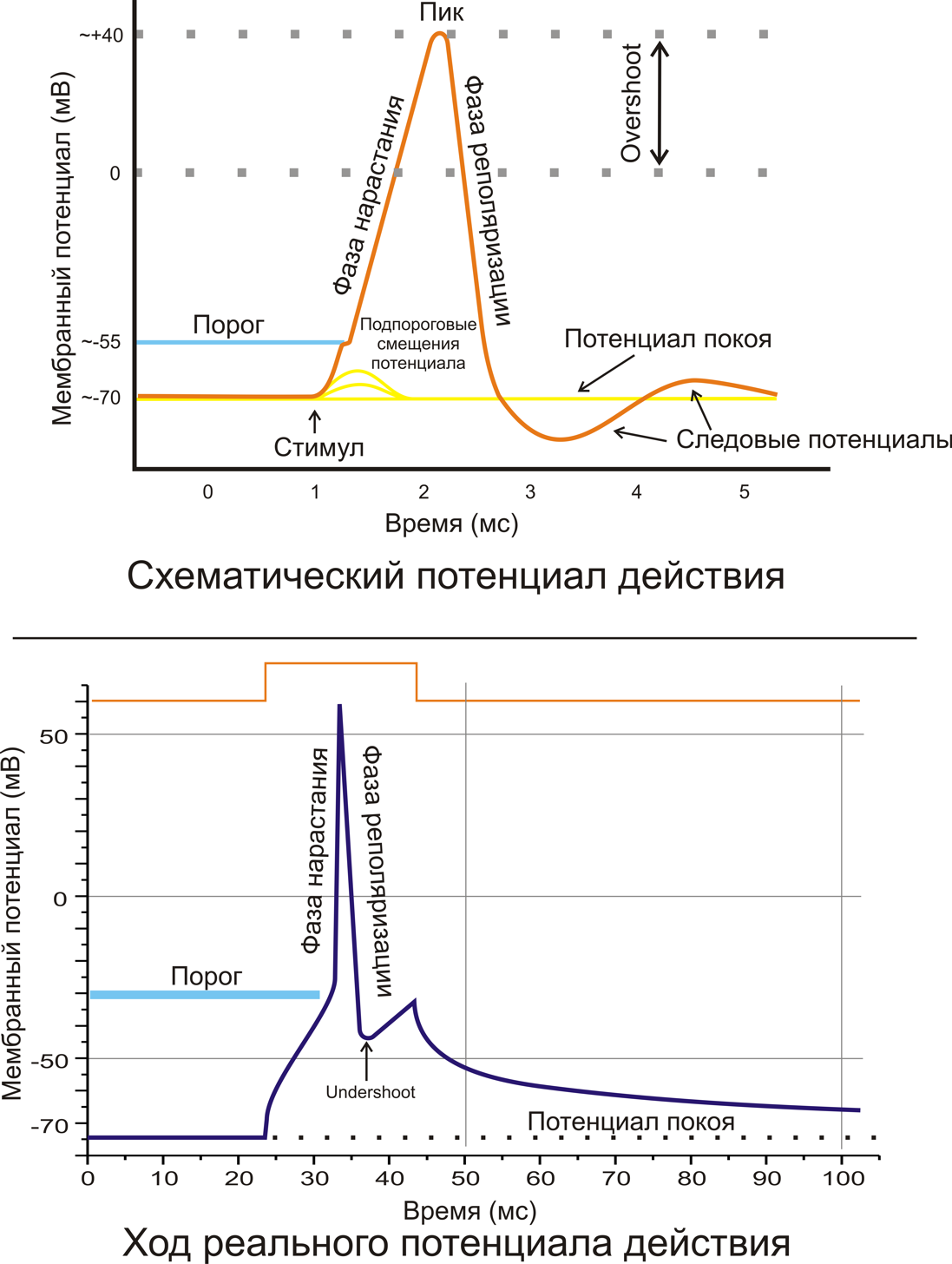
- Фазы потенциала действия
- Предспайк — процесс медленной деполяризации мембраны до критического уровня деполяризации (местное возбуждение, локальный ответ).
- Пиковый потенциал, или спайк, состоящий из восходящей части (деполяризация мембраны) и нисходящей части (реполяризация мембраны).
- Отрицательный следовой потенциал — от критического уровня деполяризации до исходного уровня поляризации мембраны (следовая деполяризация).
- Положительный следовой потенциал — увеличение мембранного потенциала и постепенное возвращение его к исходной величине (следовая гиперполяризация).
Общие положения
Поляризация мембраны живой клетки обусловлена отличием ионного состава с её внутренней и наружной стороны. Когда клетка находится в спокойном (невозбуждённом) состоянии, ионы по разные стороны мембраны создают относительно стабильную разность потенциалов, называемую потенциалом покоя. Если ввести внутрь живой клетки электрод и измерить мембранный потенциал покоя, он будет иметь отрицательное значение (порядка −70 — −90 мВ). Это объясняется тем, что суммарный заряд на внутренней стороне мембраны существенно меньше, чем на внешней, хотя с обеих сторон содержатся и катионы, и анионы. Снаружи — на порядок больше ионов натрия, кальция и хлора, внутри — ионов калия и отрицательно заряженных белковыхмолекул, аминокислот, органических кислот, фосфатов, сульфатов. Надо понимать, что речь идёт именно о заряде поверхности мембраны — в целом среда и внутри, и снаружи клетки заряжена нейтрально.
Потенциал мембраны может изменяться под действием различных стимулов. Искусственным стимулом может служить электрический ток, подаваемый на внешнюю или внутреннюю сторону мембраны через электрод. В естественных условиях стимулом часто служит химический сигнал от соседних клеток, поступающий черезсинапс или путём диффузной передачи через межклеточную среду. Смещение мембранного потенциала может происходить в отрицательную (гиперполяризация) или положительную (деполяризация) сторону.
В нервной ткани потенциал действия, как правило, возникает при деполяризации — если деполяризация мембраны нейрона достигает некоторого порогового уровня или превышает его, клетка возбуждается, и от её тела к аксонам и дендритам распространяется волна электрического сигнала. (В реальных условиях на теле нейрона обычно возникают постсинаптические потенциалы, которые сильно отличаются от потенциала действия по своей природе — например, они не подчиняются принципу «всё или ничего». Эти потенциалы преобразуются в потенциал действия на особом участке мембраны — аксонном холмике, так что потенциал действия не распространяется на дендриты).
Это обусловлено тем, что на мембране клетки находятся ионные каналы — белковые молекулы, образующие в мембране поры, через которые ионы могут проходить с внутренней стороны мембраны на наружную и наоборот. Большинство каналов ионоспецифичны — натриевый канал пропускает практически только ионы натрия и не пропускает другие (это явление называют селективностью). Мембрана клеток возбудимых тканей (нервной и мышечной) содержит большое количество потенциал-зависимых ионных каналов, способных быстро реагировать на смещение мембранного потенциала. Деполяризация мембраны в первую очередь вызывает открытие потенциал-зависимых натриевых каналов. Когда одновременно открывается достаточно много натриевых каналов, положительно заряженные ионы натрия устремляются через них на внутреннюю сторону мембраны. Движущая сила в данном случае обеспечивается градиентом концентрации (с внешней стороны мембраны находится намного больше положительно заряженных ионов натрия, чем внутри клетки) и отрицательным зарядом внутренней стороны мембраны (см. Рис. 2). Поток ионов натрия вызывает ещё бо́льшее и очень быстрое изменение мембранного потенциала, которое и называют потенциалом действия (в специальной литературе обозначается ПД).
Рис. 3. Простейшая схема, демонстрирующая мембрану с двумя натриевыми каналами в открытом и закрытом состоянии, соответственно
Согласно закону «всё-или-ничего» мембрана клетки возбудимой ткани либо не отвечает на стимул совсем, либо отвечает с максимально возможной для неё на данный момент силой. То есть, если стимул слишком слаб и порог не достигнут, потенциал действия не возникает совсем; в то же время, пороговый стимул вызовет потенциал действия такой же амплитуды, как и стимул, превышающий пороговый. Это отнюдь не означает, что амплитуда потенциала действия всегда одинакова — один и тот же участок мембраны, находясь в разных состояниях, может генерировать потенциалы действия разной амплитуды.
После возбуждения нейрон на некоторое время оказывается в состоянии абсолютной рефрактерности, когда никакие сигналы не могут его возбудить снова, затем входит в фазу относительной рефрактерности, когда его могут возбудить исключительно сильные сигналы (при этом амплитуда ПД будет ниже, чем обычно). Рефрактерный период возникает из-за инактивации быстрого натриевого тока, то есть инактивации натриевых каналов (см. ниже).
Распространение потенциала действия
Распространение потенциала действия по немиелинизированным волокнам
По немиелинизированному волокну ПД распространяется непрерывно. Проведение нервного импульса начинается с распространением электрического поля. Возникший ПД за счет электрического поля способен деполяризовать мембрану соседнего участка до критического уровня, в результате чего на соседнем участке генерируются новые ПД. Сами ПД не перемещаются, они исчезают там же, где возникают. Главную роль в возникновении нового ПД играет предыдущий.
Если внутриклеточным электродом раздражать аксон посередине, то ПД будет распространяться в обоих направлениях. Обычно же ПД распространяется по аксону в одном направлении (от тела нейрона к нервным окончаниям), хотя деполяризация мембраны происходит по обе стороны от участка, где в данный момент возник ПД. Одностороннее проведение ПД обеспечивается свойствами натриевых каналов — после открывания они на некоторое время инактивируются и не могут открыться ни при каких значениях мембранного потенциала (свойство рефрактерности). Поэтому на ближнем к телу клетки участке, где до этого уже «прошел» ПД, он не возникает.
При прочих равных условиях распространение ПД по аксону происходит тем быстрее, чем больше диаметр волокна. По гигантским аксонам кальмара ПД может распространяться почти с такой же скоростью, как и по миелинизированным волокнам позвоночных (около 100 м/c).
Распространение потенциала действия по миелинизированным волокнам
По миелинизированному волокну ПД распространяется скачкообразно (сальтаторное проведение). Для миелинизированных волокон характерна концентрация потенциалзависимых ионных каналов только в областях перехватов Ранвье; здесь их плотность в 100 раз больше, чем в мембранах безмиелиновых волокон. В области миелиновых муфт потенциалзависимых каналов почти нет. ПД, возникший в одном перехвате Ранвье, за счет электрического поля деполяризует мембрану соседних перехватов до критического уровня, что приводит к возникновению в них новых ПД, то есть возбуждение переходит скачкообразно, от одного перехвата к другому. В случае повреждения одного перехвата Ранвье ПД возбуждает 2-ой, 3-ий, 4-ый и даже 5-ый, поскольку электроизоляция, создаваемая миелиновыми муфтами, уменьшает рассеивание электрического поля. Это увеличивает скорость распространения ПД по миелинизированным волокнам по сравнению с немиелинизированными. Кроме того, миелинизированные волокна толще, а электрическое сопротивление более толстых волокон меньше, что тоже увеличивает скорость проведения импульса по миелинизированным волокнам. Другим преимуществом сальтаторного проведения является его экономичность в энергетическом плане, так как возбуждаются только перехваты Ранвье, площадь которых меньше 1 % мембраны, и, следовательно, необходимо значительно меньше энергии для восстановления трансмембранных градиентов Na+ и K+, расходующихся в результате возникновения ПД, что может иметь значение при высокой частоте разрядов, идущих по нервному волокну.
Чтобы представить, насколько эффективно может быть увеличена скорость проведения за счёт миелиновой оболочки, достаточно сравнить скорость распространения импульса по немиелинизированным и миелинизированным участкам нервной системы человека. При диаметре волокна около 2 µм и отсутствии миелиновой оболочки скорость проведения будет составлять ~1 м/с, а при наличии даже слабой миелинизации при том же диаметре волокна — 15-20 м/с. В волокнах большего диаметра, обладающих толстой миелинововой оболочкой, скорость проведения может достигать 120 м/с.
Скорость распространения потенциала действия по мембране отдельно взятого нервного волокна отнюдь не является постоянной величиной — в зависимости от различных условий, эта скорость может очень значительно уменьшаться и, соответственно, увеличиваться, возвращаясь к некоему исходному уровню.
Активные свойства мембраны
Активные свойства мембраны, обеспечивающие возникновение потенциала действия, основываются главным образом на поведении потенциалзависимых натриевых (Na+) и калиевых (K+) каналов. Начальная фаза ПД формируется входящим натриевым током, позже открываются калиевые каналы и выходящий K+-ток возвращает потенциал мембраны к исходному уровню. Исходную концентрацию ионов затем восстанавливает натрий-калиевый насос.
Схема строения мембраны клетки
По ходу ПД каналы переходят из состояния в состояние: у Na+ каналов основных состояний три — закрытое, открытое и инактивированное (в реальности дело сложнее, но этих трёх достаточно для описания), у K+ каналов два — закрытое и открытое.
Поведение каналов, участвующих в формировании ПД, описывается через проводимость и высчиляется черезкоэффициенты переноса (трансфера).
Коэффициенты переноса были выведены Ходжкиным и Хаксли.
Проводимость для калия GK на единицу площади [S/cm²]
Проводимость для натрия GNa на единицу площади [S/cm²]
рассчитывается сложнее, поскольку, как уже было сказано, у потенциал-зависимых Na+ каналов, помимо закрытого/открытого состояний, переход между которыми описывается параметром 
 , , |
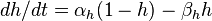 , , |
| где: | где: |
 – коэффициент трансфера из закрытого в открытое состояние для Na+ каналов [1/s]; – коэффициент трансфера из закрытого в открытое состояние для Na+ каналов [1/s]; |
 – коэффициент трансфера из инактивированного в не-инактивированное состояние для Na+ каналов [1/s]; – коэффициент трансфера из инактивированного в не-инактивированное состояние для Na+ каналов [1/s]; |
 – коэффициент трансфера из открытого в закрытое состояние для Na+ каналов [1/s]; – коэффициент трансфера из открытого в закрытое состояние для Na+ каналов [1/s]; |
 – коэффициент трансфера из не-инактивированного в инактивированное состояние для Na+ каналов [1/s]; – коэффициент трансфера из не-инактивированного в инактивированное состояние для Na+ каналов [1/s]; |
 – фракция Na+ каналов в открытом состоянии; – фракция Na+ каналов в открытом состоянии; |
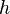 – фракция Na+ каналов в не-инактивированном состоянии; – фракция Na+ каналов в не-инактивированном состоянии; |
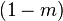 – фракция Na+ каналов в закрытом состоянии – фракция Na+ каналов в закрытом состоянии |
 – фракция Na+ каналов в инактивированном состоянии. – фракция Na+ каналов в инактивированном состоянии. |
Материал из Википедии — свободной энциклопедии