Полинейропатия — это патология периферической нервной системы, которая развивается в результате диффузного повреждения периферических нервов и их аксонов. Отсюда и название болезни. В ее основе — генерализованное поражение осевого цилиндра периферических нервов.
Что такое аксональная полинейропатия
Полиневропатия (второе название — полиневрит) — это клинический синдром, который возникает из-за ряда факторов, влияющих на периферическую нервную систему, и отличается размытыми патогенетическими изменениями. Заболевание занимает одно из лидирующих мест в перечне недугов периферической нервной системы, уступая первенство только вертеброгенной патологии, превосходящей по сложности клинической картины и последствиям, развивающимся из-за нее.
Аскональная полинейропатия считается междисциплинарной проблемой, с ней часто сталкиваются доктора различных специализаций. В первую очередь с данным заболеванием обращаются к неврологу. Частота возникающего синдрома неизвестна, так как отсутствуют статистические данные.
На данный момент известны всего три важных патоморфологических механизма, которые лежат в истоках формирования полинейропатии:
- валлеровская дегенерация;
- первичная демиелинизация;
- первичная аксонопатия.
В соответствии с иммунологической теорией полинейропатия является результатом перекрестного образования иммунных глобулинов, уничтожающих собственные клетки, в результате чего возникает некроз тканей и мышечное воспаление.
Исследователи выдвигают ряд гипотез возникновения и проблем течения аксональной полинейропатии:
- Сосудистая. Базируется на вовлечении в процесс сосудов, по которым кислород и питательные вещества поступают в периферические нервы. Изменяются характеристики крови по качественному и количественному составу, что может привести к ишемии нервных окончаний.
- Теория оксидативного стресса. Позиционирует формирование болезни со стороны нарушения обмена оксида азота, вследствие чего изменяются калий-натриевые механизмы, лежащие в основе формирования нервного возбуждения и проведения импульсов по нервам.
- Теория деактивации факторов роста нерва. Говорит о том, что болезнь возникает из-за недостатка аксонального транспорта с последующим развитием аксонопатии.
- Иммунологическая. Объясняет развитие заболевания в результате перекрестного образования антител к структурам периферической нервной системы, которое сопровождается аутоиммунным воспалением, а затем и некрозом нервов.
Даже при использовании ультрасовременных методов диагностики сложно найти достоверную причину патологии, выяснить ее получается только у 50-70% пострадавших.
Факторов возникновения полинейропатии нижних конечностей по аксональному типу очень много. Однако даже инновационные способы исследования не позволяют установить истинную этиологию заболевания.
Мнение эксперта
Автор: Алексей Владимирович Васильев
Руководитель НПЦ болезни двигательного нейрона/БАС, кандидат медицинских наук, врач высшей категории
Аксональная полинейропатия — это одно из самых опасных неврологических заболеваний, сопровождающееся поражением периферической нервной системы. При болезни разрушаются периферические нервные волокна.
Причин возникновение аксональной полинейропатии несколько. Самые распространенные:
- Сахарный диабет нарушает структуру крови, питающей нервы, в свою очередь происходит сбой в обменных процессах.
- Длительный дефицит витаминов В. Именно они максимально важны для правильной работы нервной системы, поэтому долгая нехватка способна привести к аксональной полинейропатии.
- Воздействие токсинов на организм. К ним относят разнообразные отравляющие вещества, например, алкоголь, а также ВИЧ. При отравлении опасными веществами заболевание может развиться уже через несколько дней.
- Наследственный фактор.
- Синдром Гийена-Барре.
- Различные травмы, к которым также относится длительное сдавливание нервов, которое характерно при грыже или остеохондрозе.
Лечение аксональной полинейропатии обязательно должно быть комплексным, иначе нужного эффекта достичь не удастся. Категорически запрещается заниматься самолечением и при возникновении первых же симптомов нужно срочно обратиться к доктору. Врачи Юсуповской больницы подбирают лечение индивидуально для каждого пациента. В зависимости от тяжести патологии и симптоматики назначается комплексное лечение под наблюдением опытных специалистов.
Причины
Самые распространенные причины возникновения аксональной полинейропатии нижних конечностей:
- истощение организма;
- длительный недостаток витаминов группы В;
- недуги, ведущие к дистрофии;
- острые инфекции;
- токсическое поражение ртутью, свинцом, кадмием, угарным газом, спиртными напитками, метиловым спиртом, фосфорорганическими соединениями, медицинскими препаратами, принимаемыми без согласования с врачом;
- болезни сердечно-сосудистой, кроветворной, кровеносной и лимфатической систем;
- эндокринологические патологии, в том числе инсулинозависимость.
Главными факторами, которые провоцируют развитие моторной или сенсомоторной аксональной полинейропатии, являются:
- эндогенная интоксикация при почечной недостаточности;
- аутоиммунные процессы, протекающие в организме;
- амилоидоз;
- вдыхание токсических веществ или паров.
Также болезнь может быть обусловлена наследственностью.
Нехватка в организме витаминов группы В, а в особенности пиридоксина и цианокобаламина, крайне негативно воздействует на проводимость нервных и моторных волокон и может вызывать сенсорную аксональную полинейропатию нижних конечностей. Это же происходит при хронической алкогольной интоксикации, глистной инвазии, заболеваниях желудочно-кишечного тракта, которые ухудшают скорость всасывания.
Токсическое отравление лекарственными препаратами, аминогликозидами, золотыми солями и висмутом занимают большой процент в структуре факторов аксональной невропатии.
У пациентов с сахарным диабетом нарушена функция периферических нервов из-за нейротоксичности кетоновых тел, то есть метаболитов жирных кислот. Происходит это из-за невозможности организма использовать глюкозу как главный источник энергии. Поэтому вместо нее окисляются жиры.
При аутоиммунных заболеваниях, протекающих в организме, иммунная система человека атакует собственные нервные волокна, воспринимая их как источник опасности. Это происходит из-за провокации иммунитета, возникающей при неосторожном приеме иммуностимулирующих медикаментов и нетрадиционных методик лечения. Поэтому у людей, которые склонны к возникновению аутоиммунных заболеваний, пусковыми факторами аксональной полинейропатии являются:
- иммуностимуляторы;
- вакцины;
- аутогемотерапия.
При амилоидозе в организме накапливается такой белок, как амилоид. Именно он нарушает основные функции нервных волокон.
Первые признаки
Заболевание обычно начинает развиваться с поражения толстых или тонких нервных волокон. Зачастую аксональная полинейропатия имеет дистальное симметричное распределение на кисти или стопы. Нейропатия чаще всего сначала поражает нижние конечности, а затем симметрично распространяется вверх по телу. К самым частым первичным симптомам поражения относят:
- мышечную слабость;
- болевой синдром в конечностях;
- жжение;
- ощущение ползания мурашек;
- онемение кожных покровов.
Симптоматика ярче всего проявляется в вечернее и ночное время суток.
Симптомы
Врачи подразделяют хроническое, острое и подострое течение аксональной полинейропатии. Заболевание подразделяется на два вида: первично-аксональный и демиелинизирующий. В ходе течения болезни к ней присовокупляется демиелинизация, а затем и вторично аксональный компонент.
К основным проявлениям недуга относятся:
- вялость в мышцах ног или рук;
- спастический паралич конечностей;
- чувство подергивания в мышечных волокнах;
- головокружение при резкой перемене положения тела;
- отек конечностей;
- жжение;
- покалывание;
- ощущение ползания мурашек;
- снижение чувствительности кожных покровов к высокой или низкой температуре, боли и касаниям;
- нарушение ясности речи;
- проблемы с координацией.
Вегетативными признаками сенсомоторной полинейропатии асконального типа считаются следующие симптомы:
- учащенный или, напротив, замедленный сердечный ритм;
- неумеренное потоотделение;
- чрезмерная сухость кожи;
- изменение цвета кожных покровов;
- нарушение эякуляции;
- эректильная дисфункция;
- проблемы с мочеиспусканием;
- сбой двигательных функций желудочно-кишечного тракта;
- повышенное слюнотечение или, наоборот, сухость во рту;
- расстройство аккомодации глаза.
Заболевание проявляется в нарушениях функций поврежденных нервов. Именно периферические нервные волокна отвечают за двигательные функции мышечной ткани, чувствительность, а также оказывают вегетативное воздействие, то есть регулируют сосудистый тонус.
Для нарушения функции проводимости нервов характерны расстройства чувствительности, например:
- чувство ползания мурашек;
- гиперестезия, то есть увеличение чувствительности кожи к внешним раздражителям;
- гипестезия, то есть уменьшение чувствительности;
- отсутствие ощущения собственных конечностей.
Когда поражены вегетативные волокна, то из-под контроля выходит регуляция сосудистого тонуса. При аксонально-демиелинизирующей полинейропатии наступает сдавление капилляров, из-за чего ткани отекают. Нижние, а затем и верхние конечности из-за скапливания в них жидкости существенно увеличиваются в размерах. Так как при полинейропатии нижних конечностей основное количество крови накапливается именно в пораженных областях тела, то у пациента возникает стойкое головокружение при принятии вертикального положения. Из-за того, что пропадает трофическая функция, могут возникнуть эрозивно-язвенные поражения нижних конечностей.
Аксональная моторная полинейропатия проявляется в двигательных нарушениях верхних и нижних конечностей. Когда моторные волокна, отвечающие за движения рук и ног, повреждены, то наступает полный или частичный паралич мышц. Обездвиживание может проявляться совершенно нетипично — может ощущаться как скованность мышечных волокон, так и чрезмерная их расслабленность. При средней степени поражения ослаблен мышечный тонус.
В ходе течения заболевания могут быть усилены или ослаблены сухожильные и надкостничные рефлексы. В редких случаях доктор-невролог их не наблюдает. При болезни часто могут быть поражены черепные нервы, которые проявляются следующими нарушениями:
- глухотой;
- онемением подъязычных мышц и мускулатуры языка;
- невозможностью проглотить еду или жидкость из-за проблем с глотательным рефлексом.
Когда поражен тройничный, лицевой или глазодвигательный нерв, изменяется чувствительность кожных покровов, развиваются параличи, возникает асимметрия лица и подергивание мышц. Иногда при диагностированной аксонально-демиелинизирующей полинейропатии поражения верхних или нижних конечностей могут быть асимметричными. Такое случается при множественной мононейропатии, когда коленные, ахилловы и карпорадиальные рефлексы несимметричны.
Диагностика
Главной методикой исследования, которая позволяет обнаружить локализацию патологического процесса и степень пораженности нервов, является электронейромиография.
Чтобы определить причину заболевания, врачи назначают следующие анализы:
- определение уровня сахара в плазме крови;
- токсикологические тесты;
- полный анализ мочи и крови;
- выявление уровня холестерина в организме.
Нарушение нервных функций устанавливается при помощи определения температурной, вибрационной и тактильной чувствительности.
При первичном осмотре применяется зрительная методика исследования. То есть врач, к которому обратился с жалобами пострадавший, осматривает и анализирует такие внешние симптомы, как:
- уровень давления крови в верхних и нижних конечностях;
- чувствительность кожных покровов к прикосновениям и температуре;
- наличие всех необходимых рефлексов;
- диагностика отечности;
- изучение внешнего состояния кожи.
Выявить аксональную полинейропатию можно при помощи следующих инструментальных исследований:
- магнитная резонансная томография;
- биопсия нервных волокон;
- электронейромиография.
Лечение аксональной полинейропатии
Лечение аксональной полинейропатии должно быть комплексным и направленным на причину развития заболевания, его механизмы и симптоматику. Гарантией эффективной терапии является своевременное выявление болезни и лечение, которое сопровождается абсолютным отказом от сигарет, алкоголя и наркотических веществ, ведением здорового образа жизни и соблюдением всех рекомендаций врача. В первую очередь проводятся следующие терапевтические мероприятия:
- избавление от токсического воздействия на организм, если оно присутствует;
- антиоксидантная терапия;
- прием препаратов, которые воздействуют на тонус кровеносных сосудов;
- восполнение дефицита витаминов;
- регулярный контроль концентрации глюкозы в плазме крови.
Отдельное внимание уделяется лечению, направленному на купирование острого болевого синдрома.
Если присутствуют периферические парезы, то есть существенное снижение мышечной силы с многократным уменьшением амплитуды движений, то в обязательном порядке показана лечебная физкультура и специальные физические упражнения, направленные на возвращение тонуса мышечным тканям и предотвращение образования различных контрактур. Особенно важна регулярная психологическая поддержка, которая не дает пациенту впасть в депрессию, сопровождающуюся расстройством сна и чрезмерной нервной возбудимостью.
Лечение аксональной полинейропатии — это продолжительный процесс, так как нервные волокна восстанавливаются долго. Поэтому не стоит ожидать моментального выздоровления и возвращения к привычному образу жизни. Медикаментозная терапия включает такие препараты, как:
- обезболивающее;
- глюкокортикоиды;
- витамины группы В;
- антиоксиданты;
- сосудорасширяющие;
- средства, ускоряющие метаболизм и улучшающие микроциркуляцию крови.
Терапия лекарственными препаратами направлена на восстановление функций нервов, улучшение проводимости нервных волокон и скорости передачи сигналов центральной нервной системе.
Лечение следует проводить длительными курсами, которые не стоит прерывать, хоть и эффект от них проявляется не сразу. Чтобы устранить болевые ощущения и расстройство сна, назначают следующие медикаменты:
- антидепрессанты;
- противосудорожные;
- препараты, купирующие аритмию;
- обезболивающие.
Для избавления от боли используют нестероидные противовоспалительные препараты. Но стоит помнить, что применять их можно только короткий промежуток времени, так как длительное употребление может привести к повреждению слизистой оболочки желудочно-кишечного тракта.
К физиотерапевтическим методам лечения аксональной полинейропатии относятся:
- терапия магнитными волнами;
- грязелечение;
- электростимуляция;
- иглоукалывание;
- лечебный массаж;
- физкультура;
- ультрафонофорез;
- гальванотерапия.
Именно лечебная физкультура позволяет сохранить работоспособность мышечных тканей и поддерживать конечности в нужном положении. Регулярные занятия спортом вернут мышцам тонус, гибкость и увеличат амплитуду движений до нормальной.
Прогноз
Если заболевание обнаружено на ранней стадии и комплексно лечится квалифицированными специалистами, то прогноз для жизни и здоровья пациента более чем благоприятный. Стоит вести правильный образ жизни, рацион должен быть богат витаминами и минералами, необходимыми для правильного функционирования организма.
Если долгое время игнорировать болезнь и не предпринимать никаких действий, результат будет плачевным вплоть до полного паралича.
Профилактика
Пациент в обязательном порядке должен совершать профилактические мероприятия, которые помогут избежать рецидива или возникновения опасного заболевания. Они включают в себя обогащение рациона витаминами, регулярный контроль уровня сахара в крови, полный отказ от табакокурения, наркотических веществ и алкогольных напитков.
В целях профилактики болезни рекомендуется:
- носить удобную обувь, которая не пережимает стопу, ухудшая кровоток;
- регулярно осматривать обувь, чтобы избежать образования грибка;
- исключить пешие прогулки на длительные расстояния;
- не стоять долгое время на одном месте;
- мыть ноги прохладной водой или делать контрастные ванночки, что помогает улучшить циркуляцию крови в организме.
Пострадавшим в стадии ремиссии категорически запрещается принимать лекарственные препараты без согласования с лечащим врачом. Важно своевременно лечить воспалительные заболевания, соблюдать меры предосторожности при работе с токсическими веществами, которые оказывают пагубное воздействие на организм, регулярно выполнять лечебные физические упражнения.
Российский государственный медицинский университет;
НИИ цереброваскулярной патологии и инсульта, Москва
Аксональные полинейропатии: патогенез и лечение
Как цитировать:
Ковражкина Е.А. Аксональные полинейропатии: патогенез и лечение. Журнал неврологии и психиатрии им. С.С. Корсакова.
2013;113(6):22‑25.
Kovrazhkina EA. Axonal polyneuropathies: pathogenesis and treatment. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2013;113(6):22‑25. (In Russ.)

Полинейропатия (ПНП) — заболевание периферической нервной системы, развивающееся в результате диффузного поражения периферических нервов — их аксонов (аксональные полинейропатии), миелиновой оболочки (демиелинизирующие полинейропатии) либо тел нейронов (нейронопатии) [9]. В основе патогенеза полинейропатий аксонального типа лежит генерализованное повреждение осевых цилиндров периферических нервов.
Патогенез. Аксональная дегенерация (аксонопатия) — результат нарушения метаболизма нейрона вследствие недостаточной выработки энергии в митохондриях и/или нарушения аксонального транспорта. Миелиновая оболочка при аксонопатиях страдает вторично (вторичная демилинизация). Миелин может повреждаться в результате ишемии нервов (поражения vasa nevrorum), отложения токсичных для нерва веществ или иммунных комплексов в эндоневрии (что характерно, например, для сахарного диабета, особенно 1-го типа — с высокой гипергликемией и аутоиммунными нарушениями) [4]. Соответственно, среди причин аксонопатии периферических нервов указывают нарушения метаболизма, токсические влияния, ишемию нервных стволов, наследственную предрасположенность и аутоиммунные механизмы [5]. По этиологическому фактору подавляющее большинство аксональных ПНП составляют метаболические и токсические, среди которых первое место занимают диабетическая (до 50% среди пациентов с сахарным диабетом и до 90% поражений нервной системы при диабете [9, 12]) и алкогольная (до 50% среди больных алкоголизмом [2, 9]).
Причиной токсико-метаболических ПНП является экзо- и эндогенные интоксикации. Поступающие извне вещества или собственные его метаболиты, токсичные для периферических нервов, вызывают их повреждение. Тяжесть этого повреждения зависит от степени токсичности данного агента (выделяют острые метаболические ПНП, развивающиеся на фоне тяжелой общей интоксикации, например, ПНП при быстро нарастающих печеночной недостаточности или уремии, при отравлении фосфоорганическими веществами, мышьяком, свинцом, как нежелательный эффект лечения препаратами лития, цитостатиками), длительности его воздействия, собственных генетических особенностей метаболизма нервной ткани, немаловажную роль играет также аутоиммунный фактор [13].
Большинство часто встречающихся в клинике метаболических ПНП являются итогом длительного воздействия эндо- и экзогенного токсического агента (диабетическая, печеночная, уремическая, алкогольная, профессиональная, лекарственная). Результатом такой интоксикации является повреждение осевого цилиндра аксона. Клинически это проявляется не только нарушениями чувствительности и мышечной слабостью (что свойственно и для демиелинизирующих ПНП), но и мышечными гипотрофиями, выраженными трофическими нарушениями. Все эти признаки свидетельствуют о длительном страдании аксонов периферических нервов. При электронейромиографии (ЭНМГ) выявляется снижение (иногда — вплоть до полного отсутствия) амплитуды сенсорных потенциалов и М-ответов периферических нервов. У пациентов с ПНП аксонального типа зачастую в достаточной степени сохранены двигательные функции (отсутствуют выраженные парезы, больные сохраняют способность ходить, часто без дополнительной опоры), тогда как инвалидизирующими являются чувствительные (боли и парестезии) и трофические нарушения. Так, аксональная сенсомоторная ПНП является одним из важных патогенетических факторов развития синдрома диабетической стопы [3]. Аксональное повреждение нервов развивается медленно, исподволь, но при правильном лечении потенциально обратимо.
При массивном воздействии токсичного для периферической нервной системы агента, участии ишемического компонента (за счет страдания vasa nevrorum), аутоиммунных влияний развиваются ПНП аксонально-демиелинизирующего типа такие, например, как уремическая, свинцовая, амиодароновая, вызываемые воздействиями высокотоксичных для нервов веществами [9]. При наиболее распространенной диабетической ПНП, демиелинизирующий компонент максимально представлен при инсулинпотребном сахарном диабете (характеризующимся более высокой гипергликемией), а выраженность демиелинизации периферических нервов нарастает при резких повышениях уровня глюкозы крови [4, 7]. На представленность демиелинизирующего компонента при метаболических ПНП влияют наследственные факторы (генетически обусловленная миелинопатия, которая протекала бы субклинически без дополнительного воздействия токсического агента), аутоиммунное повреждение (например, миелинопатия более выражена при сахарном диабете 1-го типа, при котором иммунокомпетентные клетки повреждают ткань поджелудочной железы) [4, 14].
ПНП аксонально-демиелинизирующего типа протекают более тяжело, с выраженными парезами, сенситивной атаксией, нейропатическим болевым синдромом, но нередко, при своевременном устранении действия токсического фактора, быстро регрессируют. При очень тяжелом и упорном течении заболевания, учитывая роль аутоиммунного механизма в развитии данного типа метаболических ПНП, необходимо кратковременное назначение иммуномодулирующей терапии (чаще глюкокортикоидов, иногда цитостатиков) [9, 11].
Клиническое течение ПНП. Как уже было сказано, при длительном воздействии умеренно токсичного для нервов агента аксонопатия развивается медленно, что не всегда заметно. Преимущественное поражение бедно миелинизированых вегетативных и сенсорных волокон вызывает парестезии, повышенную холодовую чувствительность кистей и стоп, негрубые трофические нарушения. При ЭНМГ не всегда удается выявить характерные признаки сенсорной и моторной аксонопатии — снижение амплитуд сенсорных потенциалов и М-ответов — если исследуются крупные богато миелинизированные нервы, аксоны которых страдают позднее. Быстрее выявляются признаки вторичной миелинопатии, как клинические — присоединение нейропатических болей, парезов, так и миографические — снижение скорости распространения возбуждения (СРВ) по нервам.
При условии адекватной терапевтической стратегии — устранения действия повреждающего периферические нервы фактора, назначение препаратов, влияющих на метаболизм нервной ткани, — наступает ремиелинизация, что отражается и на ЭНМГ в виде нарастания СРВ, и клинически — в виде регресса парезов и нейропатических болей, улучшения чувствительности. Однако, если полинейропатия развивалась в условиях длительного действия токсического агента, поражение аксонов периферических нервов, снижение амплитуд сенсорных потенциалов и М-ответов на ЭНМГ сохраняется, поскольку осевые цилиндры нервов обладают гораздо меньшей способностью к регенерации, чем миелин.
Так, в проведенном исследовании [8], посвященном лечению алкогольной ПНП, ведущим ЭНМГ-признаком поражения периферических нервов у большинства пациентов имелось снижение СРВ. В условиях элиминации токсического фактора (в данном случае приема алкоголя) и лечения препаратом α-липоевой кислоты (берлитион в суточной дозе 600 мг), у пациентов быстро, в течение 1-го месяца, регрессировали ЭНМГ и клинические признаки миелинопатии — уменьшалась выраженность парезов и болевого синдрома (в баллах по визуальной аналоговой шкале с 5,2±1,0 до 2,6±0,5) достоверно (р<0,05) нарастала СРВ (по моторным волокнам n. tibialis с 36,93±1,12 до 42,22±0,8 м/с, по сенсорным волокнам n. suralis c 32,45±0,70 до 38,24±0,50 м/с), но признаки аксонопатии (снижение амплитуд сенсорных и моторных ответов периферических нервов, сенсорные выпадения по полиневритическому типу, трофические нарушения) сохранялись и после 6 нед лечения.
Таким образом, можно представить следующую схему развития и течения метаболических ПНП (см. таблицу): высокотоксичные, высококонцентрированные токсические агенты приводят к развитию полинейропатии аксонально-демиелинизирующего типа (в развитии которых также значительную роль играют наследственный, сосудистый, аутоиммунный факторы), длительно действующие эндо- и экзогенные яды приводят преимущественно к страданию аксонов с умеренно выраженным вторичным поражением миелина (так как постоянно идет процесс ремиелинизации) [7].
Лечение. Аксональное повреждение нервов как первичного, так и вторичного характера, обратимо за счет регенерации поврежденных аксонов и концевого спрутинга сохранившихся аксонов, однако этот процесс протекает медленно (месяцы), часто аксональная регенерация бывает неполной. Для регресса аксонопатии периферических нервов необходимо нивелировать воздействие токсического агента (коррекция метаболических и алиментарных нарушений, детоксикация, влияние на аутоиммунные механизмы), большое значение имеет также патогенетическая терапия, направленная на восстановление нарушенного метаболизма аксонов (митохондриальные нарушения, повреждения, вызванные окислительным стрессом).
Таким образом, в патогенетическом лечении аксональных ПНП, в зависимости от их нозологического и клинико-электрофизиологического варианта, должны присутствовать детоксикация и коррекция метаболических и алиментарных нарушений; сосудистая терапия (дезагреганты, венотоники, пентоксифиллин, вазопростан); препараты, воздействующие на универсальные механизмы поражения аксонов (витамины и витаминоподобные препараты); при необходимости — воздействие на аутоиммунные компоненты (глюкокортикоиды, плазмаферез). В некоторых случаях, когда представленность миелинопатии в структуре поражения периферических нервов велика и трудно отличить токсико-метаболическую полинейропатию от воспалительной (например, синдром Гийена-Барре у пациента с алкоголизмом или дебют хронической воспалительной демиелинизирующей ПНП у больного с сахарным диабетом) необходимо проводить пробную иммуномодулирующую терапию, ее быстрая эффективность позволит высказаться в пользу превалирования у пациента аутоиммуного механизма поражения периферических нервов [7, 11].
В лечении всех метаболических ПНП необходимо устранить (по возможности) поражающий периферические нервы яд и использовать препараты, улучшающие метаболизм нервной ткани периферических нервов. Последние необходимо применять в течение длительного времени, так как первым эффектом данных препаратов будет ускорение ремиелинизации, но для восстановления самих аксонов — а данные ПНП являются аксональными — требуется значительно большее количество времени.
α-липоевая (тиоктовая) кислота — витаминоподобное вещество, эндогенно образующееся в организме, как кофермент участвует в окислительном декарбоксилировании α-кетокислот. Основная функция эндогенной липоевой кислоты в организме — участие в аэробном метаболизме продукта гликолиза пирувата. Тиоктовая кислота является коферментом в окислительном декарбоксилировании пировиноградной кислоты до ацетил-КоА и α-кетоглутаровой до сукцинил-КоА в цикле Кребса. Облегчая превращение молочной кислоты в пировиноградную с последующим декарбоксилированием последней, α-липоевая способствует ликвидации метаболического ацидоза [6]. Тиоктовая кислота обладает сложным комплексным действием: гипогликемическим, липотропным, гепатопротекторным, антиатеросклеротическим, является мощным антиоксидантом. Липоевая кислота может существовать в окисленной (-S-S-) и восстановленной (SH-)-формах, благодаря чему реализуются ее коферментные и антиоксидантные функции. Восстановленная форма, дигидролипоевая кислота, служит донором электронов для восстановления других антиоксидантов (витамины С, Е и глутатион), осуществляет рецикл витамина Е при его истощении. Дигидролипоат повышает интра- и экстрацеллюлярный уровни глутатиона — эндогенного антиоксиданта.
Эффект экзогенно вводимой α-липоевой кислоты в отношении полиневритического синдрома впервые обнаружен при сахарном диабете. Обусловленная сахарным диабетом гипергликемия приводит к отложению глюкозы на матричных протеинах кровеносных сосудов и образованию конечных продуктов прогрессирующего гликозилирования, в результате чего уменьшается эндоневральный кровоток, возникает эндоневральная ишемия. α-липоевая кислота приводит к снижению уровня глюкозы в крови и повышению содержания гликогена в печени, обладает гипогликемическим действием. На фоне воздействия препарата уменьшается выраженность сенсорных симптомов полинейропатии — боли, жжения, ощущения онемения и «ползания мурашек» в конечностях.
Применение α-липоевой кислоты оказывает положительное влияние на универсальные механизмы аксонального повреждения, такие как повреждающее действие окислительного стресса и митохондриальная дисфункция — за счет антиоксидантного действия, повышения содержания глутатиона. Энергокорригирующее действие α-липоевой кислоты, тропное именно к аксонам нервов, способствует, в конечном итоге, быстрейшей регенерации аксонов [18].
Препарат не только редуцирует проявления окислительного стресса, но и оказывает влияние на сосудистый компонент поражения периферических нервов, нормализуя эндоневральный кровоток (что имеет большое значения, например, при дибетической микроангиопатии) [16, 17]. Комплексный механизм действия α-липоевой кислоты объясняет ее эффективность в отношении всех аксональных ПНП, патогенез которых связан с токсико-дисметаболическим и сосудистым факторами. Так, эффективность тиоктовой кислоты показана при уремической и алкогольной ПНП, при поражении периферических нервов, индуцированном цитостатиками [15]. Для регенерации аксонов периферических нервов на фоне токсико-метаболических влияний важны также детоксикационный и гепатопротекторный эффекты α-липоевой кислоты. Положительный эффект препарата отмечен в отношении заболеваний печени, печеночной комы, некоторых интоксикаций, в том числе алкогольной [6, 10].
При значительно выраженной аксонопатии, учитывая медленную скорость регенерации аксонов, необходимо длительное применение достаточно высоких доз α-липоевой кислоты. Обычно ее суточная доза составляет 600 мг. Предпочтительнее начинать лечение с внутривенного капельного введения препарата — 600 мг (24 мл раствора) в разведении на 200 мл физиологического раствора, длительность инфузии составляет от 2 до 4 нед в зависимости от тяжести ПНП. В особо тяжелых случаях препарат вводят внутривенно капельно в дозе 1200 мг в сутки. После переходят на пероральный прием α-липоевой кислоты — в таблетках по 600 мг не менее 2 месяцев [1].
В соответствии с такой клинической потребностью — необходимостью длительного приема достаточно высоких доз α-липоевой кислоты, учитывая потенциально обратимый, но медленный характер аксональной регенерации — разработаны и фармацевтические формы препарата. Например, берлитион 300 и берлитион 600, производимые в виде раствора для внутривенных вливаний по 12 и 24 мл соответственно (для начального этапа лечения ПНП), так и таблеток по 300 и 600 мг (для продолжения терапии).
Соблюдение всех условий патогенетического лечения ПНП — нормализация гликемии, прекращение поступления экзогенного яда, детоксикация, коррекция аутоиммунных нарушений, длительное применение препаратов, нормализующих аксональный метаболизм, способствует постепенной регенерации аксонов, уменьшению выраженности чувствительных и двигательных нарушений, болевого синдрома, парестезий, парезов. Для уточнения динамики различных видов метаболических ПНП на фоне подобного терапевтического подхода необходимы дальнейшие исследования.
Невролог
Cтаж — 17 лет
Кандидат наук
Медицинский центр «TERVE» на проспекте Красноярский рабочий
Лаборатория «Terve Lab»
Дата публикации 11 марта 2020Обновлено 4 августа 2021
Определение болезни. Причины заболевания
Невропатия, или нейропатия (Neuropathy) — повреждение одного или нескольких нервов периферической нервной системы. К ней относятся черепные и спинальные нервы, а также нервы и сплетения вегетативной нервной системы [2][3]. Невропатия проявляется нарушением чувствительности, болью в поражённом участке, судорогами, мышечной слабостью и затруднением движений. Выделяют две основные группы невропатий:
- мононевропатия — повреждение отдельного нерва, например срединного.
- полинейропатия — множественные повреждения нервов при диабетической полинейропатии, диффузной нейропатии, полирадикулопатии, плексопатии.
Распространённость нейропатии среди населения составляет 2-7 %. Риск развития заболевания увеличивается с возрастом: в 40 лет патология встречается в 15 % случаев [4][5][6].
Повреждение периферических нервов может вызывать множество причин. Даже после комплексного обследования выявить их удаётся не всегда. К основным факторам, приводящим к заболеванию, относят:
- Сахарный диабет — невропатией страдает более 70 % пациентов [22].
- Химиотерапия. При лечении токсичными препаратами патология развивается в 15-23 % случаев. Выраженность невропатии зависит от дозы препарата и продолжительности курса лечения [7].
- Васкулит (воспаление кровеносных сосудов). При повреждении отдельных нервов нейропатия бывает первым проявлением васкулита. Но может возникать и при комплексном поражении органов. При системном васкулите нейропатия поражает 60-70 % пациентов. Средний возраст — 58-62 года. Женщины заболевают чаще, чем мужчины [8].
- ВИЧ-инфекция. Распространённость нейропатии среди ВИЧ-инфицированных возросла с 13 % в 1993 году до 42 % в 2006 году. Вероятно, это связано с применяемыми антиретровирусными препаратами.
- Гепатит С. Как и в случае с ВИЧ, к нейропатии приводит приём токсичных для нервной ткани лекарств. Исследование, проведённое во Франции, выявило развитие сенсорной и моторной невропатии у 10 % больных гепатитом С.
- Поражение кишечника в 10 % случаев приводит к центральным и периферическим нарушениям нервной системы.
- Варикозное расширение вен нижних конечностей. Заболевание осложняется нейропатией из-за нарушения кровоснабжения нервной ткани.
- Хроническая почечная недостаточность — в 70 % случаев приводит к нейропатии.
- Ожирение [6][9][10][11][12][13].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы невропатии
Несмотря на то, что нейропатию вызывают различные причины, основные симптомы заболевания схожи [9][14][15][16][17]:
- Двигательные нарушения, слабость мышц. Пациент с трудом выполняет действия, связанные с мелкой моторикой, например застёгивание пуговиц. Возникают проблемы с ходьбой — больной может упасть из-за слабости мышц стопы.
- Сенсорные нарушения — онемение, повышенная тактильная чувствительность, резкая стреляющая боль, подобная удару электрическим током.
- Снижение и выпадение сухожильных рефлексов. Появляются трудности при выполнении повседневных действий, таких как надевание одежды, перемещение предметов.
- Расстройства сердечно-сосудистой системы. Выражается в нестабильности артериального давления и его снижении при резком вставании, проявляется головокружением и потемнением в глазах .
- Расстройства желудочно-кишечного тракта — запоры и кишечная непроходимость, вызванные ухудшением тонуса мышц кишечника.
- Боли в кистях и стопах.
- Нарушение равновесия и координации движений.
- Повышенная потливость.
- Задержка мочеиспускания.
- Сексуальная дисфункция.
При нейропатии могут поражаться не только нервы конечностей, но и черепно-мозговые нервы:
- невропатия зрительного нерва (оптическая нейропатия) приводит к нечёткости, затуманенности зрения, нарушению цветового восприятия, слепоте;
- поражение глазодвигательного нерва проявляется опущением верхнего века и параличом глазных мышц;
- патология отводящего нерва вызывает сходящееся косоглазие, опущение верхнего века, двоение в глазах;
- лицевого нерва — паралич мимических мышц;
- преддверно-улиткового (слухового нерва) — потерю слуха;
- языкоглоточного нерва — нарушение подвижности языка;
- гортанного нерва — дыхательную недостаточность [15].
На начальных стадиях двигательные расстройства могут не проявляться. Но в дальнейшем нейропатия значительно ограничивает физическую активность пациента [5][7][16][17].
Для повреждения периферической нервной системы характерны основные синдромы:
- Поражение переднего корешка спинного мозга — приводит к ослаблению или параличу мышц. Возможны судороги и подёргивания.
- Поражение заднего корешка спинного мозга — проявляется повышенной тактильной чувствительностью, жжением, нарушением спинальных рефлексов, болью в области поражения.
- Поражение межпозвоночного узла — вызывает жжение, покалывание, снижение болевого порога, интенсивные жгучие боли, обострение герпесвирусной инфекции.
- Поражение спинального нерва — приводит к расстройствам чувствительности и двигательным нарушениям.
- Поражение сплетения периферических нервов — вызывает боль, но менее интенсивную, чем при повреждении корешков [16].
Патогенез невропатии
К нейропатии могут приводить нарушения обмена веществ и иммунной системы, генетические факторы, инфекционное и токсическое воздействие [1].
Развитие заболевания при обменных нарушениях, например при сахарном диабете, вызвано чрезмерным накоплением глюкозы в клетке. Гипергликемия приводит к отложению в нервных клетках продукта обмена — сорбитола. Избыток сорбитола нарушает функции клеток периферических нервов. При этом уменьшается выработка мио-инозитола — соединения, влияющего на передачу сигналов в мозге и защиту нервных клеток от повреждения. Всё это приводит к ухудшению регенеративных способностей нервной ткани и снижению её проводимости [9].
В развитии нейропатии важная роль принадлежит митохондриям (органеллам, обеспечивающих клетку энергией). Они повреждаются при гипергликемии и приёме противоопухолевых препаратов: паклитаксела, бортезомиба, оксалиплатина. Эти лекарства влияют и на другие внутриклеточные структуры (например микротрубочки, поддерживающие форму клетки), негативно воздействуют на клеточные процессы и в результате активируют запрограммированную гибель нейронов [9][15][18]. Схожие нарушения возникают и у ВИЧ-инфицированных пациентов, принимающих антиретровирусные препараты [9][15].
Классификация и стадии развития невропатии
Попытки систематизировать различные виды нейропатии предпринимались многократно как отечественными, так и зарубежными авторами. Но ни одна из классификаций не удовлетворяет всем потребностям клиницистов. Это связано с тем, что к развитию заболевания приводит множество сложных и до конца не изученных факторов [16].
По одной из классификаций, нейропатии разделяют на следующие группы:[19]
I. Мононевропатии (поражение одного нерва).
- Травматические мононевропатии — возникают при травмах, ранениях, электротравмах, химических повреждениях.
- Туннельные синдромы — это ущемление нерва при длительном сдавлении и травматизации в костно-мышечных каналах. К ним относятся: синдром карпального канала (сдавление нерва в области запястья), пронаторный синдром (поражение нерва в плече), синдром кубитального канала (в локте), синдром тарзального канала (сдавление большеберцового нерва), синдром ложа Гийона (сдавление глубокой ветви локтевого нерва) и др.
II. Множественные нейропатии (поражение нескольких отдельных нервов).
- Моторная мультифокальная нейропатия с блоками проведения — аутоиммунное заболевание, проявляющееся слабостью мышц стоп и кистей.
- Моторно-сенсорная невропатия с блоками проведения — вызывает поражение не только моторных, но и сенсорных волокон.
- Множественная невропатия при васкулитах.
III. Полиневропатии (множественные поражения нервной ткани).
1. Наследственные полиневропатии: Шарко — Мари — Тута, синдром Руси — Леви, Дежерина — Сотта и др.
2. Приобретённые полиневропатии.
2.1. Аутоиммунные полиневропатии — возникают при сбое в работе иммунной системы (синдром Гийена — Барре, синдром Миллера — Фишера, хроническая воспалительная демиелинизирующая полинейропатия, парапротеинемические полиневропатии, паранеопластические полинейропатии).
2.2. Метаболические полинейропатии — диабетическая, уремическая, печёночная, при системных заболеваниях. Наиболее часто встречается диабетическая нейропатия.
2.2 Вызванные дефицитом витаминов В1, В6, В12.
2.3 Токсические полинейропатии — вызванная алкоголем, лекарствами, отравлением тяжёлыми металлами. Препараты, способные приводить к нейропатии:
- Оксалиплатин — крайне нейротоксичное средство. Развитие острой нейропатии возникает в 90 % случаев, а хронической — в 50 %. Приём оксалиплатина приводит к жжению, покалыванию, онемению рук, ног и области вокруг рта.
- Таксен (Палитаксел, Доцетаксел) — вызывает нарушение чувствительности, слабость и боль в мышцах, возможны редкие вегетативные симптомы.
- Препараты на основе алкалоидов барвинка (Винбластин, Винорелбин, Виндезин, Винкристин) — нарушают функции мочевого пузыря и кишечника, влияют на чувствительность в руках и ногах, ухудшают мелкую моторику, приводят к мышечной слабости и резкому снижению артериального давления.
- Бортезомиб — нарушает чувствительность, приводит к боли и вегетативным симптомам.
- Иммуномодулирующие препараты (Талидомид) — провоцирует сенсорные нарушения, преимущественно в нижних конечностях, лёгкие двигательные, желудочно-кишечные и сердечно-сосудистые расстройства [15][16][18].
2.4 Инфекционно-токсические — после гриппа, кори, дифтерии, мононуклеоза, поствакцинальные, при ВИЧ-инфекции, лепре.
IV. Поражения сплетений (шейного, верхнего плечевого, нижнего плечевого, пояснично-крестцового).
V. Вертеброгенные поражения нервных корешков (радикулиты).
Несмотря на многообразие причин, вызывающих полинейропатии, по участкам поражения их можно разделить на два вида:
- Аксональные — вовлечены нервы с наиболее длинными отростками (аксонами), к ним относится большинство токсических полинейропатий, аксональный тип наследственной моторно-сенсорной полинейропатии. Характеризуются мышечными атрофиями.
- Демиелинизирующие — вызваны разрушением миелиновой оболочки, окружающей отростки нервных клеток. Проявляются выпадением сухожильных рефлексов, развитием мышечной слабости без мышечных атрофий [19].
Осложнения невропатии
Зачастую нейропатия уже является осложнением какого-либо заболевания, например сахарного диабета. У некоторых пациентов, страдающих диабетом, может развиваться диабетическая амиотрофия — асимметричное поражение проксимальных (близких к туловищу) отделов ног с развитием болей и слабости в мышцах [16][17][19].
Если лечение не начато вовремя, нейропатия стремительно прогрессирует. В результате снижается тонус мускулатуры, наступает атрофия мышц и инвалидность. На фоне мышечной слабости случаются падения и травмы. Пациенты утрачивают способность ходить и обслуживать себя. Иногда последствиями полинейропатии становятся полный паралич конечностей или дыхательная недостаточность.
Диагностика невропатии
Неврологи используют различные шкалы для оценки тяжести нейропатии. Универсального опросника, соответствующего всем потребностям клиницистов, не существует. Это связано с различным прогнозом, проявлениями и причинами нейропатии [21].
Во время обследования оценивают проводимость нерва, учитывая временную динамику [17]. Для диагностики применяют следующие методы:
- Электромиография (ЭМГ) — регистрация электрической активности в мышце при её сокращении. Позволяет определить характер двигательных расстройств, уточняет степень разрушения нерва и выявляет заболевание до появления симптомов. ЭМГ позволяет провести дифференциальную диагностику невропатии с миастенией, миотонией, миоплегией, полимиозитом [16][17].
- Электронейромиография (ЭНМГ) — оценивает прохождение импульса по нервному волокну. ЭНМГ поможет не только выявить расположение поражённых участков, но и определить момент начала патологического процесса [17].
- УЗИ — распространённый метод визуализации периферических нервов. Ультразвук поможет выявить нарушения, которые незаметны при электродиагностике. Оценивается изменение диаметра нерва, непрерывность и ухудшение звукопроводимости. УЗИ позволяет обнаружить опухоли периферических нервов, травматические невромы, разрывы, воспаление, демиелинизирующие процессы.
- МРТ — визуализирует нервы и структуру мягких тканей, выявляет злокачественные опухоли и предоставляет информацию о мышечной атрофии и поражении нервов. МРТ выявляет повреждение нерва в областях, которые трудно исследовать при помощи электродиагностики или ультразвука.
Согласно статистике, УЗИ выявляет мононевропатии или плечевые плексопатии чаще, чем МРТ [20].
Лечение невропатии
Выбор методов лечения нейропатии зависит от вызвавших её причин:
- Метаболические нейропатии, в частности диабетическую нейропатию лечат препаратами альфа-липоевой кислоты. Перспективный препарат для терапии диабетических невропатий — канитин. Однако основное лечение при сахарном диабете заключается в контроле уровня глюкозы [6].
- При комплексной терапии применяют препараты с витаминами. Высокие дозы принимают не более месяца.
- При возникновении болевого синдрома используют противосудорожные препараты, трициклические антидепрессанты. Их противоболевое действие связано с блокированием болевого импульса в головном мозге и устранением болевой «памяти». К физическим методам воздействия относят магнитотерапию, лазеротерапию, электрофорез с прозерином, элетростимуляцию ослабленных мышц, иглотерапию [17][16].
- Для лечения хронической демиелинизирующей полирадикулониейропатии применяют иммуносупрессивные препараты. Иногда при терапии на первый план выходит уменьшение боли.
- При синдроме Гийена — Барре необходима госпитализация в многопрофильную больницу с отделением реанимации и интенсивной терапии, в тяжёлых случаях — вентиляция лёгких, мониторинг ЭКГ и артериального давления, введение гепарина для предупреждения тромбоза глубоких вен и лёгочной эмболии. При выраженных болях вводят опиоидные анальгетики, антиконвульсанты, проводят лечебную физкультуру, организуют рациональное (зондовое) питание. Патогенетическая терапия включает использование плазмафереза, введение иммуноглобулинов, кортикостероидную терапию. При синдроме Гийена — Барре иммунотерапия ускоряет выздоровление, но не влияет на окончательный прогноз [16][17].
- Для достижения долгосрочной ремиссии при системном васкулите, не связанном с вирусами, применяют кортикостероиды и циклофосфамид. Продолжительность терапии кортикостероидами может быть более двух лет [1][17].
- Лечение нейропатий, вызванных приёмом противоопухолевых препаратов, является сложной задачей. Общепризнанной профилактической или лечебной стратегии до сих пор не существует [15][18].
Прогноз. Профилактика
Невропатия зачастую развивается достаточно медленно. Пациенты сообщают о неврологических проявлениях врачу спустя годы после её формирования. О симптомах симметричной полинейропатии лечащий врач узнаёт в среднем через 39 месяцев. В таком случае лечение может быть запоздалым, а повреждение нерва необратимым [5].
При синдроме Гийена — Барре прогноз ухудшают пожилой возраст, быстрое развитие заболевания, потеря аксонов. Восстановление может занять несколько месяцев и быть неполным. Приблизительно у 15 % пациентов с синдромом Гийена — Барре сохраняются остаточные параличи [16][17].
Васкулитная нейропатия развивается с разной скоростью. Заболевание может протекать как в прогрессирующей хронической форме, так и в рецидивирующей с длительными периодами ремиссии.
Прогноз при сахарном диабете зависит от поддержания оптимального уровня сахара в крови. Приверженность лечению позволяют замедлить развитие нейропатии.
Прогноз после травмы периферической нервной системы плохой. При повреждении эндоневральной трубки (внешнего слоя соединительной ткани, окружающей периферические нервы) пациенты редко восстанавливаются полностью [17].
После терапии противоопухолевыми средствами нейропатия может сохраняться несколько лет [18]. Обратимость патологии остаётся под вопросом, особенно при приёме противораковых препаратов на основе платины и таксанов. Для уменьшения тяжести симптомов онкологи могут снизить дозировку или прекратить применение нейротоксических противоопухолевых препаратов [15][18].
Не все нейропатии можно предотвратить. Однако часть нарушений возможно избежать или отсрочить их появление на несколько лет. Это в первую очередь относится к эндокринным нейропатиям, например диабетической, и нейропатии, вызванной дефицитом витаминов в организме.
Периферическая нейропатия (нейропатия нерва) обозначает повреждение периферической нервной системы, обширной системы коммуникативных нервных волокон, передающей информацию от головного и спинного мозга к любой части тела. Периферические нервы также посылают сенсорную информацию обратно в головной и спинной мозг, информируя о наличии воздействий на ткани (простуда или ожог). При повреждении периферической нервной системы нарушаются эти жизненно важные связи.
Это можно сравнить с нарушением связи на телефонной станции, когда связь между станцией и абонентами нарушается (аналогичные прерывание связи происходит между мозгом и частями тела). Поскольку у каждого периферического нерва есть своя узкоспециализированная функция в определенной части тела, при повреждении нерва может быть различная симптоматика. У некоторых это может проявляться онемением, покалыванием, избыточной чувствительностью к прикосновению (парестезия), или слабостью мышцы. У других могут быть более выраженные симптомы, включая острую боль (особенно ночью), гипотрофия мышцы, паралич, или дисфункция железистой ткани или органа. Люди могут испытывать неспособность нормального переваривания пищи поддержания нормального АД потливость нарушения репродуктивных функций. В наиболее тяжелых случаях могут быть нарушения функции дыхания или органная недостаточность. При некоторых формах невропатии происходит повреждение только одного нерва, и называются эти повреждения мононейропатиями. При поражении большого числа нервов оказывающих влияние на конечности такие повреждении называют полинейропатиями. Иногда бывают поражения двух или более отдельных нервов в определенных областях тела это называют мультифокальным мононевритом. При острых невропатиях, таких как синдром Гийена-Барре, симптомы появляются внезапно , происходит быстрое прогрессирование и восстановление функций происходит медленно так как возникают повреждения нервных волокон. При хронических формах невропатии симптомы появляются постепенно и медленно прогрессируют. У некоторых пациентов периоды ремиссии сменяются периодами обострений. У других состояние может достичь определенного плато, при котором симптомы сохраняются неизменными в течение многих месяцев или лет. Некоторые хронические невропатии прогрессируют в течение долгого времени, но очень немного форм оказываются смертельными, если нет осложнений связанных с другими заболеваниями. Нередко невропатия — симптом другого заболевания.
При наиболее распространенных формах полинейропатии, нервные волокна наиболее удаленные от мозга начинают дисфункционировать в первую очередь. Боль и другие симптомы часто появляются симметрично, например, в обеих ногах, сопровождаемых постепенным прогрессией в обеих ногах. Иногда повреждаются пальцы рук и руки с прогрессированием выше к середине тела. У многих пациентов с диабетической нейропатией- именно такая форма прогрессирования и повреждения нервов.
Классификация периферических невропатий
Существует более 100 типов периферической невропатии, которые были идентифицированы, каждый с характерным симптомокомплексом структурой развития, и прогнозом. Нарушенная функция и симптомы зависят от типа нервов, которые подверглись повреждению (моторные, сенсорные, или вегетативные). Двигательные нервы управляют движениями всех мышц под контролем сознания, такими как ходьба, хватание или речь. Сенсорные нервы передают информацию о процессах восприятия, таких как тактильное чувство или боль вследствие пореза. Пучки вегетативных нервных волокон регулируют биологические действия, которыми выполняются без сознательно, такие как дыхание, переваривание пищи, деятельность сердца или желез секреции. Хотя некоторые невропатии могут оказать влияние на все три типа нервов, чаще всего происходит нарушение функции одного или двух типов нервов. Поэтому, врачи могут использовать термин, такой как преобладающе моторная невропатия, преимущественно сенсорная невропатия, сенсорно-моторная невропатия, или автономная невропатия.
Симптомы и причины
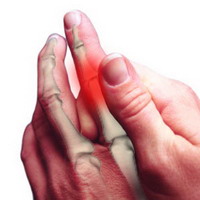
Сенсорное повреждение нервов вызывает более широкий диапазон симптомов, потому что у сенсорных нервов существует целая группа узкоспециализированных функций. Большие сенсорные волокна окружены миелиновой оболочкой и регистрируют вибрацию тактильные ощущения и проприорецепцию. Повреждение больших сенсорных волокон снижает способность чувствовать колебания и прикосновение что в результате дает онемение, особенно в руках и ногах. Люди могут чувствовать ощущения надетых перчаток или чулков. Многие пациенты не различают по прикосновению размер предмета или его форму. Это повреждение сенсорных волокон может способствовать потере рефлексов (также как и при повреждении моторных нервов). Потеря проприорецепции (чувство положения тела в пространстве) усложняет возможность координировать сложные движения или устойчивость с закрытыми глазами. Невропатической болью трудно поддается лечению и может оказывать серьезное влияние на эмоциональное состояние и общее качество жизни. Невропатическая боль часто усиливается ночью, серьезно нарушая сон, что еще больше ведет к эмоциональному дискомфорту.
Меньшие сенсорные волокна без миелиновых оболочек передают боль и температурные ощущения. Повреждение этих волокон может нарушить в способность чувствовать боль или изменения в температуре. Люди могут быть не в состоянии ощутить ранение от пореза или нагноение раны. Другие пациенты, возможно, не чувствуют боли, которая является предупреждающим сигналом при угрожающим жизни сердечном приступе или других острых состояниях. Потеря ощущения боли — особенно серьёзная проблема у пациентов с диабетом, что способствует высокой частоте ампутаций нижней конечности среди этой группы населения. Болевые рецепторы в коже могут также стать сверхчувствительными, так, что пациенты чувствуют сильную боль (allodynia) от воздействий, которые обычно являются безболезненными (например, при проведении тканью по коже или легком касании).
Симптомы повреждения пучков вегетативных нервных волокон разнообразны и зависят от органа иннервируемого ими. Дисфункция вегетативных нервных волокон может быть опасной для жизни и иногда требует экстренной медицинской помощи, особенно когда нарушается дыхание или частота сердцебиения. Общие симптомы повреждения пучков вегетативных нервных волокон включают нарушение потоотделения, которое необходимо при перегревании, нарушение функции мочеотделения которое может привести к недержанию мочи или инфекции мочевого пузыря; и нарушение управления мышцами, отвечающими за сокращениями кровеносных сосудов, что может влиять на поддержание нормального артериального давления. Потеря контроля над кровяным давлением может вызвать головокружение, тошноту, или даже обморок, когда человек внезапно падает при перемене положения тела (состояние известное как постуральная или ортостатическая гипотензия).
Желудочно-кишечные симптомы часто сопровождают вегетативную невропатию. Нервы, управляющие сокращениями мышц кишечника работают со сбоями, приводя к диарее, запору. У многих пациентов возникают также проблемы, связанные с глотанием при повреждении соответствующих нервных волокон.
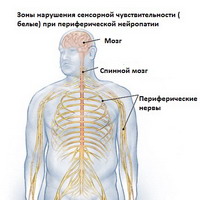
Травматическое повреждение является наиболее распространенной причиной повреждения нерва. Ранение или бытовая травма, от автокатастроф, падений, или связанных с занятиями спортом может привести к разволокнению нервов компрессии нервов растяжению или полному отрыву от спинного мозга. Даже не очень сильные травмы также могут вызвать серьезное повреждение нервов. Сломанные или вывихнувшиеся кости могут оказывать повреждающее давление на соседние нервы, и также при грыжах диска может возникать компрессия нервных корешков.
Системные заболевания — состояния, которые оказывают влияние на все тело и нередко вызывают периферическую невропатию. Эти состояния могут включать: метаболические и эндокринные нарушения. Ткани нерва очень чувствительности к изменениям метаболизма тканей процессам регенерации, которые могут изменяться при системных заболеваниях. Сахарный диабет, характеризующийся хронически высокими уровнями глюкозы в крови, является главной причиной периферической невропатии в некоторых странах (США). Приблизительно у 60 — 70% пациентов с диабетом имеются как умеренные, так и тяжелые формы повреждения нервной системы. Заболевания почек могут привести к избытку токсических веществ в крови, что может серьезно повреждать ткань нервов. У большинства пациентов, с необходимостью диализа из-за почечной недостаточности, развивается полинейропатия. Некоторые заболевания печени также приводит к невропатиям в результате нарушения обмена веществ.
Гормональные дисбалансы могут изменить нормальные метаболические процессы и вызвать невропатии. Например, недостаток гормонов щитовидной железы замедляет метаболизм, приводя к задержке жидкости и отеку тканей, которые могут оказывать давление на периферические нервы. Избыточная выработка соматотропина может привести к акромегалии, состояние, характеризующееся патологическим увеличением многих частей скелета, включая суставы. Нервы, снабжающие эти измененные суставы, часто тоже повреждаются.
Дефициты витамина и хронический алкоголизм могут вызвать необратимые повреждения тканей нерва. Витамины. Витамины Е, B1, B6, B12, и никотиновая кислота очень важны для нормальной функции нервов. Дефицит тиамина, в частности распространен у людей с хроническим алкоголизмом, потому что у этих людей нарушено поступление тиамина с пищей. Дефицит тиамина может вызвать достаточно болезненную невропатию конечностей. Некоторые исследователи полагают, что чрезмерное употребление алкоголя может, само по себе, способствовать непосредственному повреждению нервов, что называются алкогольной невропатией. Сосудистые заболевания и болезни крови могут уменьшить доставку кислорода к периферическим нервам и быстро привести к серьезному повреждению или гибели тканей нерва (к примеру, острая гипоксия мозга приводит к инсульту). Диабет часто приводит к сужению кровеносного сосуда. Различные формы васкулита часто приводят к утолщению стенки сосуда и уменьшения диаметра сосудов за счет рубцовой ткани. Эту категорию повреждения нервов, в котором повреждены изолированные нервы в различных областях, называют мультифокальная мононевропатией.
Заболевания соединительной ткани и хроническое воспаление могут вызвать прямое или косвенное повреждение нервов. Когда окружающие нервы слои тканей находятся в длительном воспалительном процессе, то воспаление может затронуть и непосредственно волокна нерва. Хроническое воспаление также приводит к прогрессивной деструкции соединительной ткани, подвергая волокна нерва, большему риску компрессии и инфицирования. Суставы при воспалении могут отекать и вовлекать нервы, причиняя боль.
Рак и доброкачественные опухоли могут прорастать и оказывать деструктивное действие на нервы. Опухоли также могут образоваться непосредственно из клеток ткани нерва. Достаточно нередко полинейропатия связана с нейрофиброматозом, генетическим заболеваниям, при котором происходит образование множественных доброкачественных опухолей из тканей нерва. Формирование невромы может быть одним элементом из регионального болевого синдрома или синдромом симпатической рефлекторной дистрофии, который может быть вызван травматическими причинами или хирургической травмой. Паранеопластический синдром, группа редких дегенеративных нарушений, которые вызваны реакцией иммунной системы человека на злокачественную опухоль, также может косвенно вызвать множественное повреждение нервов. Повторное стрессовое воздействие часто приводит к компрессионным невропатиям. Кумулятивное повреждение может появиться вследствие повторных чрезмерных движений, которые требуют сгибания любой группы суставов в течение длительного периода времени. В результате таких движений может возникнуть воспаление и отек сухожилия и мышц что может привести к сужению каналов через которые проходят некоторые нервы. Такие повреждения нередки во время беременности, вероятно, потому что увеличение веса и задержка жидкости также сужают каналы нервов.
Токсические вещества могут также вызвать повреждение периферических нервов. У люди, которые подверглись воздействию тяжелых металлов (мышьяк, свинец, ртуть, таллий), производственных токсинов, или экологических токсинов часто развиваются невропатии. У определенных препаратов для лечения от рака, противосудорожных препаратов, противовирусных средств, антибиотиков есть побочные эффекты, которые могут включать повреждение периферических нервов, что иногда является протипоказанием для их длительного применения.
Инфекции и аутоиммунные нарушения могут вызвать периферическую невропатию. Вирусы и бактерии, которые могут воздействовать на ткани нерва, включают опоясывающий лишай, вирус Эпштейн-Барра, вирус цитомегалии, и другие разновидности вирусов герпеса. Эти вирусы избирательно повреждают сенсорные нервы, вызывая приступообразные острые боли. Постгерпетическая невралгия часто встречается после эпизода опоясывающего лишая и может быть очень болезненной.
Вирус иммунодефицита человека (ВИЧ), также вызывает значительное повреждение в центральной и периферической нервной системе. Вирус может вызвать несколько различных форм невропатии, каждая из которых четко связана с определенной стадией иммунодефицита. Быстро прогрессирующая, болезненная полинейропатия, с вовлечением рук и ног, часто является первым клиническим симптомом ВИЧ-инфекции.
Болезнь Лайма, дифтерия, и лепра — бактериальные заболевания, характеризующиеся обширным повреждением периферических нервов. Дифтерия и лепра теперь встречаются достаточно редко, но болезнь Лайма стала встречаться чаще. Болезнь Лайма может вызвать широкий диапазон невропатических нарушений, включая быстрое развитие, болезненной полиневропатии, часто в течение нескольких недель после начального инфицирования во время укуса клеща.
Вирусные и бактериальные инфекции могут также вызвать вторичное повреждение нервов, способствую возникновению вызывая аутоиммунных нарушений, при которых происходит агрессия иммунной системы против собственных тканей. Аутоиммунные процессы, как правило, вызывают деструкцию миелиновых оболочек нервов или аксонов (волокон нерва).
Некоторые невропатии вызваны воспалением, следующим из реакции иммунной системы, а не от прямого повреждения инфекционными агентами. Воспалительные невропатии могут развиваться быстро или медленно, и хронические формы могут иметь периоды как ремиссии, так и рецидива. Острая воспалительная демиелинизирующая полинейропатия, известная как синдром Гийена-Барре, может повредить моторные, сенсорные волокна, и пучки вегетативных нервных волокон. Большинство людей выздоравливает после развития от этого синдрома, но иногда бывают тяжелые формы представляющие угрозу для жизни, хотя тяжелые случаи могут быть опасными для жизни. Мультифокальная моторная невропатия — форма воспалительной невропатии, которая проявляется повреждение исключительно моторных нейронов (может быть как острой, так и хронической).
Наследственные формы периферической невропатии вызваны врожденными сбоями в генетическом коде или мутациями. Некоторые генетические аномалии приводят к умеренным невропатиям с симптомами, которые начинаются в подростков возрасте и потом со временем симптоматика нивелируется. Более тяжелые наследственные невропатии часто появляются в грудном возрасте или в детстве. Наиболее распространенной наследственной невропатией является болезнь Шарот — Мари — Тусс. Эти невропатии возникают из-за нарушения в генах, ответственных за формирование нейронов или миелиновое оболочек. Признаки типичной болезни Шарлот_Мари-Тусс включают чрезвычайное ослабление мышц голени и стопы расстройства походки исчезновения сухожильных рефлексов и онемение в нижних конечностях.
Диагностика
Диагностирование периферической невропатии подчас бывает трудным, в связи с вариабельностью симптомов. Нередко требуется полное неврологическое обследование, включая: симптомы пациента, профессию, социальные привычки, наличие любых токсинов, наличие хронического алкоголизма, возможность наличия ВИЧ или другой инфекционной болезни, и наличие в анамнезе родственников с невропатией, проведение анализов, которые могут идентифицировать причину невропатии, и проведение обследований позволяющих определить степень и тип повреждения нервов.
Общее обследование тесты и анализы могут выявить наличие повреждения нервов вследствие системного заболевания. Анализы крови могут диагностировать диабет, дефицит витаминов, печеночную или почечную недостаточность, другие нарушения обмена веществ, и признаки патологической активности иммунной системы. Экспертиза цереброспинальной жидкости, которая циркулирует в головном и спинном мозге, может выявить патологические антитела, связанные с невропатией. Более узкоспециализированные анализы могут выявить болезни крови или сердечнососудистые заболевания, заболевания соединительных тканей, или злокачественные образования. Тесты на мышечную силу выявление признаком судорожной активности мышц или фасцикуляций могут указывать на повреждение моторных нейронов. Оценка способности пациента восприятия вибрации, мягкого прикосновения, положение тела (проприорецепция), температурную и болевую чувствительность помогает определить повреждение сенсорных волокон как больших, так и малых сенсорных волокон. На основе результатов неврологического осмотра, физического осмотра, подробной истории заболевания может быть назначены дополнительные тесты и обследования для уточнения диагноза.
Компьютерная томография, является атравматичным, безболезненным исследованием, которое дает возможность визуализировать органы костные мягкие ткани. Компьютерной томографии может выявить костные или сосудистые изменения опухоли головного мозга кисты грыжи межпозвоночного диска, энцефалит, спинальный стеноз (сужение спинномозгового канала), и другие нарушения.
Магнитно-резонансная томография (ЯМР или МРТ) может исследовать состояние мышцы ее размер, выявить замену ткани мышцы жировой тканью, и определить, было ли компрессионное воздействие на нервное волокно. Аппараты МРТ создают сильное магнитное поле вокруг тела. Радиоволны проходят через тело и вызывают резонанс, который может быть фиксирован под различными углами в пределах тела. Компьютер обрабатывает этот резонансный эффект и преобразует в трехмерное изображение.
Электромиография (ЭМГ) представляет собой введение тонкой иглы в мышцу для измерения электрической активности мышцы в покое и при сокращении. Анализы ЭМГ могут помочь дифференцировать повреждение самой мышцы и нервных волокон. Скорость проведения импульса по нерву может точно определить степень повреждения в больших нервных волокнах, четко указывая связаны симптомы с дегенерацией миелиновой оболочки или аксона. Во время этого исследование производится электрическая стимуляция волокна, в ответ на которое в нерве возникает ответный импульс. Электрод, помещенный дальше по ходу нерва, измеряет скорость передачи импульса вдоль аксона. Медленная скорость передачи и блокировка импульса, как правило, указывают на повреждение миелиновой оболочки, в то время как снижение уровня импульсов — признак аксональной дегенерации.
Биопсия нерва представляет собой удаление и исследование образца ткани нерва, чаще всего в голени. Хотя этот анализ может давать ценную информацию о степени повреждения нервов, это — инвазивная процедура, достаточно трудная в выполнение и сама вызывающая повреждение нерва и появление признаков невропатии. В большинстве случае эта процедура не показана для диагностики и может самостоятельно вызвать нейропатические побочные эффекты.
Биопсия кожи — анализ, при котором удаляют маленький кусочек кожи и исследуют окончания нервных волокон. Этот метод диагностики имеет преимущества перед ЭМГ и биопсией нерва, когда необходимо диагностировать повреждение в меньших сенсорных волокнах. Кроме того в отличие от обычной биопсии нерва, биопсия кожи менее инвазивна, имеет меньше побочных эффектов, и легче выполняется.
Лечение
Методов лечения наследственных периферических невропатий не существует. Однако есть методы лечения для многих других форм. Вначале проводится лечение причины заболевания и проводится симптоматическое лечение. У периферических нервов есть способность регенерировать, в том случае если сохранена сама нервная клетка. Симптоматику можно нивелировать, и устранение причин определенных форм невропатии часто может предотвратить повторное повреждение.
В общем, если вести здоровый образ жизни — как поддержание оптимального веса, исключение попадание токсинов в организм, правильное питание с наличием достаточного количества витаминов ограничение или исключение приема алкоголя — могут уменьшить физические и эмоциональные эффекты периферической невропатии. Активные и пассивные физические нагрузки могут уменьшить судороги, улучшить эластичность и силу мышц, и предотвратить атрофию мышц в парализованных конечностях. Различные диеты могут улучшить желудочно-кишечные симптомы. Своевременное лечение при травмах может помочь предотвратить необратимые изменения. Бросание курение особенно важно, потому что при курении происходит спазм кровеносных сосудов, которые доставляют питательные вещества в периферические нервы и могут ухудшить симптомы невропатии. Навыки хорошего ухода, такие как тщательный уход, за ногами и ранами при диабете необходимы, потому что у этих пациентов снижена болевая чувствительность. Хороший уход позволяет облегчить симптомы и улучшить качество жизни и стимулировать регенерацию нерва.
Системные заболевания часто требуют более комплексного лечения. Строгий контроль над уровнем глюкозы в крови, как показали исследования, уменьшает нейропатические симптомы и помогает пациентам с диабетической невропатией избежать дальнейшего повреждения нервов. Воспалительные и аутоиммунные заболевания, приводящие к невропатии, можно лечить несколькими способами. Иммунодепрессанты, такие как преднизон, циклоспорин, или имуран могут быть очень эффективными. Процедура плазмофереза, при которой происходит очистка крови от иммунных клеток и антител, может уменьшить воспаление или подавить активность иммунной системы. Большие дозы иммуноглобулинов, которые функционируют как антитела, также могут подавить патологическую активность иммунной системы. Но невропатическая боль трудно поддается лечению. Умеренная боль может иногда облегчаться анальгезирующими средствами. Некоторые препараты (применяемые для лечения других заболеваний) оказались полезными для многих пациентов, страдающих от тяжелых форм хронической невропатической боли. Они включают Мексилитин, лекарство, созданное для лечения нарушения сердечного ритма (но иногда вызывающее выраженные побочные действия); некоторые противоэпилептические средства, включая габапентин, фенитоин, и карбамазепин; и некоторые виды антидепрессантов, включая трициклические, такие как амитриптилин. Инъекции местных анестетиков, таких как лидокаин или использование пластырей, содержащие лидокаин, могут облегчить сильную боль. В самых тяжелых случаях болей можно хирургически разрушить нервы; однако, результаты являются подчас временными, и процедура может привести к осложнениям.
Ортопедические изделия могут помочь уменьшить боль и уменьшить воздействие физической инвалидности. Различные ортезы для руки или ноги могут компенсировать слабость мышцы или уменьшить компрессию нерва. Ортопедическая обувь может улучшить нарушения походки, и помочь предотвратить травмы стопы у людей со снижением восприятия боли.
Хирургическое вмешательство часто может обеспечить непосредственное облегчение при мононейропатиях, вызванных ущемлением нерва или компрессией. Удаление грыжи диска вызывает декомпрессию корешка. При удалении опухолей тоже уменьшается воздействие опухолевой ткани на нервы. Кроме того, декомпрессия нерва может быть достигнута с помощью релизинга связок и сухожилий.
В современной русскоязычной научно-медицинской литературе невропатиями принято называть заболевания нервной системы с преимущественным поражением периферических нервов. Традиционно выделяют мононевропатии, обусловленные вовлечением одного из периферических нервов и проявляющиеся клиническими симптомами и признаками, строго соответствующими известным зонам иннервации. Формы, обусловленные множественным (системным) поражением периферических нервов, называют полиневропатиями (ПНП) [1].
Термин «нейропатия» обычно используют как синоним «невропатии», однако некоторые зарубежные авторы подразумевают под нейропатией не только вовлечение аксонов и миелиновой оболочки периферических нервов, но и нейронов, что, на наш взгляд, не корректно (поражение нейронов в классической невропатологии принято называть нейронопатией).
Согласно данным европейских регистров, общая распространенность периферических невропатий в популяциях составляет в среднем 2400 × 10-5, а среди лиц пожилого возраста достигает 8000 × 10-5. Первичная заболеваемость невропатиями обычно не превышает 40 × 10-5 в год [3]. В России диагноз полиневропатии регистрируют не менее чем у 60% пациентов с признаками поражения периферической нервной системы [4].
В МКБ-10 мононевропатии относят к рубрикам G50-G53, G56-G59, полиневропатии — к рубрикам G60 (наследственные и идиопатические), G63 (воспалительные) и G63 (другие) [5], что очевидно не отражает многообразия форм и причин развития этой патологии.
В настоящее время отсутствует единая и удобная клиническая классификация ПНП.
По характеру клинической картины выделяют моторные, сенсорные, вегетативные и смешанные формы ПНП.
В зависимости от течения заболевания ПНП классифицируют на острые, подострые и хронические.
Согласно электронейромиографии (ЭНМГ) различают: 1) аксональные, характеризующиеся снижением амплитуды М-ответа при нормальной или незначительно сниженной скорости проведения импульса (СПИ) по нервам; 2) демиелинизирующие, характеризующиеся снижением СПИ по моторным и/или сенсорным волокнам; 3) смешанные (аксонально-демиелинизирующие) ПНП.
В соответствии с этиологией выделяют идиопатические ПНП, значительная часть которых генетически детерминирована, этиология других форм остается неизвестной.
Для обозначения ПНП, являющихся проявлением или осложнением других известных медицине заболеваний (инфекционные, эндокринные, онкологические заболевания, диффузные болезни соединительной ткани (ДБСТ), экзогенные интоксикации, заболевания внутренних органов и др.), не существует единого термина, однако по сути они являются вторичными (симптоматическими). Именно эта патология периферической нервной системы является одним из наиболее частых поводов обращения пациентов к врачам различных специальностей.
В зарубежной литературе используют понятие «болевые невропатии» и активно рассматривают проблемы купирования нейропатической боли [2]. Однако надо иметь в виду, что, с одной стороны, любое поражение периферических нервов так или иначе проявляется или сопровождается болью (для одних форм боль — обязательное проявление и критерий диагностики, для других — осложнение, вызванное прогрессированием заболевания с развитием мышечно-тонических нарушений, контрактур, деформаций скелета и др.), с другой стороны, не всегда боль (в силу указанных выше причин) при невропатии является нейропатической.
Согласно классическим канонам невропатологии, ПНП характеризуются наличием нарушений чувствительности по полинейропатическому типу и болевым синдромом, преимущественно выраженными в дистальных отделах конечностей; слабости мышц, ограничения амплитуды движений в конечностях и двигательной активности в целом (в т. ч. нарушением ходьбы), сопровождающихся атрофией и гипотонией мышц, угасанием сухожильных и периостальных рефлексов, а также вегетативных нарушений. Одними из ключевых критериев, позволяющих диагностировать ПНП, является преимущественное поражение дистальных отделов конечностей и относительная симметричность патологического процесса.
Диагностика ПНП как синдрома (топическая) обычно не вызывает значительных клинических сложностей, однако нередко возникают затруднения при определении этиологии и нозологической принадлежности ПНП. Так, даже при тщательном (в т. ч. нейрофизиологическом) обследовании в специализированных европейских клиниках причина ПНП остается не установленной примерно в 25% случаев, а в медицинских учреждениях общего профиля затруднения в определении нозологического диагноза возникают при обследовании 50% больных [6, 7].
В силу вариабельности клинических проявлений ПНП, в перечень для дифференциальной диагностики приходится включать значительное число других нервно-мышечных заболеваний, таких как радикулопатия, миастения, нейронопатия и другие. Особые трудности возникают при обследовании лиц пожилого возраста, поскольку более 90% из них страдают коморбидной патологией, такой как сахарный диабет, заболевания щитовидной железы и онкологические заболевания. Не меньшие сложности испытывают доктора в процессе лечения ВИЧ-инфицированных лиц, страдающих оппортунистическими заболеваниями.
В настоящее время известно не менее 200 причин развития ПНП, среди которых интоксикации (воздействие промышленных токсинов и солей тяжелых металлов, употребление наркотических препаратов и злоупотребление алкоголем), инфекции (вирусные, такие как ВИЧ, и бактериальные, такие как бруцеллез), системные заболевания соединительной ткани, дефицит витаминов, особенно группы В (В6, В12), злокачественные новообразования (лейкозы, лимфогранулематоз и др.), эндокринные заболевания (заболевания щитовидной железы, сахарный диабет и др.), ятрогенное воздействие лекарственных препаратов (антибактериальных, в т. ч. противотуберкулезных, и антиретровирусных препаратов, антиаритмических и гиполипидемических средств и др.), сывороток и вакцин [8].
Боль является одной из наиболее частых причин обращения пациентов с ПНП к доктору. По результатам исследования EPIC, проведенного в 2008 г., выявлено, что из всех пациентов, амбулаторно обратившихся к неврологам, 39% обращались по поводу болевого синдрома, а 18% предъявляли жалобы, характерные для проявлений нейропатии [9].
Боль при ПНП наиболее часто носит нейропатический характер, однако она может быть и ноцицептивной, и смешанной.
Наиболее часто в клинической практике встречаются дисметаболические ПНП, среди которых значительно преобладает диабетическая. Среди пациентов с сахарным диабетом ПНП диагностируют более чем в 50% случаев [10, 11]. Хроническая нейропатическая боль выявляется у 16–26% пациентов при сахарном диабете.
Патогенез боли при различных дисметаболических ПНП аналогичен, но наиболее изучен на модели поражения периферических нервов при сахарном диабете.
Одним из основных механизмов нейропатической боли является повышение возбудимости мембран нервных волокон, связанное с повышением экспрессии потенциал-зависимых натриевых каналов [12]. В ходе ряда экспериментов установлено, что в поддерживании нейропатической боли важную роль играют патологические взаимодействия периферических сенсорных волокон: при дегенерации эфферентных волокон нерва отмечается спонтанная эктопическая нейрональная активность в интактных С-волокнах, сенситизация нейронов на фоне экспрессии цитокинов и нейротрофических факторов. Сенситизация нервных волокон, возникновение термической гипералгезии обусловлены действием серотонина. Возникновение боли при этом связывают с работой основных натриевых каналов: Nav1.3, Nav1.7, Nav1.8 и Nav1.9 [13]. Увеличение численности Na-каналов способствует развитию воспаления и вторичной центральной сенситизации. Показано, что каналы Nav1.7, Nav1.8, Nav1.9 экспрессированы на тонких ноцицептивных волокнах и участвуют в проведении болевой афферентации [14–17]. Повышенная экспрессия каналов Nav1.3, которые в норме у взрослых лишь в небольшой степени представлены в периферической нервной системе, и Nav 1.6 может играть важную роль в повышении возбудимости нейронов и развитии нейропатической боли при повреждении периферических нервов и спинного мозга [18, 19].
Другой механизм развития боли при ПНП обусловлен повреждением Aδ- и C-волокон [20, 21]. При нейропатической боли определяется более низкий порог активации Аβ- и Аδ-волокон на механическую стимуляцию, а также отмечается увеличение спонтанной активности в С-волокнах. Установлено, что аллодиния, возникающая при диабетической ПНП, является следствием гибели С-волокон с дальнейшей центральной сенситизацией, а повреждение Аδ-волокон, воспринимающих холодовые стимулы, ведет к холодовой гипералгезии.
Имеются данные об увеличении высвобождения нейротрансмиттеров при активации вольтажзависимых кальциевых каналов. Установлено, что у пациентов с сахарным диабетом отмечается увеличение плотности кальциевых каналов с α2Δ-1 субъединицей, что обуславливает развитие аллодинии.
В ряде экспериментальных работ показано, что при сахарном диабете интенсивность боли обусловлена быстрой активацией как MARK-киназы (the mitogen-activated protein kinase), так и внеклеточной сигнал-зависимой киназы — компонента ERK-каскада (extracellular signal-regulated protein kinase) не только в поврежденных, но и в интактных нейронах [22].
Среди токсических преобладает алкогольная ПНП, выявляющаяся у 12–30% пациентов, наблюдающихся по поводу хронического алкоголизма [23]. При проведении ЭНМГ ПНП выявляется у 97–100% больных, хронически злоупотребляющих алкоголем [24]. Механизм развития ПНП обусловлен токсическим действием ацетальдегида и пировиноградной кислоты, приводящим к аксональной дегенерации, а в патогенезе демиелинизации основное значение имеет дефицит витаминов группы В и никотиновой кислоты [25]. Поражение тонких волокон при алкогольной ПНП приводит к избирательной потере болевой или температурной чувствительности, парестезиям, дизестезиям, спонтанной боли.
Другой разновидностью токсических являются ПНП, обусловленные применением химиотерапии. Наиболее часто поражение периферических нервов развивается при применении винкристина, цисплатина, оксалиплатина и карбоплатина [26].
Патофизиология нейропатических нарушений наиболее изучена на экспериментальных моделях винкристиновой ПНП, при назначении которого в патогенезе болевого синдрома важную роль играет активация протеинкиназ А и С, оксида азота, способствующих возникновению механической гипералгезии [27].
Кроме того, экзогенные токсические полинейропатии могут быть следствием интоксикации солями тяжелых металлов, органическими, в том числе и фосфорорганическими, соединениями и лекарственными препаратами. В основе патологического процесса лежит аксональная дегенерация, а вторичная демиелинизация чаще всего имеет сегментарный характер и менее выражена.
Среди больных соматической патологией наиболее часто клинические признаки ПНП выявляют при тяжелых хронических заболеваниях печени, почек, желудочно-кишечного тракта, легких. Так, при билиарном циррозе ПНП диагностируется у 60–70% больных. Уремическую ПНП выявляют почти у 50% больных с хронической почечной недостаточностью [28, 29]. При заболеваниях желудочно-кишечного тракта, сопровождающихся нарушением питания и мальабсорбцией, развитие ПНП часто связано с дефицитом витаминов группы В [30, 31].
Среди пациентов, страдающих инфекционными заболеваниями, ПНП наиболее часто возникает у ВИЧ-инфицированных. Различные варианты периферической нейропатии клинически проявляются у 20–35% больных ВИЧ, а при аутопсии признаки поражения периферических нервов обнаруживают в 95% случаев [32]. Механизм боли преимущественно связан с поражением C-волокон, опосредующих восприятие тепловых стимулов [33], а также непосредственным токсическим действием антиретровирусных препаратов.
При воспалительных полинейропатиях боль является следствием поражения аксонов на фоне нарушения распределения натриевых каналов и выброса воспалительных медиаторов, что приводит к раздражению ноцицептивных рецепторов. В данном случае боль обусловлена повышением уровня циклооксигеназы-2, ПГ2 как в нейронах дорсального ганглия, так и задних рогах спинного мозга [34, 35].
Среди идиопатических воспалительных наиболее часто встречается острая воспалительная демиелинизирующая полирадикулонейропатия (ОВДП, синдром Guillain–Barré). Заболеваемость ОВДП составляет 1,1–1,8 × 10-5 и возрастает с увеличением возраста: у лиц до 16 лет она составляет 0,4–1,4-5, а у лиц старше 60 лет — 3,3 × 10-5 в год [36, 37].
Нейропатическая боль при васкулитах и ДБСТ также обусловлена увеличением экспрессии провоспалительных цитокинов в периферических нервах [38]. Частота возникновения ПНП при различных формах ДБСТ различна. Так, у пациентов с системной красной волчанкой ПНП развивается в 8–56% случаев; при ревматоидном артрите ПНП диагностируют практически у всех пациентов; при системной склеродермии и синдроме Шегрена — у 5–10% больных, при саркоидозе — у 5–15% пациентов [39–43].
Паранеопластические ПНП составляют около 1% всех ПНП и встречаются приблизительно у 5% больных с онкологическими заболеваниями [44]. Наиболее часто ПНП возникают у больных раком легких или дыхательных путей — 2,5–5,5% случаев, при миеломной болезни — в 5%. По данным ЭНМГ, изменения периферических нервов обнаруживают почти у 30% пациентов с впервые установленным диагнозом онкологического заболевания [45–47]. В таких случаях ПНП не связана со сдавлением нервов опухолью, метастатическим поражением нервной ткани или побочными эффектами химиотерапии и лучевой терапии, метаболическими, сосудистыми, гормональными изменениями. В ходе исследований выявлена связь паранеопластических синдромов с определенным типом онконевральных антител к антигенам Hu, CV2 [48, 49].
Около 25% случаев нейропатических нарушений неясной этиологии обусловлены наследственными ПНП. Среди которых выделяют наследственные моторно-сенсорные нейропатии (НМСН) и ряд ПНП, встречающихся при других наследственных заболеваниях. Наличие метаболического дефекта выявлено при некоторых наследственных ПНП: метахроматической лейкодистрофии, болезни Фабри, болезни Рефсума, болезни Бассейна–Корнцвейга и некоторых других.
При болезни Фабри — врожденном заболевании, характеризующемся наследственным дефицитом фермента альфа-G4-галактозидазы, ПНП обусловлена отложением сфингогликолипидов и гликопротеидов в тканях и нервных ганглиях. Нейропатическая боль является одним из ведущих клинических синдромов. Боль носит характер «кризов», в виде приступов интенсивных мучительных жгучих болей в руках и ногах, с иррадиацией в другие части тела, продолжительностью от нескольких минут до нескольких дней, лихорадки, каузалгии.
Прогрессирующая болевая ПНП встречается у пациентов при семейном варианте амилоидоза, парапротеинемиях и в 10% случаев первичного амилоидоза [50]. В настоящее время описано более 40 мутаций белка транстиретина (Amiloid-Transtiretin — A-TTR), ассоциированных с отложением амилоидных включений, которые выявляются при биопсии нервов.
ПНП, как правило, имеют хроническое течение, медленно прогрессируя на протяжении нескольких лет. Во многих случаях своевременно установить правильный нозологический диагноз и назначить адекватное лечение ПНП можно, применяя пошаговые алгоритмы с анализом анамнестических сведений, результатов осмотра и доступных лабораторных исследований (рис.).
Прежде всего больного следует расспросить о злоупотреблении алкоголем, воздействии токсических веществ и приеме лекарственных препаратов. В случае выявления показаний пациента необходимо направлять на консультацию к психиатру-наркологу. При подозрении на наличие нежелательных явлений лекарственных препаратов важно своевременно провести коррекцию терапии (шаг 1).
Устранение этиологических факторов при токсической ПНП позволяет надеяться на значительное улучшение состояния пациента. Патогенетическое лечение может включать дезинтоксикационную терапию, препараты тиоктовой кислоты (при алкогольной ПНП), витамины группы В (при ПНП, вызванной употреблением алкоголя, противотуберкулезных препаратов и др.). Симптоматическое лечение направлено на купирование боли.
Следующим шагом необходимо оценить соматическое состояние пациента и, с учетом анамнеза и жалоб, назначить обследование с целью исключения инфекционной патологии (в первую очередь — ВИЧ-инфекции, сифилиса, бруцеллеза, боррелиоза). При выявлении инфекционного заболевания пациента необходимо направить к профильным специалистам (шаг 2).
Своевременное и адекватное этиотропное лечение (специфическая антиретровирусная или антибактериальная терапия) позволяет в ряде случаев добиться улучшения или стабилизации состояния больного. Патогенетическая терапия является вспомогательной и недифференцированной. Симптоматическое лечение (купирование боли) может потребоваться в начале этиотропной терапии или на терминальных стадиях заболеваний. При ВИЧ-ассоциированных ПНП в случаях незначительной боли предлагают использовать ацетаминофен, нестероидные противовоспалительные препараты (НПВП) в сочетании с гастропротекторами (ингибиторами протонной помпы), при умеренной боли — НПВП в сочетании с легкими опиоидными анальгетиками, при сильной боли — опиоидные анальгетики. В качестве адъювантной терапии рекомендуют антидепрессанты и (или) антиконвульсанты [51].
С целью скрининга эндокринных заболеваний и патологии внутренних органов при выявлении симптомов и признаков ПНП в рутинной практике рекомендуют: общий клинический анализ крови, общий анализ мочи, биохимический анализ, позволяющий оценить функцию печени и почек, определение уровня гликемии, Т3 и тиреотропного гормона, витамина В12 и фолиевой кислоты. В случае отклонения результатов лабораторных анализов от референсных значений пациент должен быть проконсультирован терапевтом или эндокринологом с целью уточнения этиологического диагноза для последующего назначения или коррекции уже имеющейся терапии (шаг 3). При необходимости обследование дополняют определением уровня HbA1с, тестом на толерантность к глюкозе.
Если причина ясна и клиническая картина типична для определенной формы ПНП (например, при диабетической ПНП), соответствующее патогенетическое лечение в дополнение к этиотропному (например, заместительной терапии инсулином при сахарном диабете) может быть начато без дальнейшего обследования и включать препараты тиоктовой кислоты (при диабетической ПНП), витамины группы В (при ПНП, возникшей на фоне дефицита витамина В12). Симптоматическое лечение направлено на купирование боли. Наиболее эффективным считается назначение антиконвульсантов, достаточно эффективны — антидепрессанты, капсаицин, чрескожная стимуляция нервов.
Если причина ПНП по-прежнему не ясна, в дальнейшем необходимо предпринять попытку провести поиск онкологических заболеваний, ДБСТ и иной соматической патологии.
Зарубежные авторы рекомендуют включать в план обследования электрофорез белков сыворотки крови и мочи с иммунофиксацией, исследование активности ангиотензин-превращающего фермента, определение уровня антинуклеарных антител (АТ), Р-ANCA, С-ANCA, исследование на наличие паранеопластических АТ (anti-Hu, anti-Yo, anti-Ri, anti-Tr, anti-Ma, anti-CV2), антисульфатидных АТ, криоглобулинов, компьютерную томографию органов грудной клетки и брюшной полости, при необходимости выполнить позитронно-эмиссионную томографию [3, 8].
Однако, прежде чем проводить указанное выше углубленное обследование, необходимо исключить наследственный характер ПНП. При указании на повторные случаи в семье заболеваний со сходной клинической картиной необходимо проведение медико-генетического консультирования, включающего консультацию генетиком и молекулярно-генетические исследования, доступные в настоящее время (шаг 4). В спорадических случаях углубленное медико-генетическое консультирование может быть проведено параллельно с обследованием внутренних органов.
К сожалению, в большинстве случаев генетически детерминированных заболеваний патогенетическое лечение не разработано, а симптоматическая терапия недостаточно эффективна. Исключение составляют единичные заболевания, например, болезни Фабри. При своевременной диагностике заболевания и раннем назначении заместительной ферментной терапии (агалсидаза бета) можно рассчитывать на стабилизацию состояния больного и уменьшение боли.
Если причина ПНП остается не ясной или клиническая картина заболевания атипична, обязательным является выполнение электронейромиографии [6, 8]. Основные задачи нейрофизиолога: определить уровень (распространенность), характер (аксональный, демиелинизирующий или смешанный) и выраженность поражения периферических нервов (шаг 5).
Аксональная ПНП, согласно результатам ЭНМГ, может быть сенсорной или моторно-сенсорной. Среди причин, большинство из которых можно уточнить при сборе анамнестических сведений, наиболее частыми являются заболевания щитовидной железы и сахарный диабет, алкогольная и другие интоксикации, дефицит витаминов группы В. Значительно реже аксональные ПНП развиваются вследствие интоксикации солями тяжелых металлов, порфирии, паранеопластическом синдроме. Хроническая аксональная ПНП может быть идиопатической (наследственная моторно-сенсорная нейропатия II типа) или вторичной (ПНП при мультисистемных заболеваниях).
В случае выявления по данным ЭНМГ изменений демиелинизирующего характера, крайне важно оценить симметричность патологического процесса. Если снижение скорости проведения импульсов обнаружено при анализе ЭНМГ всех исследованных нервов, следует заподозрить наследственную моторно-сенсорную нейропатию I типа и направить пациента для проведения медико-генетического консультирования.
Иная ЭНМГ-картина наблюдается при демиелинизирующих воспалительных ПНП. Для хронической воспалительной демиелинизирующей полиневропатии характерны мультифокальные нарушения с частичным блоком проведения по моторным нервам.
В случае выявления воспалительной ПНП должно быть начато адекватное патогенетическое лечение — согласно отечественным и Европейской федерации неврологических сообществ (European Federation of Neurological Societies, EFNS) рекомендациям, курсовое внутривенное введение IgG (ВВИГ) и (или) плазмаферез. При хронической ВДП в дополнение возможно назначение кортикостероидов. Важное значение для верификации диагноза ВДП имеет динамическое наблюдение, включающее оценку изменения клинических и ЭНМГ-признаков в ответ на лечение, исследование цереброспинальной жидкости, определение anti-МАG IgM, АТ к ганглиозидам [8]. Симптоматическая терапия направлена на купирование боли и включает антиконвульсанты, НПВП и (или) легкие опиоидные анальгетики.
В 10% случаев демиелинизирующая ПНП обусловлена парапротеинемией.
Если в ходе диагностики так и не удается установить причину ПНП, рекомендуют провести гистологическое исследование биоптата нерва. Чаще всего в таких случаях обнаруживают признаки васкулита.
Однако, даже после выполнения всего спектра доступных современной медицине обследований, в 25% случаев причина ПНП по-прежнему остается неизвестной. Идиопатические хронические формы заболевания чаще всего наблюдают у лиц пожилого возраста, они представляют собой сенсорные медленно прогрессирующие ПНП.
Во всех случаях ПНП одним из важнейших направлений лечения является немедикаментозная реабилитация, которая направлена на сохранение или восстановление функции ходьбы и включает активную и пассивную лечебную физкультуру (ЛФК) под контролем методиста и врача ЛФК, массаж с целью профилактики контрактур; профилактику пролежней, гипостатической пневмонии, тромбозов глубоких вен; контроль и коррекцию нарушений глотания, дыхания, состояния функций мочевого пузыря и желудочно-кишечного тракта.
Анализ отечественной и зарубежной литературы показывает, что в настоящее время отсутствует единый подход к классификации и тактике ведения пациентов с ПНП. Учитывая высокую распространенность ПНП и значительный фенотипический полиморфизм, для практического здравоохранения крайне важно наличие простого доступного алгоритма диагностики и лечения, который бы позволял в условиях многопрофильных медицинских учреждений рационально планировать мероприятия по обследованию и реабилитации больных ПНП.
Литература
- Неврология. Национальное руководство / Под ред. Е. И. Гусева, А. Н. Коновалова, В. И. Скворцовой, А. Б. Гехт. М.: ГЭОТАР-Медиа. 2010: 1040. ISBN: 978–5-9704–0665–6.
- Marchettini P., Lacerenza M., Mauri E., Marangoni C. Painful Peripheral Neuropathies // Current Neuropharmacology. 2006; 4: 175–181.
- Hughes R. A. Clinical review: peripheral neuropathy // BMJ. 2002; 324: 466–469.
- Жулев Н. М. Невропатии. Руководство для врачей / Под ред. Н. М. Жулева. СПб: СПбМАПО, 2005. 416 c.
- http://apps.who.int/classifications/icd10/browse/2015/en#/G60-G64 (дата обращения: 25.09.2016).
- Imreova H., Pura M. Differential diagnosis of peripheral neuropathy // Cas Lek Cesk. 2005; 144 (9): 628–635.
- Smith A. G., Singleton J. R. The Diagnostic yield of a standardized approachto idiopathic sensory-predominant neuropathy // Arch Intern Med. 2004; 164: 1021–1025.
- Azhary H., Farooq M. U., Bhanushali M. et al. Peripheral neuropathy: differential diagnosis and management // Am Fam Physician. 2010; 81 (7): 887–892.
- Яхно Н. Н., Кукушкин М. Л., Давыдов О. С. и др. Результаты Российского эпидемиологического исследования распространенности невропатической боли (EPIC Study). Лечение невропатической боли // Consilium medicum. Неврология 2008; 2: 64–70.
- Bhadada S. K., Sahay R. K., Jyotsna V. P. et al. Diabetic Neuropathy: Current Concepts // Journal of Indian Academy of Clinical Medicine. 2001; 2: 304–318.
- Kaur S., Pandhi P., Dutta P. Painful diabetic neuropathy: an update // Annals of Neurosciences. 2011; 18 (4): 168–175.
- Dworkin R. H. Advances in neuropathic pain // Arch. Neurol. 2003; 60: 1524–1534.
- Craner M. J., Klein J. P., Renganathan M. et al. Changes of sodium channel expression in experimental painful diabetic neuropathy // Annals of Neurosciences. 2002; 52: 786–792.
- Minett M. S., Falk S., Santana-Varela S. et al. Pain without Nociceptors? Nav1.7-Independent Pain Mechanisms // Cell Reports. 2014; 6 (2): 301–312.
- Thakor D. K., Lin A., Matsuka Y. et al. Increased peripheral nerve excitability and local NaV1.8 mRNA up-regulation in painful neuropathy // Molecular Pain. 2009; 5: 14.
- Ahn H. S., Black J. A., Zhao P. et al. Nav1.7 is the predominant sodium channel in rodent olfactory sensory neurons // Molecular Pain. 2011; 7: 32.
- Huang J., Han C., Estacion M. et al. Gain-of-function mutations in sodium channel Na (v)1.9 in painful neuropathy // Brain. 2014; 137 (6): 1627–1642.
- Sittl R., Lampert A., Huth T. et al. Anticancer drug oxaliplatin induces acute cooling-aggravated neuropathy via sodium channel subtype NaV1.6-resurgent and persistent current // Proceedings of the National Academy of Sciences of the United States of America. 2012; 109 (17): 6704–6709.
- Alessandri-Haber N., Alcaraz G., Deleuze C. et al. Molecular determinants of emerging excitability in rat embryonic motoneurons // The Journal of Physiology. 2002; 541 (1): 25–39.
- Строков И. А., Баринов А. Н. Клиника, патогенез и лечение болевого синдрома при диабетической полиневропатии // Неврологический журнал. 2001; 6: 47–54.
- Vinik A. I., Mehrabyan A. Diabetic neuropathies // Med Clin North Am. 2004; 88: 947–999.
- Schafers M., Lee D. H., Brors D. et al. Increased sensitivity of injured and adjacent uninjured rat primary sensory neurons to exogenous tumor necrosis factor-alpha after spinal nerve ligation // J. Neuroscience. 2003; 23: 3028–3038.
- Beghi E., Monticelli M. L. Chronic symmetric symptomatic polyneuropathy in the elderly: a field screening investigation of risk factors for polyneuropathy in two Italian communities // J. Clin. Epidemiol. 1998; 51: 697–702.
- Dyck P. J., Thomas P. K. Peripheral neuropathy. W. B. Saunders Company. 1984; 2: 1912–1931.
- Koike H., Iijima M., Sugiura M. et al. Alcoholic neuropathy is clinicopathologically distinct from thiamine-deficiency neuropathy // Ann Neurol. 2003; 54 (1): 19–29.
- Quasthoff S., Hartung H. P. Chemotherapy-induced peripheral neuropathy // J. Neurol. 2002; 249: 9–17.
- Aley K. O., Levine J. D. Different peripheral mechanisms mediate enhanced nociception in metabolic/toxic and traumatic painful peripheral neuropathies in the rat // Neuroscience. 2002; 111: 389–397.
- Bolton C. F. Peripheral Neurophathies Associated With Chronic Renal Failure // Canadian Journal of Neurological Sciences. 1980; 7: 89–96.
- Janda K., Stompor T., Gryz E. et al. Evaluation of polyneuropathy severity in chronic renal failure patients on continuous ambulatory peritoneal dialysis or on maintenance hemodialysis // Przegl Lek. 2007; 64 (6): 423–430.
- McCombe P. A., McLeod J. G. The peripheral neuropathy of vitamin B 12 deficiency // Journal of the neurological sciences. 1984; 66: 117–126.
- Koike H., Misu K., Hattori N. et al. Postgastrectomy polyneuropathy with thiamine deficiency. J. Neurol Neurosurg Psychiatry. 2001; 71: 357–362.
- Estanislao L., Hart P., Simpson D. HIV neuropathy and selected infectious neuropathies // Continuum. 2003; 9 (6): 118–145.
- Martin C., Solders G., Sonnerborg A. et al. Painful and non-painful neuropathy in HIV-infected patients: an analysis of somatosensory nerve function // Eur. J. Pain. 2003; 7: 23–31.
- Ma W., Eisenach J. C. Morphological and pharmacological evidence for the role of peripheral prostaglandins in the pathogenesis of neuropathic pain // Eur. J. Neuroscience. 2002; 15: 1037–1047.
- Ma W., Du W., Eisenach J. C. Role for both spinal cord COX-1 and COX-2 in maintenance of mechanical hypersensitivity following peripheral nerve injury // Brain Res. 2002; 937: 94–99.
- Hughes R. A., Rees J. H. Clinical and epidemiologic features of Guillain-Barre syndrome // J. Infect Dis. 1997; 176: 92–98.
- McGrogan A., Madle G. C., Seaman H. E. et al. The epidemiology of Guillain-Barré syndrome worldwide. A systematic literature review // Neuroepidemiology 2009; 32 (2): 150–163.
- Heuss D., Schlotter-Weigel B., Sommer C. Diagnosis and therapy of vasculitic neuropathy // Fortschr Neurol Psychiatr. 2003; 71: 172–186.
- Bougea A., Anagnostou Konstantinos G. et al. A systematic review of peripheral and central nervous system involvement of rheumatoid arthritis, systemic lupus erythematosuS., primary Sjogren’s syndrome, and associated immunological profiles // International Journal of Chronic Diseases. 2015; 2015: 910352.
- Agarwal V., Singh R., Wiclaf et al. A clinical, electrophysiological, and pathological study of neuropathy in rheumatoid arthritis // Clin Rheumatol 2008; 27: 841–844.
- Sim M. K., Kim D. Y., Yoon J. et al. Assessment of peripheral neuropathy in patients with rheumatoid arthritis who complain of neurologic symptoms // Annals of Rehabilitation Medicine. 2014; 38 (2): 249–255.
- Cojocaru I. M., Cojocaru M., Silosi I. et al. Peripheral Nervous System Manifestations in Systemic Autoimmune Diseases // Mædica. 2014; 9 (3): 289–294.
- Said G., Lacroix C., Planté-Bordeneuve V. et al. Nerve granulomas and vasculitis in sarcoid peripheral neuropathy: a clinicopathological study of 11 patients // Brain 2002; 125: 264–75.
- Шнайдер Н. А., Кантимирова Е. А. Паранеопластическая полинейропатия: дефиниция, этиопатогенез, диагностика // Сибирское медицинское обозрение. 2010; 1: 12–16.
- Grisold W., Drlicek M. Paraneoplastic neuropathy // Curr. Opin. Neurol. 1999; 12 (5): 617–625.
- Шнайдер Н. А., Кантимирова Е. А. Паранеопластическая полинейропатия: дефиниция, этиопатогенез, диагностика // Сибирское медицинское обозрение. 2010; 1: 12–16.
- Forman A. D. Peripheral neuropathy and cancer // Current oncology reports. 2004; 6 (1): 20–25.
- Antoine J. C., Honnorat J., Camdessanche J. P. et al. Paraneoplastic anti-CV2 antibodies react with peripheral nerve and are associated with a mixed axonal and demyelinating peripheral neuropathy // Ann. Neurol. 2001; 49: 214–221.
- Antoine J. C., Mosnier J. F., Honnorat J. et al. Paraneoplastic demyelinating neuropathy, subacute sensory neuropathy, and anti-Hu antibodies: clinicopathological study of an autopsy case // Muscle Nerve. 1998; 21 (7): 850–857.
- Plante-Bordeneuve V., Ferreira A., Lalu T. et al. Diagnostic pitfalls in sporadic transthyretin familial amyloid polyneuropathy (TTR-FAP) // Neurology. 2007; 69: 693–698.
- https://aidsetc.org/guide/pain-syndrome-and-peripheral-neuropathy (дата обращения: 25.09.2016).
- Javed S., Petropoulos I. N., Alam U., Malik R. A. Treatment of painful diabetic neuropathy // Ther Adv Chronic Dis. 2015; 6 (1): 15–28.
И. В. Ситкали
О. В. Колоколов1, доктор медицинских наук
А. В. Фисун
ФГБОУ ВО СГМУ им. В. И. Разумовского МЗ РФ, Саратов
1 Контактная информация: kolokolov@inbox.ru
Полинейропатия — это патология периферической нервной системы, которая развивается в результате диффузного повреждения периферических нервов и их аксонов. Отсюда и название болезни. В ее основе — генерализованное поражение осевого цилиндра периферических нервов.

Главный редактор, заведующий хирургическим отделением
Задать вопрос
Врач-хирург высшей квалификационной категории, доктор медицинских наук, профессор кафедры общей хирургии АГМУ.
Содержание
- Что такое аксональная полинейропатия
- Причины
- Первые признаки
- Симптомы
- Диагностика
- Прогноз
- Профилактика
- Идиопатическая прогрессирующая невропатия
- Лечение
- Госпитализация
- Профилактика
Что такое аксональная полинейропатия
Аскональная полинейропатия считается междисциплинарной проблемой, с ней часто сталкиваются доктора различных специализаций. В первую очередь с данным заболеванием обращаются к неврологу. Частота возникающего синдрома неизвестна, так как отсутствуют статистические данные.
На данный момент известны всего три важных патоморфологических механизма, которые лежат в истоках формирования полинейропатии:
- валлеровская дегенерация;
- первичная демиелинизация;
- первичная аксонопатия.
В соответствии с иммунологической теорией полинейропатия является результатом перекрестного образования иммунных глобулинов, уничтожающих собственные клетки, в результате чего возникает некроз тканей и мышечное воспаление.
Исследователи выдвигают ряд гипотез возникновения и проблем течения аксональной полинейропатии:
- Сосудистая. Базируется на вовлечении в процесс сосудов, по которым кислород и питательные вещества поступают в периферические нервы. Изменяются характеристики крови по качественному и количественному составу, что может привести к ишемии нервных окончаний.
- Теория оксидативного стресса. Позиционирует формирование болезни со стороны нарушения обмена оксида азота, вследствие чего изменяются калий-натриевые механизмы, лежащие в основе формирования нервного возбуждения и проведения импульсов по нервам.
- Теория деактивации факторов роста нерва. Говорит о том, что болезнь возникает из-за недостатка аксонального транспорта с последующим развитием аксонопатии.
- Иммунологическая. Объясняет развитие заболевания в результате перекрестного образования антител к структурам периферической нервной системы, которое сопровождается аутоиммунным воспалением, а затем и некрозом нервов.
Даже при использовании ультрасовременных методов диагностики сложно найти достоверную причину патологии, выяснить ее получается только у 50-70% пострадавших.
Факторов возникновения полинейропатии нижних конечностей по аксональному типу очень много. Однако даже инновационные способы исследования не позволяют установить истинную этиологию заболевания.
Причины
Самые распространенные причины возникновения аксональной полинейропатии нижних конечностей:
- истощение организма;
- длительный недостаток витаминов группы В;
- недуги, ведущие к дистрофии;
- острые инфекции;
- токсическое поражение ртутью, свинцом, кадмием, угарным газом, спиртными напитками, метиловым спиртом, фосфорорганическими соединениями, медицинскими препаратами, принимаемыми без согласования с врачом;
- болезни сердечно-сосудистой, кроветворной, кровеносной и лимфатической систем;
- эндокринологические патологии, в том числе инсулинозависимость.
Главными факторами, которые провоцируют развитие моторной или сенсомоторной аксональной полинейропатии, являются:
- эндогенная интоксикация при почечной недостаточности;
- аутоиммунные процессы, протекающие в организме;
- амилоидоз;
- вдыхание токсических веществ или паров.
Также болезнь может быть обусловлена наследственностью.
Нехватка в организме витаминов группы В, а в особенности пиридоксина и цианокобаламина, крайне негативно воздействует на проводимость нервных и моторных волокон и может вызывать сенсорную аксональную полинейропатию нижних конечностей. Это же происходит при хронической алкогольной интоксикации, глистной инвазии, заболеваниях желудочно-кишечного тракта, которые ухудшают скорость всасывания.
Токсическое отравление лекарственными препаратами, аминогликозидами, золотыми солями и висмутом занимают большой процент в структуре факторов аксональной невропатии.
У пациентов с сахарным диабетом нарушена функция периферических нервов из-за нейротоксичности кетоновых тел, то есть метаболитов жирных кислот. Происходит это из-за невозможности организма использовать глюкозу как главный источник энергии. Поэтому вместо нее окисляются жиры.
При аутоиммунных заболеваниях, протекающих в организме, иммунная система человека атакует собственные нервные волокна, воспринимая их как источник опасности. Это происходит из-за провокации иммунитета, возникающей при неосторожном приеме иммуностимулирующих медикаментов и нетрадиционных методик лечения. Поэтому у людей, которые склонны к возникновению аутоиммунных заболеваний, пусковыми факторами аксональной полинейропатии являются:
- иммуностимуляторы;
- вакцины;
- аутогемотерапия.
При амилоидозе в организме накапливается такой белок, как амилоид. Именно он нарушает основные функции нервных волокон.
Первые признаки
Заболевание обычно начинает развиваться с поражения толстых или тонких нервных волокон. Зачастую аксональная полинейропатия имеет дистальное симметричное распределение на кисти или стопы. Нейропатия чаще всего сначала поражает нижние конечности, а затем симметрично распространяется вверх по телу. К самым частым первичным симптомам поражения относят:
- мышечную слабость;
- болевой синдром в конечностях;
- жжение;
- ощущение ползания мурашек;
- онемение кожных покровов.
Симптоматика ярче всего проявляется в вечернее и ночное время суток.
Симптомы
Врачи подразделяют хроническое, острое и подострое течение аксональной полинейропатии. Заболевание подразделяется на два вида: первично-аксональный и демиелинизирующий. В ходе течения болезни к ней присовокупляется демиелинизация, а затем и вторично аксональный компонент.
К основным проявлениям недуга относятся:
- вялость в мышцах ног или рук;
- спастический паралич конечностей;
- чувство подергивания в мышечных волокнах;
- головокружение при резкой перемене положения тела;
- отек конечностей;
- жжение;
- покалывание;
- ощущение ползания мурашек;
- снижение чувствительности кожных покровов к высокой или низкой температуре, боли и касаниям;
- нарушение ясности речи;
- проблемы с координацией.
Вегетативными признаками сенсомоторной полинейропатии асконального типа считаются следующие симптомы:
- учащенный или, напротив, замедленный сердечный ритм;
- неумеренное потоотделение;
- чрезмерная сухость кожи;
- изменение цвета кожных покровов;
- нарушение эякуляции;
- эректильная дисфункция;
- проблемы с мочеиспусканием;
- сбой двигательных функций желудочно-кишечного тракта;
- повышенное слюнотечение или, наоборот, сухость во рту;
- расстройство аккомодации глаза.
Заболевание проявляется в нарушениях функций поврежденных нервов. Именно периферические нервные волокна отвечают за двигательные функции мышечной ткани, чувствительность, а также оказывают вегетативное воздействие, то есть регулируют сосудистый тонус.
Для нарушения функции проводимости нервов характерны расстройства чувствительности, например:
- чувство ползания мурашек;
- гиперестезия, то есть увеличение чувствительности кожи к внешним раздражителям;
- гипестезия, то есть уменьшение чувствительности;
- отсутствие ощущения собственных конечностей.
Когда аксонально-демиелинизирующая полинейропатия поражает вегетативные волокна, нарушается регуляция сосудистого тонуса. Это приводит к сдавливанию капилляров, что вызывает отек тканей. Скопление жидкости в пораженных участках может привести к значительному увеличению размеров как нижних, так и верхних конечностей. Поскольку при полинейропатии этого типа в этих областях скапливается много крови, вставание может вызывать у пациента постоянное головокружение. Отсутствие трофической функции может также привести к эрозивным и язвенным поражениям на нижних конечностях.
Аксональная моторная полинейропатия проявляется в двигательных нарушениях верхних и нижних конечностей. Когда моторные волокна, отвечающие за движения рук и ног, повреждены, то наступает полный или частичный паралич мышц. Обездвиживание может проявляться совершенно нетипично — может ощущаться как скованность мышечных волокон, так и чрезмерная их расслабленность. При средней степени поражения ослаблен мышечный тонус.
В ходе течения заболевания могут быть усилены или ослаблены сухожильные и надкостничные рефлексы. В редких случаях доктор-невролог их не наблюдает. При болезни часто могут быть поражены черепные нервы, которые проявляются следующими нарушениями:
- глухотой;
- онемением подъязычных мышц и мускулатуры языка;
- невозможностью проглотить еду или жидкость из-за проблем с глотательным рефлексом.
Когда поражен тройничный, лицевой или глазодвигательный нерв, изменяется чувствительность кожных покровов, развиваются параличи, возникает асимметрия лица и подергивание мышц. Иногда при диагностированной аксонально-демиелинизирующей полинейропатии поражения верхних или нижних конечностей могут быть асимметричными. Такое случается при множественной мононейропатии, когда коленные, ахилловы и карпорадиальные рефлексы несимметричны.
Диагностика
Главной методикой исследования, которая позволяет обнаружить локализацию патологического процесса и степень пораженности нервов, является электронейромиография.
Чтобы определить причину заболевания, врачи назначают следующие анализы:
- определение уровня сахара в плазме крови;
- токсикологические тесты;
- полный анализ мочи и крови;
- выявление уровня холестерина в организме.
Нарушение нервных функций устанавливается при помощи определения температурной, вибрационной и тактильной чувствительности.
При первичном осмотре применяется зрительная методика исследования. То есть врач, к которому обратился с жалобами пострадавший, осматривает и анализирует такие внешние симптомы, как:
- уровень давления крови в верхних и нижних конечностях;
- чувствительность кожных покровов к прикосновениям и температуре;
- наличие всех необходимых рефлексов;
- диагностика отечности;
- изучение внешнего состояния кожи.
Выявить аксональную полинейропатию можно при помощи следующих инструментальных исследований:
- магнитная резонансная томография;
- биопсия нервных волокон;
- электронейромиография.
Лечение аксональной полинейропатии
Лечение аксональной полинейропатии должно быть комплексным и направленным на причину развития заболевания, его механизмы и симптоматику. Гарантией эффективной терапии является своевременное выявление болезни и лечение, которое сопровождается абсолютным отказом от сигарет, алкоголя и наркотических веществ, ведением здорового образа жизни и соблюдением всех рекомендаций врача. В первую очередь проводятся следующие терапевтические мероприятия:
- избавление от токсического воздействия на организм, если оно присутствует;
- антиоксидантная терапия;
- прием препаратов, которые воздействуют на тонус кровеносных сосудов;
- восполнение дефицита витаминов;
- регулярный контроль концентрации глюкозы в плазме крови.
Отдельное внимание уделяется лечению, направленному на купирование острого болевого синдрома.
Если присутствуют периферические парезы, то есть существенное снижение мышечной силы с многократным уменьшением амплитуды движений, то в обязательном порядке показана лечебная физкультура и специальные физические упражнения, направленные на возвращение тонуса мышечным тканям и предотвращение образования различных контрактур. Особенно важна регулярная психологическая поддержка, которая не дает пациенту впасть в депрессию, сопровождающуюся расстройством сна и чрезмерной нервной возбудимостью.
Лечение аксональной полинейропатии — это продолжительный процесс, так как нервные волокна восстанавливаются долго. Поэтому не стоит ожидать моментального выздоровления и возвращения к привычному образу жизни. Медикаментозная терапия включает такие препараты, как:
- обезболивающее;
- глюкокортикоиды;
- витамины группы В;
- антиоксиданты;
- сосудорасширяющие;
- средства, ускоряющие метаболизм и улучшающие микроциркуляцию крови.
Терапия лекарственными препаратами направлена на восстановление функций нервов, улучшение проводимости нервных волокон и скорости передачи сигналов центральной нервной системе.
Лечение следует проводить длительными курсами, которые не стоит прерывать, хоть и эффект от них проявляется не сразу. Чтобы устранить болевые ощущения и расстройство сна, назначают следующие медикаменты:
- антидепрессанты;
- противосудорожные;
- препараты, купирующие аритмию;
- обезболивающие.
Для избавления от боли используют нестероидные противовоспалительные препараты. Но стоит помнить, что применять их можно только короткий промежуток времени, так как длительное употребление может привести к повреждению слизистой оболочки желудочно-кишечного тракта.
К физиотерапевтическим методам лечения аксональной полинейропатии относятся:
- терапия магнитными волнами;
- грязелечение;
- электростимуляция;
- иглоукалывание;
- лечебный массаж;
- физкультура;
- ультрафонофорез;
- гальванотерапия.
Именно лечебная физкультура позволяет сохранить работоспособность мышечных тканей и поддерживать конечности в нужном положении. Регулярные занятия спортом вернут мышцам тонус, гибкость и увеличат амплитуду движений до нормальной.
Прогноз
Если заболевание обнаружено на ранней стадии и комплексно лечится квалифицированными специалистами, то прогноз для жизни и здоровья пациента более чем благоприятный. Стоит вести правильный образ жизни, рацион должен быть богат витаминами и минералами, необходимыми для правильного функционирования организма.
Если долгое время игнорировать болезнь и не предпринимать никаких действий, результат будет плачевным вплоть до полного паралича.
Профилактика
Пациент в обязательном порядке должен совершать профилактические мероприятия, которые помогут избежать рецидива или возникновения опасного заболевания. Они включают в себя обогащение рациона витаминами, регулярный контроль уровня сахара в крови, полный отказ от табакокурения, наркотических веществ и алкогольных напитков.
В целях профилактики болезни рекомендуется:
- носить удобную обувь, которая не пережимает стопу, ухудшая кровоток;
- регулярно осматривать обувь, чтобы избежать образования грибка;
- исключить пешие прогулки на длительные расстояния;
- не стоять долгое время на одном месте;
- мыть ноги прохладной водой или делать контрастные ванночки, что помогает улучшить циркуляцию крови в организме.
Пострадавшим в стадии ремиссии категорически запрещается принимать лекарственные препараты без согласования с лечащим врачом. Важно своевременно лечить воспалительные заболевания, соблюдать меры предосторожности при работе с токсическими веществами, которые оказывают пагубное воздействие на организм, регулярно выполнять лечебные физические упражнения.
Идиопатическая прогрессирующая невропатия
Полирадикулоневропатии — группа заболеваний периферической нервной системы, характеризующихся диффузным поражением периферических нервных волокон, входящих в состав различных нервов. Клинически полиневропатии проявляются периферическим тетрапарезом, арефлексией, нарушением чувствительности (часто по типу «носков и перчаток») и вегетативной дисфункцией, в частности вазомоторными нарушениями, расстройством потоотделения и другими проявлениями периферической нервной системы. При поражении волокон глубокой чувствительности развивается сенситивная атаксия.
Хроническая идиопатическая аксональная невропатия (ХИАН) — встречается преимущественно в среднем и пожилом возрасте, у детей редко и служит причиной до 3% случаев полиневропатий. Чаще всего она проявляется ощущением жжения и онемением в стопах, иногда легкой вегетативной дисфункцией, слабостью и атрофией мышц дистальных отделов нижних конечностей, а иногда и легкими нарушениями глубокой чувствительности. Течение обычно медленно прогрессирующее.
Хроническая воспалительная демиелинизирующая полирадикулоневропатия (ХВДП) — является причиной 5% полиневропатий. В отличие от синдрома Гийена-Барре характеризуется более медленным развитием, хроническим ремиттирующим или непрерывно прогрессирующим (в течение не менее 2 мес.) течением. Восстановление часто бывает неполным. Эта форма заболевания напоминает болезни мотонейронов. Заболевание встречается в любом возрасте. Предполагается, что в основе патогенеза ХВДП лежат нарушения иммунной системы. Может быть повышен титр антител к ганглиозидам. Слабость в начале отмечается в дистальных отделах ног, затем распространяется на руки и проксимальные отделы ног. Параллельно развиваются арефлексия и нарушения чувствительности. Выраженные парезы редко сопровождаются нарастающей атрофией. В 10% случаев чувствительные нарушения преобладают над двигательными. У части больных поражаются черепные нервы, обычно лицевой и бульбарные, реже глазодвигательные.
Лечение
Тактика лечения
Прежде всего, необходимо проверить, не является ли ХВДП проявлением иного заболевания, и если оно будет найдено — назначить соответствующее лечение. При идиопатической хронической воспалительной демиелинизирующей полирадикулоневропатии применяют кортикостероиды, плазмаферез и азатиоприл. Тактика определяется тяжестью симптоматики и возможностью проведения плазмофереза. С помощью комбинированной, адекватной иммунотерапии удается добиться улучшения у 90% больных ХВДП, однако главная проблема лечения ХВДП заключается в том, чтобы удержать достигнутый положительный результат. В настоящее время существует 3 основных средств лечения ХВДП — кортикостероиды, плазмоферез, внутривенно иммуноглобулин.
Цель лечения: достижение стойкой ремиссии, сохраняющейся после иммунотропных средств, улучшение двигательной активности, увеличение силы и объема активных движений, предупреждение осложнений (контрактур, атрофий), социальная адаптация, улучшение качества жизни.
Немедикаментозное лечение
Диета низкосолевая с высоким содержанием белка, но низким содержанием жира.
Активная реабилитация включает лечебную физкультуру, которая занимает одно из ведущих мест в лечении больных. Основная задача лечебных упражнений в раннем восстановительном периоде — тренировка основных параметров двигательной системы, которая заключается в постепенном и дозированном увеличении силы мышечного сокращения, амплитуды. Применяют пассивные и пассивно-активные упражнения с переходом к активным упражнениям.
Стимулирующий массаж пораженных конечностей, мышц спины.
Физиолечение — магнитотерапия, биоптрон, УВЧ на пораженные сегменты спинного мозга, СМТ паретичных мышц, озокеритовые аппликации, электрофорез с прозерином.
Иглорефлексотерапия.
Медикаментозное лечение
Кортикостероиды. Чаще всего лечение начинают с преднизолона в дозе — длительное назначение в дозе 0,5-1,5 мг/кг/сут. (до 100 мг в день). После достижения эффекта (обычно через 3-4 недели) дозу начинают осторожно снижать, постепенно переходя на прием препарата через день. Эту дозу сохраняют в течение нескольких месяцев — до тех пор, пока не произойдет существенно стойкого регресса неврологического дефицита. В последующем производят снижение дозы на 10 мг в месяц (или 5 мг каждые 2 недели) до 20 мг через день, после чего дозу снижают на 2,5 мг каждые 2-3 недели.
В отсутствии эффекта (10-15% больных) кортикостероиды отменяют гораздо быстрее. Во избежание рецидива прием поддерживающей дозы (5-10 мг через день) продолжают на протяжении нескольких лет. У части больных препарат в конце концов удается отменить, но у других на фоне отмены, состояние вновь ухудшается, и они вынуждены принимать его достаточно длинное время. В тяжелых случаях лечение начинают с высокой дозы метилпреднизолона (1000 мг внутривенно, капельно на 200 мл 5% глюкозы в течение 3-5 дней), после чего переходят на прием преднизолона внутрь, но иногда лечение проводят курсами пульс-терапии метилпреднизолона, повторными каждые 4-8 недель (интервалы между курсами могут постепенно увеличиваться).
На фоне лечения кортикостероидами мышечная сила обычно начинает увеличиваться через 1-2 месяца и может сохраняться до года и более. Для защиты пищеварительной системы следует принимать такие препараты, как ранитидин для H2-рецепторов (150 мг дважды в день) или ингибитор протонной помпы омепразол (20 мг в день). Кроме того, люди, находящиеся на длительной кортикостероидной терапии, должны следить за своим весом, артериальным давлением, уровнем глюкозы в крови, а также уровнем калия. Чтобы минимизировать риски для здоровья, такие как остеопороз и сердечные заболевания, важно соблюдать низкосолевую диету с высоким содержанием белка и низким содержанием жира, а также принимать добавки кальция, бисфосфонаты и, при необходимости, анаболические стероиды. Тем пациентам с идиопатической хронической воспалительной демиелинизирующей полирадикулонейропатией, которые хорошо реагируют на кортикостероиды, для достижения наилучших результатов, скорее всего, потребуется пожизненная поддерживающая доза в 5-20 мг каждый день.
Азатиоприл. При малой эффективности или непереносимости кортикостероидов, а также в тех случаях, когда их дозу не удается снизить, назначают цитостатики (азатиоприн 2,5 мг/кг/сут.). Взрослым азатиоприл назначают по 50 мг 3 раза в сутки; добавляют к кортикостероидам, если не получено улучшение после 3-4 недель лечения, или назначают одновременно с плазмаферезом, если он выбран в качестве основного метода лечения.. В ряде случаев получено улучшение при лечении циклофосфамидом, 1 г/м 2 внутривенно капельно, ежемесячно, или циклоспорин, 4-6 мг/кг/сут.). При тяжелых формах с самого начала используют сочетание азатиоприна с кортикостероидами. Во время лечения необходимо следить за состоянием кроветворения и функции печени.
Плазмаферез. С тем, чтобы избежать длительного приема кортикостероидов и цитостатиков, используют плазмаферез и иммуноглобулин. Циклы плазмафереза проводят в комбинации с медикаментозным лечением иммуносупрессорами. Повторные циклы плазмафереза элиминируют антитела IgG против периферической нервной ткани. Обнаружение последних служит прямым показанием для проведения плазмафереза. Проводят 2 сеанса в неделю, в течение 3 недель, добавляют к кортикостероидам, если они не эффективны в течение первых 1-2 недель.
Иммуноглобулин (октагам, сандоглобуллин, хумаглобин и др.) вводят — внутривенное введение в дозе 0,4 г/кг/сут. в 1 мл физиологического раствора, в течение 3-5 дней подряд (скорость инфузии 6-8 час), если отмечается позитивный клинический эффект, курс введения иммуноглобулина повторяется. Побочные эффекты — головная боль, тошнота, лихорадка. Улучшение проявляется в течение 3 недель и продолжается в среднем 6 недель. Однако продолжительность улучшения не превышает нескольких недель или месяцев, после чего введение иммуноглобулина приходится повторять (1 г/кг в течение 1-2 дней).
В связи с этим разработаны схемы с более плавным прекращением лечения (например, 1 мг/кг/сут., в течение 2 дней, затем ту же дозу вводят через 2 и 4 недели, после чего повторяют ежемесячно на протяжении нескольких месяцев).
При частых рецидивах целесообразно присоединение малых доз преднизолона (0,5 мг/сет). Комбинировать плазмаферез и в/в введение иммуноглобулина не целесообразно. Серьезных побочных эффектов нет, однако пока не установлено, достаточно ли эффективен иммуноглобулин в качестве монотерапии.
В ряде исследований показана эффективность при ХВДП интерферонов (альфа и бета), методов иммуноабсорбции, однако их роль в лечении данного заболевания остается неясной.
Витаминотерапия: витамины группы В — В, В6, В.
Лечение препаратами, действующими на сосудистую систему, улучшающими реологические свойства крови и микроциркуляцию, проводится в виде последовательных курсов, каждый из них длительностью 2-3 недели. Применяются в возрастных дозировках — трентал, кавинтон, танакан.
Препараты, улучшающие метаболизм: церебролизин, актовегин, пирацетам, пиритинол, гинкго-билоба;
Метаболические средства — фолиевая кислота, аевит, оротат калия.
Дальнейшее ведение:
- — диспансерный учет у невропатолога по месту жительства;
- — регулярные занятия ЛФК;
- — соблюдение низкосолевой диеты с высоким содержанием белка, но низким содержанием жира;
- — продолжить прием преднизолона с постепенным снижением дозы, прием ранитидина.
Перечень основных медикаментов:
- Азатиоприн, 50 мг
- Актовегин, ампулы по 80 мг
- Аскорбиновая кислота, таблетки 0,05
- Иммуноглобулин человека для внутривенного введения (хумаглобин), 5 мл (250 мг), 10 мл (500 мг), 20 мл (1000 мг), 50 мл (2500 мг), 100 мл (000 мг)
- Кальций-Д3 Никомед, таблетки 0,5
- Нейромидин, таблетки 20 мг
- Пиридоксин гидрохлорид (витамин В6), ампулы 5% 1 мл
- Преднизолон, ампулы 30 мг
- Преднизолон, таблетки 5 мг
- Ранитидин, таблетки 0,15
- Тиамин бромид (витамин В1), ампулы 5% 1 мл
- Фолиевая кислота, таблетки 0,001
- Цианокобаламин (витамин В12), ампулы 500 мкг
Дополнительные медикаменты:
1. Актовегин, ампулы 2 мл 80 мг
2. Винпоцетин (кавинтон), таблетки 5 мг
3. Калия оротат, таблетки 0,5
4. Метандростенолон, таблетки 0,005
5. Метилпреднизолон (метилпред, солюмедрол), суспензия для инъекций 1 мл, 40 мг
6. Оксибрал, ампулы 2 мл
7. Октагам, флаконы по 50 мл, 100 мл и 200 мл
8. Омепразол, капсулы 20 мг
9. Пентоксифиллин (трентал), таблетки 0,1
10. Пирацетам, ампулы 5 мл
11. Ретоболил, ампулы по 1 мл 5% (50 мг) в масле
12. Танакан, таблетки 40 мг
13. Церебролизин, ампулы 1 мл
14. Циклоспорин (сандиммун), капсулы 10 мг, 25 мг, 100 мг
Индикаторы эффективности лечения:
1. Увеличение мышечной силы, объема активных движений, мышечного тонуса в пораженных конечностях.
2. Улучшение походки.
3. Улучшение трофики паретичных мышц, двигательных функций.
4. Удержание достигнутого положительного результата.
Госпитализация
Показания к госпитализации (плановая): парезы, параличи, нарушение походки, слабость и нарушение чувствительности в конечностях, контрактуры, деформации стоп.
Профилактика
Профилактические мероприятия:
1. Профилактика рецидивов заболевания.
2. Предупреждение контрактур, атрофий, растяжение мышц, ретракции сухожилий, скелетных деформаций — сколиоза, подвывиха и вывиха суставов, эквиноварусной деформации стопы.
Полинейропатия
Полинейропатия — это группа заболеваний, характеризующаяся множественным и диффузным поражением корешков, сплетений и периферических нервов. Болезнь не ограничивается одним нервом и поражает сразу множество периферийных нервных волокон, вызывая нарушения чувствительности, слабость и сложность в управлении конечностями. Часто полинейропатии сопровождаются ощущением покалывания, мурашек, жжения, онемения или болевым синдромом.
В зависимости от того, какие нервные волокна в большей степени вовлекаются в патологический процесс, возникают следующие жалобы:
- чувствительные симптомы: пациента беспокоят онемение, покалывание, жжение, «ползанье мурашек» в кистях и/или стопах; неустойчивость при ходьбе, усиливающаяся в темноте и при закрывании глаз;
- двигательные симптомы: развивается неловкость, слабость в кистях и/или стопах; похудание мышц рук и ног; нарушение мелкой моторики (сложности при застегивании пуговиц и молнии, завязывании шнурков и т.д.); затруднения при ходьбе («шлепанье» стоп, трудности при подъеме и спуске с лестницы и т.д.);
- вегетативные симптомы: колебание цифр артериального давления, «перебои» в работе сердца, запоры или диарея, сухость кожи или повышенная потливость, снижение либидо, нарушение эрекции.
При полинейропатии может происходить как изолированное поражение определенного типа нервных волокон, так и их сочетание, что приводит к появлению разнообразной клинической картины.
Причины полинейропатии
Полинейропатии существуют, как следствие поражения нервных волокон в результате различных заболеваний. Негативное влияние на нервную ткань могут оказывать травмы, инфекционные заболевания, патологические процессы в разных органах, гормональные нарушения.
Как правило, заболевание поражает определенный тип нервных волокон:
- Двигательных (укусы клещей, спинальная мышечная атрофия);
- Сенсорных (онкология, острая интоксикация, сахарный диабет);
- Черепных (болезнь Лайма, дифтерия).
Также причинами поражения нервной ткани, приводящими к развитию полинейропатий, могут выступать отравления солями тяжелых металлов, передозировки некоторых лекарственных препаратов, употребление в пищу токсичных растений и грибов, укусы некоторых насекомых. При острых отравлениях нервная ткань разрушается стремительно, с током крови, поэтому даже при выживании пациента высока вероятность инвалидизации.
Важно как можно раньше уточнить причину полинейропатии, т.к. от этого зависит прогноз и тактика лечения!
Симптомы полинейропатии
Главный механизм работы всех полинейропатий — разрушение нерва: аксона, его миелиновой оболочки или питающих нервную ткань кровеносных сосудов. Миелиновая оболочка, или миелин, присутствует не у всех нервных волокон — только у тех, для которых повышение скорости нервного импульса критически важно. Оболочка выполняет электроизолирующую функцию за счет множества тончайших слоев клеточной мембраны, и скорость передачи импульса ускоряется в 5-10 раз.* Такой защитно-изолирующий слой окутывает сам нерв, а также кровеносные и лимфатические сосуды, которые его питают.
Таким образом, повреждение миелиновой оболочки сопровождается:
- парестезиями, то есть, нарушением чувствительности нервных волокон;
- снижением рефлексов;
- уменьшением чувствительности к температурам и боли;
- мышечной слабостью.
Повреждения миелина называют демиелинизацией нерва. Процесс часто связан с иммунным ответом на бактериальные и вирусные инфекции, в редких случаях возникает при вакцинации.
Нарушение кровоснабжения нерва обычно связано с атеросклерозом, васкулитом, гиперкоагуляцией крови, а также возникает при травмах и длительном пережатии сосудов. Так, мурашки, которые появляются в отсиженной ноге, являются одним из признаков временно нарушенного кровообращения. При полинейропатии, вызванной нарушением кровоснабжения, редко полностью выпадают рефлексы, гораздо чаще наблюдаются:
- болезненность, жжение, мурашки, онемение, неприятные ощущения, которые пациенту сложно описать;
- несимметричные нарушения — страдает одна рука или нога, реже — одна половина парных нервов корпуса;
- вегетативная дисфункция, изменение цвета и фактуры кожи — она словно усыхает, становится тонкой, прозрачной и глянцевой;
- со временем нарастает мышечная слабость.
Повреждение аксона нерва, или аксонопатия, может быть симметричной и несимметричной, поражая сначала конечности, а позже распространяется выше. Основными признаками выступают:
- болевой синдром в икроножных мышцах, пальцах и кистях рук;
- парестезии конечностей;
- мышечная слабость;
- хромота, изменение походки.
Какими методами диагностики можно уточнить причину полинейропатии?
Для уточнения причин, вызвавших распространенное поражение периферических нервов необходимо тщательное обследование:
- комплексное лабораторное исследование крови: минимальный объем — развернутый общий и биохимический анализ крови, RW, анти-ВИЧ, HBsAg и анти-HCV, уровень витаминов В1, В6, В9, В12, гомоцистеин (при необходимости, в каждом случае индивидуально, спектр лабораторного обследования расширяется)
- при подозрении на наследственную нейропатию — молекулярно-генетический анализ (поиск мутаций в гене PMP22, панель «нервно-мышечные заболевания» или полное геномное секвенирование) и т.д.;
- электрофорез белков сыворотки и мочи с иммунофиксацией + freelite;
- люмбальная пункция с общим анализом ликвора;
- инструментальное общесоматическое обследование, в том числе онкоскрининг (КТ легких, УЗИ молочных желез, маммография, УЗИ простаты и мошонки, ЭГДС, колоноскопия, УЗИ органов брюшной полости и малого таза, ПЭТ-КТ и т.д.).
План обследования составляется индивидуально!
Остановить и восстановить
Лечением данного заболевания занимается врач. Лечение полинейропатии проводится комплексно. Правильная диагностика позволяет определить причину разрушения нервов и остановить процесс. Параллельно проводится комплекс мероприятий по восстановлению уже поврежденной нервной ткани. Дефицит витаминов группы В принимает участие в патогенезе целого ряда заболеваний центральной и периферической нервной системы.
Недостаток каждого из витаминов группы В приводит к формированию полиневропатии. При хроническом дефиците тиамина в пище развивается дистальная сенсорно–моторная полиневропатия, напоминающая алкогольную и диабетическую полиневропатии. Дефицит пиридоксина приводит к возникновению дистальной симметричной, преимущественно сенсорной полиневропатии, проявляющейся ощущением онемения и парестезиями в виде «покалывания иголками». Витамины этой группы являются одними из наиболее часто применяемых в неврологии препаратов.
Важнейшую роль в восстановлении нерва играют витамины В1 и В6, которые напрямую участвуют в процессах роста и формирования нервных клеток.
Одним из популярных комплексов выступает витаминный комплекс Мильгамма® композитум, в состав которого входит бенфотиамин — разработанный в Японии тиамин нового поколения, максимально доступный к усвоению — усваивается почти в 5 раз лучше, чем обычный тиамин. Вторым важным элементом препарата является пиридоксин, который в сочетании с бенфотиамином способствует восстановлению энергетического баланса нервных клеток, помогает усвоению микронутриентов, необходимых для восстановления нервной ткани. Доза пиридоксина в составе Мильгамма® композитум оптимальна, более высокие дозы могут привести к сенсорной нейропатии.
Принимать Мильгамму композитум следует по 1 таблетке в день. В острых случаях после консультации врача доза может быть увеличена до 1 таблетки 3 раза в день. В рамках комплексной терапии препарат обеспечивает долгосрочный эффект за счет оптимального состава для восстановления нервных волокон.
Источники:
- Michael Rubin , MDCM, New York Presbyterian Hospital-Cornell Medical Center// Полинейропатия — 2019
- Курушина О.В., Барулин А.Е. Полинейропатии при соматических заболеваниях: роль невролога в диагностике и лечении// РМЖ (Русский медицинский журнал):
- И.А. Строков, Л.Т. Ахмеджанова, О.А. Солоха Эффективность витаминов группы В при лечении болевых синдромов// Неврология, ТОМ 18, № 10, 2010
- https://www.neurology.ru/centr-zabolevaniy-perifericheskoy-nervnoy-sistemy-fgbnu-ncn/polineyropatiya, дата обращения 19.07.2021
- Пилипович А.А. Применение витаминов группы В в терапии полинейропатии разного генеза. CardioСоматика. 2018; 9 (2): 36–42. DOI: 10.26442/2221-7185_2018.2.36-42
- И.А. Строков «Витамины группы В в лечении неврологических заболеваний», РМЖ ТОМ 17, № 11, 2009.
РУ П N012551/01
RU.MILGCOMP 21.09
Полинейропатия представляет собой поражение периферических нервов и кровеносных сосудов, которые обеспечивают их питанием. Этот патологический процесс иногда называют полиневропатией, изменяя одну букву, нейропатией, полирадикулонейропатией или полиневритом, однако последнее (полиневрит) воспринимается как воспаление, а для периферических нервов истинный воспалительный процесс как-то не характерен, он если и встречается, то очень редко.
Основу полинейропатий составляют другие факторы: нарушение обмена (яркий пример – диабетическая полинейропатия), ишемические факторы, механические повреждения, которые и дают морфологические изменения в нервных волокнах. И даже инфекция, попавшая в нервные волокна, не дает типичного воспаления, а проявляется, как аллергическая реакция. Вот поэтому слово «полиневриты» постепенно уходит из терминологии.
Если, помимо периферических нервов, нарушения затрагивают корешки спинного мозга, болезнь начинают называть полирадикулонейропатией. Патологический процесс наиболее заметен при поражении дистальных отделов ног (полинейропатия нижних конечностей) – его выдает характерная «петушиная походка» больного.
Причины развития данной патологии самые разнообразные, практически любой фактор, оказавший отрицательное воздействие на организм хотя бы один раз, способен привести к возникновению болезни, при этом отдельные случаи заболевания навсегда остаются загадкой.
Как понять диагноз?
В большинстве случаев пациенты в «диагнозе» видят не просто слово «полинейропатия», обычно к нему добавлено некое определение. И если слова «алкогольная» или «токсическая» более-менее понятны людям, то другие термины («аксональная» и «демиелинизирующая») вызывают вопросы. Чтобы читателю были понятны значения этих определений, придется, опираясь на данные различных источников, сделать попытку как-то классифицировать эту патологию, поскольку общепринятого варианта классификации на сегодняшний день пока не разработано.

По происхождению выделяют следующие формы полиневропатии:
- Алиментарную.
- Наследственную.
- Аутоиммунную.
- Метаболическую (печеночная, уремическая, диабетическая полинейропатия).
- Токсическую.
- Инфекционно-токсическую.
Между тем, в литературе можно встретить и другое деление болезни по этиологическому фактору, где различают: воспалительные, хотя истинное воспаление относят к разряду крайне редких, токсические, аллергические и травматические варианты.
демиелинизация при нейропатии
В зависимости от типа патологического процесса выделено две формы заболевания и, похоже, мнения здесь не расходятся:
- Аксональная полинейропатия – она возникает при повреждении аксона;
- Демиелинизирующая – формируется от демиелинизации нервных волокон.
Следует отметить, что эти две формы недолго, а поэтому не всегда, существуют в чистом виде: при первичном поражении аксона как вторичная патология присоединяется демиелинизирующий компонент, а при демиелинизации – аксональный.
Нет особых разногласий в отношении классификации полинейропатии по характеру течения, поэтому в описании болезни можно встретить:
- Острые процессы;
- Подострый вариант;
- Хроническое течение.
Кроме этого, в зависимости от преобладания симптомов того или иного вида нейропатии, различают моторную, сенсорную вегетативные формы, которые, однако, в изолированном виде случаются довольно редко, чаще отмечаются моторно-сенсорные или сенсорно-вегетативные типы болезни.
Описать (или только перечислить) все виды нейропатии достаточно сложно – их очень много, однако следует иметь в виду, что независимо от этиологического фактора все формы имеют общие клинические проявления, которые в такой же степени, как и происхождение, определяют терапевтический подход и прогноз заболевания.
Симптомы полинейропатии
типичные зоны поражения при полинейропатии
Системное поражение периферических нервов относят к главным клиническим проявлениям, характерным для всей группы нейропатий и не столь важно: какому типу принадлежит и в каком направлении движется патологический процесс – основные симптомы будут присутствовать:
- Мышечная слабость и атрофия;
- Снижение сухожильных рефлексов;
- Периферические парезы;
- Расстройство чувствительности в дистальных отделах конечностей (гипостезии, парастезии, гиперстезии);
- Трофические вегетативно-сосудистые нарушения.
Демиелинизирующие ПНП проявляются, в основном, страданием крупных миелиновых (двигательных и чувствительных) нервных волокон, в то время как безмиелиновые вегетативные и чувствительные нервы, обеспечивающие поверхностную чувствительность, не вовлекаясь особо в процесс, остаются в целости и сохранности. Данный вариант болезни проявляется выпадением глубоких рефлексов и нарушением вибрационных ощущений с относительным сохранением поверхностной чувствительности. Демиелинизация, затрагивая не одни лишь дистальные отделы конечностей, с течением времени расширяет границы и начинает распространяться на корешки, проявляясь:
- Периферическими парезами;
- Слабостью конечностей (дистальных отделов);
- Утолщением нервов в случае хронического течения.
Такая полинейропатия нижних конечностей не принадлежит к необратимым процессам. При условии устранения этиологического фактора и проведения адекватного лечения миелиновые оболочки восстанавливаются и в течение 1,5 – 2 месяцев происходит регресс неврологической симптоматики.
Аксональные нейропатии могут затрагивать волокна разного вида с постепенным развитием патологического состояния. К характерным симптомам такого рода ПНП можно отнести:

- Чувствительные (болевые, температурные) нарушения;
- Вегетативные расстройства;
- Отсутствие нарушений глубоких рефлексов на раннем этапе болезни.
Вряд ли можно ожидать полного восстановления утраченных функциональных способностей в случае аксонопатии. Аксоны регенерируются медленно, а отростки сохранившихся аксонов, хоть и пытаются компенсировать потерю, но не имеют возможности сделать это в полной мере.
Однако, учитывая то, что для получения хорошего эффекта от терапевтических мер, прежде всего, важен причинный фактор, его поиску уделяется особое внимание.
Какие факторы заставляют страдать периферические нервы?
поражение НК при диабете
Сахарный диабет – главная причина
Чаще всего нейропатию имеют в виду, когда говорят об осложнениях весьма распространенного по всему земному шару заболевания – сахарного диабета (диабетическая нейропатия, диабетическая стопа), поэтому нельзя не подчеркнуть его главенствующее положение в списке причин. Поражение мелких сосудов при сахарном диабете отмечается у половины и более пациентов, страдающих сахарным диабетом. Когда проявит себя болезнь – прогнозировать сложно, это может случиться еще в начале заболевания и стать первыми симптомами СД, или развитие заболевания может отложиться на неопределенный срок, исчисляемый многими годами.
Главным фактором, запускающим механизм развития диабетической нейропатии выступает ишемический компонент и метаболические расстройства в нервном волокне.
Появление первых неврологических признаков диабетической полинейропатии (ощущение вибрации на лодыжках укорачивается, ахилловы рефлексы снижаются) не дает основания полагать, что болезнь начнет стремительное развитие. С этими симптомами диабетик может прожить долгие годы, не предъявляя иных жалоб до начала прогрессирования процесса, когда клиническая картина приобретает типичную для нейропатии окраску:
- Появляется сильная, очень мучительная болезненность в стопах и голенях, которая в тепле и в покое приобретает еще большую остроту;
- Стопы становятся слабыми;
- Начинает страдать вегетативная иннервация;
- Интенсивность болей с течением времени продолжает нарастать – они становятся нестерпимыми;
- Одновременно с нарастанием болей появляется зуд (не всегда, но очень часто), изменяется цвет кожных покровов (от фиолетового до черного);
- Формируется диабетическая стопа, что приводит не только к снижению функциональных возможностей нижних конечностей, но нередко является причиной их ампутации.
Полинейропатия нижних конечностей, развивающаяся на фоне сахарного диабета – это наиболее частое серьезное осложнение «сахарной» болезни 2 типа и головная боль эндокринологов, поэтому установленный диагноз (СД) уже является поводом для профилактики поражения нервных волокон, а появление первых признаков – для пересмотра терапии в сторону повышения эффективности. Помимо мероприятий, направленных на компенсацию основного заболевания (СД), назначается лечение, предусматривающее улучшение кровоснабжения, снимающее отечность, препятствующее проникновению инфекции (антибактериальная терапия местно).
Диабетическая нейропатия, видео – программа “Жить здорово!”
Запустить механизм формирования нейропатии и сделать ее сопутствующей, кроме сахарного диабета могут и другие заболевания: гематологическая патология, коллагенозы, билиарный цирроз, новообразования, гипотиреоз, множественная миелома и пр.
Дефицит витаминов группы В
Дефицит отдельных витаминов из группы В (В1, В12, В6), которые от природы обладают нейротропным эффектом (положительно влияют на ЦНС и периферические нервы), поэтому в медикаментозной форме используются в качестве важных средств патогенетического лечения. Естественно, если в организме по каким-либо причинам сложится недостаток этих витаминов, который не будет быстро восполнен, то в скором времени заявят о себе симптомы хронической аксональной полинейропатии.:
- Дефицит витамина В1 (тиамин) вызывает нейропатию нижних конечностей, напоминающую диабетическую или алкогольную;
- Недостаток В6 (пиридоксин) – формирует преимущественно сенсорные нарушения, проявляющиеся онемением и покалыванием;
- Нехватка В12 (цианокобаломин) – чаще всего приводит к дегенерации спинного мозга и поражению задних канатиков, иногда – к развитию сенсорных нарушений с онемением и покалыванием.
Основным методом лечения полинейропатии подобного типа является введение витаминов группы В и аскорбиновой кислоты в терапевтических дозах, а также диета, насыщенная данными полезными веществами.
Токсическая форма
Токсическая форма заболевания с поражением черепных нервов может развиваться, как осложнение инфекционного процесса, вызываемого такими агентами, как бацилла Леффлера (дифтерийная палочка – дифтерийная нейропатия), вирус герпеса, вирус иммунодефицита человека (ВИЧ).
Тяжелые интоксикации, развивающиеся вследствие проникновения в кровь чуждых человеческому организму веществ, которые попадают туда случайно или преднамеренно с целью свести счеты с жизнью: мышьяк, метанол, который путают с этанолом, угарный газ, дихлофос и другие фосфорорганические (или просто ядовитые) химические соединения. Токсическую полинейропатию формирует и хроническое употребление алкогольных напитков, разница лишь в том, что вышеперечисленные яды действуют очень быстро и поражают нервы за 2-4 дня, вызывая острую аксональную полинейропатию, а алкоголик травит свой организм месяцами и годами, создавая почву для прогрессирования патологического процесса. В большинстве случаев в течение полугода страдающий алкоголизмом человек «использует свои шансы» получить данную болезнь.

Алкогольная полинейропатия развивается у 2 – 3% людей, не знающих меры в горячительных напитках, и находится на втором месте после диабетической. Основную роль в формировании патологического процесса играют 2 фактора: 1) токсическое действие этанола на нервную систему, 2) метаболические нарушения в нервах. От влияния алкоголя страдают не только периферические нервы, определенные изменения затрагивают также головной и спинной мозг.
Симптомы алкогольной полинейропатии развиваются постепенно:
- Боли в икрах, усиливающиеся при надавливании, и парестезии в дистальных отделах появляются первыми;
- Несколько позже приходит слабость и параличи, которые касаются как верхних конечностей, так и нижних;
- Паретичная мускулатура быстро начинает атрофироваться;
- Глубокие рефлексы повышаются, зоны их расширяются;
- Начинает проявляться нарушение поверхностной чувствительности по типу носков и перчаток;
- Углубление клинических проявлений при отсутствии лечения может привести к тому, что внешние признаки ПНП начинают напоминать спинную сухотку при сифилисе, однако отсутствие характерных симптомов (RW – положительная, нарушение мочеиспускания, «прострелы») указывает на иной причинный фактор и другой тип нейропатии, ничего общего с сифилисом не имеющей.
Иногда алкогольная полинейропатия развивается стремительно и происходит это обычно после сильного переохлаждения. Для такого типа характерен широкий диапазон изменений в нервной системе, больные, как правило, имеют «красноречивый» внешний вид и предъявляют массу жалоб. Вазомоторные, секреторные и трофические нарушения являются причиной усиленного потоотделения, отечности дистальных отделов нижних и верхних конечностей, изменению температуры и цвета кожных покровов.
Болевые ощущения при алкогольной полинейропатии могут нарастать в течение нескольких месяцев. Между тем, своевременное лечение, которое включает витаминотерапию, ноотропы, физиотерапевтические процедуры, прозерин, способно повернуть развитие процесса вспять.
В заключение данного раздела следует вспомнить о нейропатии, развивающейся от употребления веществ, предназначенных для лечения и профилактики болезней. Медикаментозная полинейропатия развивается на фоне лечения препаратами, которые трудно отнести к простым: соли золота, висмут, сульфаниламиды, противосудорожные, антибактериальные и химиопрепараты. В иных случаях периферические нервы могут поражаться после похода на прививку (введение вакцин и сывороток).
Травмы, компрессия, переохлаждение и неизвестный фактор
В этом подразделе мы собрали несколько похожие причины, ведь нередко можно слышать, что проявления болезни развились после ушиба или переохлаждения, иногда признаки полинейропатии появились в результате инфекции или вследствие компрессионных синдромов, которыми так богат остеохондроз позвоночника.

Таким образом, причиной нейропатии нередко выступают:
- Травмы. Механическое повреждение нервов в результате травм (ушибов, вывихов, открытых и закрытых переломов, неудачных оперативных вмешательств) может стать причиной нейропатии нижних или верхних конечностей с парестезией, онемением, покалыванием. Например, травматическое нарушение целостности локтевого нерва одной из верхних конечностей дает типичную картину локтевой нейропатии: согнутые безжизненные пальцы, рука с признаками мышечной атрофии, потеря функциональной способности.
-
связь уровня поражения позвоночника с органами
Компрессия нервных корешков. Компрессионный синдром при остеохондрозе или грыже межпозвоночных дисков, где симптомы страдания периферических нервов чаще носят преходящий характер, может стать причиной радикулопатии как верхних конечностей, так и нижних, сопровождаемой двигательными, чувствительными и вегетативными расстройствами. Дегенеративно-дистрофические изменения в большей степени касаются нижних отделов позвоночника (остеохондроз и его последствия) и при отсутствии или неэффективности лечения нередко приводят к компрессии нервных корешков, которая может легко обернуться развитием нейропатии нижних конечностей. Компрессионный синдром, возникающий в результате прогрессирования ревматоидного артрита, развития опухоли, проведения медицинских манипуляций, грозит ущемлением нервов верхних конечностей, что зачастую вытекает в нейропатию плечевого сплетения (плечевой плексит) или локтевую нейропатию.
- Переохлаждение. Наряду с другими факторами (отит, сахарный диабет, травмы, инсульт, операции, опухоль, стоматологические манипуляции), влияние сквозняка и холода становится причиной возникновения такого воспалительного процесса, который заметно меняет не в лучшую сторону внешний вид (лицо перекошено, глаз не закрывается) и доставляет дополнительные неудобства (нарушение вкуса, иногда поражение слезных желез). Название этой болезни – нейропатия лицевого нерва.
- К загадочным формам болезни, поскольку происхождение до конца не определено, относят некоторые наследственные формы, а также острую воспалительную демиелинизирующую полирадикулоневропатию, называемую синдромом Гийена-Барре. Известно, что синдром Гийена-Барре нередко дает о себе знать вслед за острой инфекцией, перенесенной человеком и, возможно, вызванной фильтрующимся вирусом, который, кстати, тоже пока не выделен. Многие авторы относят данный синдром к своеобразному проявлению аллергической реакции и рассматривают патологический процесс, как аутоиммунную патологию.
Особый интерес вызывает полинейропатия, которую первоначально назвали послеродовым полиневритом. При дальнейшем изучении этого патологического состояния выяснилось, что оно не настолько послеродовое и способно развиваться на любом сроке беременности, поэтому сейчас болезни дано другое название – полинейропатия беременных.
Происхождение ПНП беременных связывают:
- С недостатком витаминов (группы В – в особенности) во время беременности;
- С повышенной чувствительностью к белкам, которые попадают в организм женщины от плаценты и плода и являются для нее чужеродными;
- С токсическим влиянием продуктов обмена на периферические нервы.
Симптомы полинейропатии нижних конечностей (парестезии, парезы, параличи и боли) появляются на фоне полного благополучия, однако нередко развитие болезни на этом не заканчивается и к симптомам ПНП присоединяются признаки интоксикации (общая слабость, тошнота, рвота и пр.).
Основное лечение данной патологии – назначение витаминных комплексов, содержащих витамины группы В, десенсибилизирующая терапия.
Наследственность
Наследственные нейропатии представляют неоднородную группу патологических состояний: некоторые мутации генов обусловливают один единственный признак, а другие, наоборот, дают массу различных симптомов, среди которых проявляет себя поражение периферических нервов.

К метаболическим нейропатиям относят амилоидозы, полученные по наследству, а также порфирии и нарушения липидного обмена того же происхождения. Загадочные формы представляют наследственные моторно-сенсорные (синдром Шарко-Мари-Тута) и сенсорно-вегетативные типы (болезнь Фабри). В качестве примера наследственных ПНП приведем болезнь Фабри (признак, сцепленный с полом, лизосомная болезнь накопления), при которой нейропатия выступает как один из многочисленных симптомов. Поскольку ген, контролирующий данную патологию, находится в Х-хромосоме, преимущественно болеют мужчины, что объяснимо – они имеют только одну Х-хромосому и, если она оказалась дефектной, болезнь неизбежна. Однако известны случаи заболевания женщин, но почему это происходит – от генетиков до сих пор однозначного ответа не последовало. Заболевание имеет богатую симптоматику (непереносимость нагрузок, снижение потоотделения, поражение внутренних органов) и характерный внешний вид больного (акромегалия). Проявления нейропатии в одинаковой мере могут затрагивать и нижние и верхние конечности: ступни и ладони испытывают постоянное жжение, онемение, болезненность. Симптомы усугубляются при кризе, который провоцируется стрессом, холодовым или тепловым воздействием.
Лечение
Хотя лечение полинейропатии определяется с учетом причинного фактора и предусматривает воздействие на основное заболевание, вызвавшее поражение периферических нервов, терапевтические меры должны быть комплексными с одновременной направленностью на ликвидацию симптомов ПНП.
Проблема лечения метаболических форм ПНП, коими в первую очередь являются самые распространенные типы: диабетическая полинейропатия (осложнение сахарного диабета 2 типа) и алкогольная полинейропатия (следствие хронической алкогольной интоксикации). Как правило, эти, а нередко и другие, нейропатии сопровождаются интенсивным болевым синдромом и выраженным нарушением чувствительности. Для уменьшения клинических проявлений современная медицина предлагает различные методы лечения:
- Витаминотерапия. Комбинированные препараты, содержащие в фармацевтических дозах витамины В1, В6, В12 (нейромультивит, мильгамма), идут в числе первых. Они дают хороший обезболивающий эффект, ликвидируют расстройство чувствительности за счет улучшения способности нервов к восстановлению своих структурных компонентов, осуществляют антиоксидантную защиту. К лечению ПНП привлекают природные формы перечисленных витаминов, комбинируя их, а также другие лекарственные средства данной фармакологической группы (витамины А, С, Е).
-
Обезболивающие препараты. Для купирования боли применяют, в основном, ненаркотические анальгетики (аспирин, трамал) и нестероидные противовоспалительные (НПВП), однако при сильных болевых ощущениях в иных случаях назначают кодеин и даже морфий. К анальгезирующей терапии считают целесообразным добавлять Магне В6, который повышает эффективность лечения анальгетиками.
- Глюкокортикоиды, плазмаферез, иммуносупрессанты. Последние результаты научных исследований показали, что в патогенезе некоторых ПНП основная роль принадлежит сбоям в тканевом иммунитете, поэтому длительная иммуномодуляция с помощью медикаментозных средств весьма себя оправдывает. В данных случаях используют такие препараты, как азатиоприн, циклоспорин, облучение лимфатической системы + циклофосфан. Однако при тяжелом состоянии пациента иммуносупрессанты нередко комбинируют с гормонами или плазмаферезом (азатиоприн + преднизолон, азатиоприн + плазмаферез). Нередко в качестве вспомогательного лекарства назначают эрбисол, который представляет собой комплекс природных органических соединений, обладающий многонаправленным действием (иммуномодулирующее, противовоспалительное, антиоксидантное, мембрано-стабилизирующее). Между тем, схемы гормонотерапии (преднизолон, метилпреднизолон) с нарастанием и убыванием дозы (с учетом состояния пациента) определяет только врач. Он же комбинирует гормонотерапию с иммуноглобулинами (иммуноглобулин человека нормальный, сандоглобулин) или плазмаферезом. Данные мероприятия проводятся в стационарных условиях.
- Другие препараты. При полинейропатии назначаются и другие лекарственные средства: способствующие ускорению утилизации глюкозы, улучшению питания тканей и реологических свойств крови, обладающие мочегонным, сосудорасширяющим, венотоническим действием (все эти качества содержит в себе инстенон), а также препараты, улучшающие клеточный метаболизм (актовегин) и нервно-мышечную проводимость (прозерин), нормализующие кровоток в микроциркуляторном русле (трентал), регулирующие окислительно-восстановительные реакции в тканях (фосфаден). В отдельных случаях проводится дезинтоксикационная или десенсибилизирующая терапия. В листке назначений больного ПНП можно встретить широкий круг препаратов из различных фармакологических групп: церебролизин, оксипин, пикамелон, энкад, пантотенат кальция… Что назначить и чем это обосновать – подумает доктор.
Полинейропатия (в зависимости от своего происхождения и клинических проявлений) иногда надолго может приковать пациента в кровати. И он сам, и, особенно, его близкие должны помнить, что не все во власти химических соединений, называемых лекарствами. Немалую роль играет правильное питание, реабилитационные мероприятия и, особенно – уход и забота.



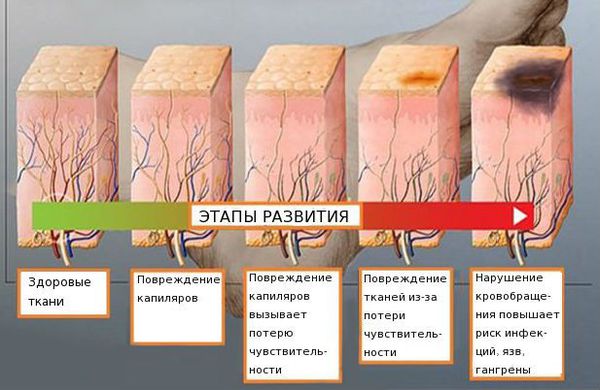
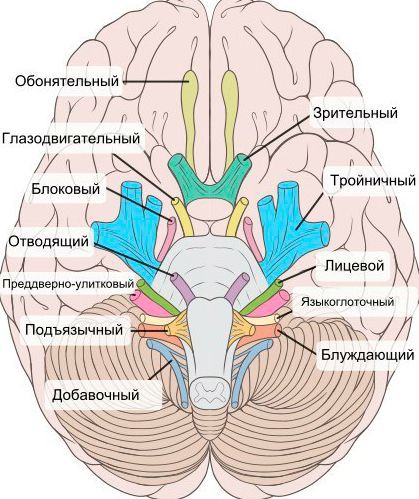
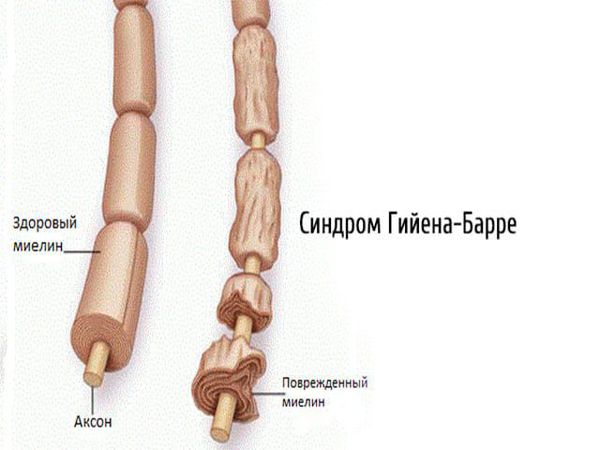






 Обезболивающие препараты. Для купирования боли применяют, в основном, ненаркотические анальгетики (аспирин, трамал) и нестероидные противовоспалительные (НПВП), однако при сильных болевых ощущениях в иных случаях назначают кодеин и даже морфий. К анальгезирующей терапии считают целесообразным добавлять Магне В6, который повышает эффективность лечения анальгетиками.
Обезболивающие препараты. Для купирования боли применяют, в основном, ненаркотические анальгетики (аспирин, трамал) и нестероидные противовоспалительные (НПВП), однако при сильных болевых ощущениях в иных случаях назначают кодеин и даже морфий. К анальгезирующей терапии считают целесообразным добавлять Магне В6, который повышает эффективность лечения анальгетиками.