Российский государственный медицинский университет;
НИИ цереброваскулярной патологии и инсульта, Москва
Аксональные полинейропатии: патогенез и лечение
Как цитировать:
Ковражкина Е.А. Аксональные полинейропатии: патогенез и лечение. Журнал неврологии и психиатрии им. С.С. Корсакова.
2013;113(6):22‑25.
Kovrazhkina EA. Axonal polyneuropathies: pathogenesis and treatment. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2013;113(6):22‑25. (In Russ.)

Полинейропатия (ПНП) — заболевание периферической нервной системы, развивающееся в результате диффузного поражения периферических нервов — их аксонов (аксональные полинейропатии), миелиновой оболочки (демиелинизирующие полинейропатии) либо тел нейронов (нейронопатии) [9]. В основе патогенеза полинейропатий аксонального типа лежит генерализованное повреждение осевых цилиндров периферических нервов.
Патогенез. Аксональная дегенерация (аксонопатия) — результат нарушения метаболизма нейрона вследствие недостаточной выработки энергии в митохондриях и/или нарушения аксонального транспорта. Миелиновая оболочка при аксонопатиях страдает вторично (вторичная демилинизация). Миелин может повреждаться в результате ишемии нервов (поражения vasa nevrorum), отложения токсичных для нерва веществ или иммунных комплексов в эндоневрии (что характерно, например, для сахарного диабета, особенно 1-го типа — с высокой гипергликемией и аутоиммунными нарушениями) [4]. Соответственно, среди причин аксонопатии периферических нервов указывают нарушения метаболизма, токсические влияния, ишемию нервных стволов, наследственную предрасположенность и аутоиммунные механизмы [5]. По этиологическому фактору подавляющее большинство аксональных ПНП составляют метаболические и токсические, среди которых первое место занимают диабетическая (до 50% среди пациентов с сахарным диабетом и до 90% поражений нервной системы при диабете [9, 12]) и алкогольная (до 50% среди больных алкоголизмом [2, 9]).
Причиной токсико-метаболических ПНП является экзо- и эндогенные интоксикации. Поступающие извне вещества или собственные его метаболиты, токсичные для периферических нервов, вызывают их повреждение. Тяжесть этого повреждения зависит от степени токсичности данного агента (выделяют острые метаболические ПНП, развивающиеся на фоне тяжелой общей интоксикации, например, ПНП при быстро нарастающих печеночной недостаточности или уремии, при отравлении фосфоорганическими веществами, мышьяком, свинцом, как нежелательный эффект лечения препаратами лития, цитостатиками), длительности его воздействия, собственных генетических особенностей метаболизма нервной ткани, немаловажную роль играет также аутоиммунный фактор [13].
Большинство часто встречающихся в клинике метаболических ПНП являются итогом длительного воздействия эндо- и экзогенного токсического агента (диабетическая, печеночная, уремическая, алкогольная, профессиональная, лекарственная). Результатом такой интоксикации является повреждение осевого цилиндра аксона. Клинически это проявляется не только нарушениями чувствительности и мышечной слабостью (что свойственно и для демиелинизирующих ПНП), но и мышечными гипотрофиями, выраженными трофическими нарушениями. Все эти признаки свидетельствуют о длительном страдании аксонов периферических нервов. При электронейромиографии (ЭНМГ) выявляется снижение (иногда — вплоть до полного отсутствия) амплитуды сенсорных потенциалов и М-ответов периферических нервов. У пациентов с ПНП аксонального типа зачастую в достаточной степени сохранены двигательные функции (отсутствуют выраженные парезы, больные сохраняют способность ходить, часто без дополнительной опоры), тогда как инвалидизирующими являются чувствительные (боли и парестезии) и трофические нарушения. Так, аксональная сенсомоторная ПНП является одним из важных патогенетических факторов развития синдрома диабетической стопы [3]. Аксональное повреждение нервов развивается медленно, исподволь, но при правильном лечении потенциально обратимо.
При массивном воздействии токсичного для периферической нервной системы агента, участии ишемического компонента (за счет страдания vasa nevrorum), аутоиммунных влияний развиваются ПНП аксонально-демиелинизирующего типа такие, например, как уремическая, свинцовая, амиодароновая, вызываемые воздействиями высокотоксичных для нервов веществами [9]. При наиболее распространенной диабетической ПНП, демиелинизирующий компонент максимально представлен при инсулинпотребном сахарном диабете (характеризующимся более высокой гипергликемией), а выраженность демиелинизации периферических нервов нарастает при резких повышениях уровня глюкозы крови [4, 7]. На представленность демиелинизирующего компонента при метаболических ПНП влияют наследственные факторы (генетически обусловленная миелинопатия, которая протекала бы субклинически без дополнительного воздействия токсического агента), аутоиммунное повреждение (например, миелинопатия более выражена при сахарном диабете 1-го типа, при котором иммунокомпетентные клетки повреждают ткань поджелудочной железы) [4, 14].
ПНП аксонально-демиелинизирующего типа протекают более тяжело, с выраженными парезами, сенситивной атаксией, нейропатическим болевым синдромом, но нередко, при своевременном устранении действия токсического фактора, быстро регрессируют. При очень тяжелом и упорном течении заболевания, учитывая роль аутоиммунного механизма в развитии данного типа метаболических ПНП, необходимо кратковременное назначение иммуномодулирующей терапии (чаще глюкокортикоидов, иногда цитостатиков) [9, 11].
Клиническое течение ПНП. Как уже было сказано, при длительном воздействии умеренно токсичного для нервов агента аксонопатия развивается медленно, что не всегда заметно. Преимущественное поражение бедно миелинизированых вегетативных и сенсорных волокон вызывает парестезии, повышенную холодовую чувствительность кистей и стоп, негрубые трофические нарушения. При ЭНМГ не всегда удается выявить характерные признаки сенсорной и моторной аксонопатии — снижение амплитуд сенсорных потенциалов и М-ответов — если исследуются крупные богато миелинизированные нервы, аксоны которых страдают позднее. Быстрее выявляются признаки вторичной миелинопатии, как клинические — присоединение нейропатических болей, парезов, так и миографические — снижение скорости распространения возбуждения (СРВ) по нервам.
При условии адекватной терапевтической стратегии — устранения действия повреждающего периферические нервы фактора, назначение препаратов, влияющих на метаболизм нервной ткани, — наступает ремиелинизация, что отражается и на ЭНМГ в виде нарастания СРВ, и клинически — в виде регресса парезов и нейропатических болей, улучшения чувствительности. Однако, если полинейропатия развивалась в условиях длительного действия токсического агента, поражение аксонов периферических нервов, снижение амплитуд сенсорных потенциалов и М-ответов на ЭНМГ сохраняется, поскольку осевые цилиндры нервов обладают гораздо меньшей способностью к регенерации, чем миелин.
Так, в проведенном исследовании [8], посвященном лечению алкогольной ПНП, ведущим ЭНМГ-признаком поражения периферических нервов у большинства пациентов имелось снижение СРВ. В условиях элиминации токсического фактора (в данном случае приема алкоголя) и лечения препаратом α-липоевой кислоты (берлитион в суточной дозе 600 мг), у пациентов быстро, в течение 1-го месяца, регрессировали ЭНМГ и клинические признаки миелинопатии — уменьшалась выраженность парезов и болевого синдрома (в баллах по визуальной аналоговой шкале с 5,2±1,0 до 2,6±0,5) достоверно (р<0,05) нарастала СРВ (по моторным волокнам n. tibialis с 36,93±1,12 до 42,22±0,8 м/с, по сенсорным волокнам n. suralis c 32,45±0,70 до 38,24±0,50 м/с), но признаки аксонопатии (снижение амплитуд сенсорных и моторных ответов периферических нервов, сенсорные выпадения по полиневритическому типу, трофические нарушения) сохранялись и после 6 нед лечения.
Таким образом, можно представить следующую схему развития и течения метаболических ПНП (см. таблицу): высокотоксичные, высококонцентрированные токсические агенты приводят к развитию полинейропатии аксонально-демиелинизирующего типа (в развитии которых также значительную роль играют наследственный, сосудистый, аутоиммунный факторы), длительно действующие эндо- и экзогенные яды приводят преимущественно к страданию аксонов с умеренно выраженным вторичным поражением миелина (так как постоянно идет процесс ремиелинизации) [7].
Лечение. Аксональное повреждение нервов как первичного, так и вторичного характера, обратимо за счет регенерации поврежденных аксонов и концевого спрутинга сохранившихся аксонов, однако этот процесс протекает медленно (месяцы), часто аксональная регенерация бывает неполной. Для регресса аксонопатии периферических нервов необходимо нивелировать воздействие токсического агента (коррекция метаболических и алиментарных нарушений, детоксикация, влияние на аутоиммунные механизмы), большое значение имеет также патогенетическая терапия, направленная на восстановление нарушенного метаболизма аксонов (митохондриальные нарушения, повреждения, вызванные окислительным стрессом).
Таким образом, в патогенетическом лечении аксональных ПНП, в зависимости от их нозологического и клинико-электрофизиологического варианта, должны присутствовать детоксикация и коррекция метаболических и алиментарных нарушений; сосудистая терапия (дезагреганты, венотоники, пентоксифиллин, вазопростан); препараты, воздействующие на универсальные механизмы поражения аксонов (витамины и витаминоподобные препараты); при необходимости — воздействие на аутоиммунные компоненты (глюкокортикоиды, плазмаферез). В некоторых случаях, когда представленность миелинопатии в структуре поражения периферических нервов велика и трудно отличить токсико-метаболическую полинейропатию от воспалительной (например, синдром Гийена-Барре у пациента с алкоголизмом или дебют хронической воспалительной демиелинизирующей ПНП у больного с сахарным диабетом) необходимо проводить пробную иммуномодулирующую терапию, ее быстрая эффективность позволит высказаться в пользу превалирования у пациента аутоиммуного механизма поражения периферических нервов [7, 11].
В лечении всех метаболических ПНП необходимо устранить (по возможности) поражающий периферические нервы яд и использовать препараты, улучшающие метаболизм нервной ткани периферических нервов. Последние необходимо применять в течение длительного времени, так как первым эффектом данных препаратов будет ускорение ремиелинизации, но для восстановления самих аксонов — а данные ПНП являются аксональными — требуется значительно большее количество времени.
α-липоевая (тиоктовая) кислота — витаминоподобное вещество, эндогенно образующееся в организме, как кофермент участвует в окислительном декарбоксилировании α-кетокислот. Основная функция эндогенной липоевой кислоты в организме — участие в аэробном метаболизме продукта гликолиза пирувата. Тиоктовая кислота является коферментом в окислительном декарбоксилировании пировиноградной кислоты до ацетил-КоА и α-кетоглутаровой до сукцинил-КоА в цикле Кребса. Облегчая превращение молочной кислоты в пировиноградную с последующим декарбоксилированием последней, α-липоевая способствует ликвидации метаболического ацидоза [6]. Тиоктовая кислота обладает сложным комплексным действием: гипогликемическим, липотропным, гепатопротекторным, антиатеросклеротическим, является мощным антиоксидантом. Липоевая кислота может существовать в окисленной (-S-S-) и восстановленной (SH-)-формах, благодаря чему реализуются ее коферментные и антиоксидантные функции. Восстановленная форма, дигидролипоевая кислота, служит донором электронов для восстановления других антиоксидантов (витамины С, Е и глутатион), осуществляет рецикл витамина Е при его истощении. Дигидролипоат повышает интра- и экстрацеллюлярный уровни глутатиона — эндогенного антиоксиданта.
Эффект экзогенно вводимой α-липоевой кислоты в отношении полиневритического синдрома впервые обнаружен при сахарном диабете. Обусловленная сахарным диабетом гипергликемия приводит к отложению глюкозы на матричных протеинах кровеносных сосудов и образованию конечных продуктов прогрессирующего гликозилирования, в результате чего уменьшается эндоневральный кровоток, возникает эндоневральная ишемия. α-липоевая кислота приводит к снижению уровня глюкозы в крови и повышению содержания гликогена в печени, обладает гипогликемическим действием. На фоне воздействия препарата уменьшается выраженность сенсорных симптомов полинейропатии — боли, жжения, ощущения онемения и «ползания мурашек» в конечностях.
Применение α-липоевой кислоты оказывает положительное влияние на универсальные механизмы аксонального повреждения, такие как повреждающее действие окислительного стресса и митохондриальная дисфункция — за счет антиоксидантного действия, повышения содержания глутатиона. Энергокорригирующее действие α-липоевой кислоты, тропное именно к аксонам нервов, способствует, в конечном итоге, быстрейшей регенерации аксонов [18].
Препарат не только редуцирует проявления окислительного стресса, но и оказывает влияние на сосудистый компонент поражения периферических нервов, нормализуя эндоневральный кровоток (что имеет большое значения, например, при дибетической микроангиопатии) [16, 17]. Комплексный механизм действия α-липоевой кислоты объясняет ее эффективность в отношении всех аксональных ПНП, патогенез которых связан с токсико-дисметаболическим и сосудистым факторами. Так, эффективность тиоктовой кислоты показана при уремической и алкогольной ПНП, при поражении периферических нервов, индуцированном цитостатиками [15]. Для регенерации аксонов периферических нервов на фоне токсико-метаболических влияний важны также детоксикационный и гепатопротекторный эффекты α-липоевой кислоты. Положительный эффект препарата отмечен в отношении заболеваний печени, печеночной комы, некоторых интоксикаций, в том числе алкогольной [6, 10].
При значительно выраженной аксонопатии, учитывая медленную скорость регенерации аксонов, необходимо длительное применение достаточно высоких доз α-липоевой кислоты. Обычно ее суточная доза составляет 600 мг. Предпочтительнее начинать лечение с внутривенного капельного введения препарата — 600 мг (24 мл раствора) в разведении на 200 мл физиологического раствора, длительность инфузии составляет от 2 до 4 нед в зависимости от тяжести ПНП. В особо тяжелых случаях препарат вводят внутривенно капельно в дозе 1200 мг в сутки. После переходят на пероральный прием α-липоевой кислоты — в таблетках по 600 мг не менее 2 месяцев [1].
В соответствии с такой клинической потребностью — необходимостью длительного приема достаточно высоких доз α-липоевой кислоты, учитывая потенциально обратимый, но медленный характер аксональной регенерации — разработаны и фармацевтические формы препарата. Например, берлитион 300 и берлитион 600, производимые в виде раствора для внутривенных вливаний по 12 и 24 мл соответственно (для начального этапа лечения ПНП), так и таблеток по 300 и 600 мг (для продолжения терапии).
Соблюдение всех условий патогенетического лечения ПНП — нормализация гликемии, прекращение поступления экзогенного яда, детоксикация, коррекция аутоиммунных нарушений, длительное применение препаратов, нормализующих аксональный метаболизм, способствует постепенной регенерации аксонов, уменьшению выраженности чувствительных и двигательных нарушений, болевого синдрома, парестезий, парезов. Для уточнения динамики различных видов метаболических ПНП на фоне подобного терапевтического подхода необходимы дальнейшие исследования.
Полинейропатия — это патология периферической нервной системы, которая развивается в результате диффузного повреждения периферических нервов и их аксонов. Отсюда и название болезни. В ее основе — генерализованное поражение осевого цилиндра периферических нервов.
Что такое аксональная полинейропатия
Полиневропатия (второе название — полиневрит) — это клинический синдром, который возникает из-за ряда факторов, влияющих на периферическую нервную систему, и отличается размытыми патогенетическими изменениями. Заболевание занимает одно из лидирующих мест в перечне недугов периферической нервной системы, уступая первенство только вертеброгенной патологии, превосходящей по сложности клинической картины и последствиям, развивающимся из-за нее.
Аскональная полинейропатия считается междисциплинарной проблемой, с ней часто сталкиваются доктора различных специализаций. В первую очередь с данным заболеванием обращаются к неврологу. Частота возникающего синдрома неизвестна, так как отсутствуют статистические данные.
На данный момент известны всего три важных патоморфологических механизма, которые лежат в истоках формирования полинейропатии:
- валлеровская дегенерация;
- первичная демиелинизация;
- первичная аксонопатия.
В соответствии с иммунологической теорией полинейропатия является результатом перекрестного образования иммунных глобулинов, уничтожающих собственные клетки, в результате чего возникает некроз тканей и мышечное воспаление.
Исследователи выдвигают ряд гипотез возникновения и проблем течения аксональной полинейропатии:
- Сосудистая. Базируется на вовлечении в процесс сосудов, по которым кислород и питательные вещества поступают в периферические нервы. Изменяются характеристики крови по качественному и количественному составу, что может привести к ишемии нервных окончаний.
- Теория оксидативного стресса. Позиционирует формирование болезни со стороны нарушения обмена оксида азота, вследствие чего изменяются калий-натриевые механизмы, лежащие в основе формирования нервного возбуждения и проведения импульсов по нервам.
- Теория деактивации факторов роста нерва. Говорит о том, что болезнь возникает из-за недостатка аксонального транспорта с последующим развитием аксонопатии.
- Иммунологическая. Объясняет развитие заболевания в результате перекрестного образования антител к структурам периферической нервной системы, которое сопровождается аутоиммунным воспалением, а затем и некрозом нервов.
Даже при использовании ультрасовременных методов диагностики сложно найти достоверную причину патологии, выяснить ее получается только у 50-70% пострадавших.
Факторов возникновения полинейропатии нижних конечностей по аксональному типу очень много. Однако даже инновационные способы исследования не позволяют установить истинную этиологию заболевания.
Мнение эксперта
Автор: Алексей Владимирович Васильев
Руководитель НПЦ болезни двигательного нейрона/БАС, кандидат медицинских наук, врач высшей категории
Аксональная полинейропатия — это одно из самых опасных неврологических заболеваний, сопровождающееся поражением периферической нервной системы. При болезни разрушаются периферические нервные волокна.
Причин возникновение аксональной полинейропатии несколько. Самые распространенные:
- Сахарный диабет нарушает структуру крови, питающей нервы, в свою очередь происходит сбой в обменных процессах.
- Длительный дефицит витаминов В. Именно они максимально важны для правильной работы нервной системы, поэтому долгая нехватка способна привести к аксональной полинейропатии.
- Воздействие токсинов на организм. К ним относят разнообразные отравляющие вещества, например, алкоголь, а также ВИЧ. При отравлении опасными веществами заболевание может развиться уже через несколько дней.
- Наследственный фактор.
- Синдром Гийена-Барре.
- Различные травмы, к которым также относится длительное сдавливание нервов, которое характерно при грыже или остеохондрозе.
Лечение аксональной полинейропатии обязательно должно быть комплексным, иначе нужного эффекта достичь не удастся. Категорически запрещается заниматься самолечением и при возникновении первых же симптомов нужно срочно обратиться к доктору. Врачи Юсуповской больницы подбирают лечение индивидуально для каждого пациента. В зависимости от тяжести патологии и симптоматики назначается комплексное лечение под наблюдением опытных специалистов.
Причины
Самые распространенные причины возникновения аксональной полинейропатии нижних конечностей:
- истощение организма;
- длительный недостаток витаминов группы В;
- недуги, ведущие к дистрофии;
- острые инфекции;
- токсическое поражение ртутью, свинцом, кадмием, угарным газом, спиртными напитками, метиловым спиртом, фосфорорганическими соединениями, медицинскими препаратами, принимаемыми без согласования с врачом;
- болезни сердечно-сосудистой, кроветворной, кровеносной и лимфатической систем;
- эндокринологические патологии, в том числе инсулинозависимость.
Главными факторами, которые провоцируют развитие моторной или сенсомоторной аксональной полинейропатии, являются:
- эндогенная интоксикация при почечной недостаточности;
- аутоиммунные процессы, протекающие в организме;
- амилоидоз;
- вдыхание токсических веществ или паров.
Также болезнь может быть обусловлена наследственностью.
Нехватка в организме витаминов группы В, а в особенности пиридоксина и цианокобаламина, крайне негативно воздействует на проводимость нервных и моторных волокон и может вызывать сенсорную аксональную полинейропатию нижних конечностей. Это же происходит при хронической алкогольной интоксикации, глистной инвазии, заболеваниях желудочно-кишечного тракта, которые ухудшают скорость всасывания.
Токсическое отравление лекарственными препаратами, аминогликозидами, золотыми солями и висмутом занимают большой процент в структуре факторов аксональной невропатии.
У пациентов с сахарным диабетом нарушена функция периферических нервов из-за нейротоксичности кетоновых тел, то есть метаболитов жирных кислот. Происходит это из-за невозможности организма использовать глюкозу как главный источник энергии. Поэтому вместо нее окисляются жиры.
При аутоиммунных заболеваниях, протекающих в организме, иммунная система человека атакует собственные нервные волокна, воспринимая их как источник опасности. Это происходит из-за провокации иммунитета, возникающей при неосторожном приеме иммуностимулирующих медикаментов и нетрадиционных методик лечения. Поэтому у людей, которые склонны к возникновению аутоиммунных заболеваний, пусковыми факторами аксональной полинейропатии являются:
- иммуностимуляторы;
- вакцины;
- аутогемотерапия.
При амилоидозе в организме накапливается такой белок, как амилоид. Именно он нарушает основные функции нервных волокон.
Первые признаки
Заболевание обычно начинает развиваться с поражения толстых или тонких нервных волокон. Зачастую аксональная полинейропатия имеет дистальное симметричное распределение на кисти или стопы. Нейропатия чаще всего сначала поражает нижние конечности, а затем симметрично распространяется вверх по телу. К самым частым первичным симптомам поражения относят:
- мышечную слабость;
- болевой синдром в конечностях;
- жжение;
- ощущение ползания мурашек;
- онемение кожных покровов.
Симптоматика ярче всего проявляется в вечернее и ночное время суток.
Симптомы
Врачи подразделяют хроническое, острое и подострое течение аксональной полинейропатии. Заболевание подразделяется на два вида: первично-аксональный и демиелинизирующий. В ходе течения болезни к ней присовокупляется демиелинизация, а затем и вторично аксональный компонент.
К основным проявлениям недуга относятся:
- вялость в мышцах ног или рук;
- спастический паралич конечностей;
- чувство подергивания в мышечных волокнах;
- головокружение при резкой перемене положения тела;
- отек конечностей;
- жжение;
- покалывание;
- ощущение ползания мурашек;
- снижение чувствительности кожных покровов к высокой или низкой температуре, боли и касаниям;
- нарушение ясности речи;
- проблемы с координацией.
Вегетативными признаками сенсомоторной полинейропатии асконального типа считаются следующие симптомы:
- учащенный или, напротив, замедленный сердечный ритм;
- неумеренное потоотделение;
- чрезмерная сухость кожи;
- изменение цвета кожных покровов;
- нарушение эякуляции;
- эректильная дисфункция;
- проблемы с мочеиспусканием;
- сбой двигательных функций желудочно-кишечного тракта;
- повышенное слюнотечение или, наоборот, сухость во рту;
- расстройство аккомодации глаза.
Заболевание проявляется в нарушениях функций поврежденных нервов. Именно периферические нервные волокна отвечают за двигательные функции мышечной ткани, чувствительность, а также оказывают вегетативное воздействие, то есть регулируют сосудистый тонус.
Для нарушения функции проводимости нервов характерны расстройства чувствительности, например:
- чувство ползания мурашек;
- гиперестезия, то есть увеличение чувствительности кожи к внешним раздражителям;
- гипестезия, то есть уменьшение чувствительности;
- отсутствие ощущения собственных конечностей.
Когда поражены вегетативные волокна, то из-под контроля выходит регуляция сосудистого тонуса. При аксонально-демиелинизирующей полинейропатии наступает сдавление капилляров, из-за чего ткани отекают. Нижние, а затем и верхние конечности из-за скапливания в них жидкости существенно увеличиваются в размерах. Так как при полинейропатии нижних конечностей основное количество крови накапливается именно в пораженных областях тела, то у пациента возникает стойкое головокружение при принятии вертикального положения. Из-за того, что пропадает трофическая функция, могут возникнуть эрозивно-язвенные поражения нижних конечностей.
Аксональная моторная полинейропатия проявляется в двигательных нарушениях верхних и нижних конечностей. Когда моторные волокна, отвечающие за движения рук и ног, повреждены, то наступает полный или частичный паралич мышц. Обездвиживание может проявляться совершенно нетипично — может ощущаться как скованность мышечных волокон, так и чрезмерная их расслабленность. При средней степени поражения ослаблен мышечный тонус.
В ходе течения заболевания могут быть усилены или ослаблены сухожильные и надкостничные рефлексы. В редких случаях доктор-невролог их не наблюдает. При болезни часто могут быть поражены черепные нервы, которые проявляются следующими нарушениями:
- глухотой;
- онемением подъязычных мышц и мускулатуры языка;
- невозможностью проглотить еду или жидкость из-за проблем с глотательным рефлексом.
Когда поражен тройничный, лицевой или глазодвигательный нерв, изменяется чувствительность кожных покровов, развиваются параличи, возникает асимметрия лица и подергивание мышц. Иногда при диагностированной аксонально-демиелинизирующей полинейропатии поражения верхних или нижних конечностей могут быть асимметричными. Такое случается при множественной мононейропатии, когда коленные, ахилловы и карпорадиальные рефлексы несимметричны.
Диагностика
Главной методикой исследования, которая позволяет обнаружить локализацию патологического процесса и степень пораженности нервов, является электронейромиография.
Чтобы определить причину заболевания, врачи назначают следующие анализы:
- определение уровня сахара в плазме крови;
- токсикологические тесты;
- полный анализ мочи и крови;
- выявление уровня холестерина в организме.
Нарушение нервных функций устанавливается при помощи определения температурной, вибрационной и тактильной чувствительности.
При первичном осмотре применяется зрительная методика исследования. То есть врач, к которому обратился с жалобами пострадавший, осматривает и анализирует такие внешние симптомы, как:
- уровень давления крови в верхних и нижних конечностях;
- чувствительность кожных покровов к прикосновениям и температуре;
- наличие всех необходимых рефлексов;
- диагностика отечности;
- изучение внешнего состояния кожи.
Выявить аксональную полинейропатию можно при помощи следующих инструментальных исследований:
- магнитная резонансная томография;
- биопсия нервных волокон;
- электронейромиография.
Лечение аксональной полинейропатии
Лечение аксональной полинейропатии должно быть комплексным и направленным на причину развития заболевания, его механизмы и симптоматику. Гарантией эффективной терапии является своевременное выявление болезни и лечение, которое сопровождается абсолютным отказом от сигарет, алкоголя и наркотических веществ, ведением здорового образа жизни и соблюдением всех рекомендаций врача. В первую очередь проводятся следующие терапевтические мероприятия:
- избавление от токсического воздействия на организм, если оно присутствует;
- антиоксидантная терапия;
- прием препаратов, которые воздействуют на тонус кровеносных сосудов;
- восполнение дефицита витаминов;
- регулярный контроль концентрации глюкозы в плазме крови.
Отдельное внимание уделяется лечению, направленному на купирование острого болевого синдрома.
Если присутствуют периферические парезы, то есть существенное снижение мышечной силы с многократным уменьшением амплитуды движений, то в обязательном порядке показана лечебная физкультура и специальные физические упражнения, направленные на возвращение тонуса мышечным тканям и предотвращение образования различных контрактур. Особенно важна регулярная психологическая поддержка, которая не дает пациенту впасть в депрессию, сопровождающуюся расстройством сна и чрезмерной нервной возбудимостью.
Лечение аксональной полинейропатии — это продолжительный процесс, так как нервные волокна восстанавливаются долго. Поэтому не стоит ожидать моментального выздоровления и возвращения к привычному образу жизни. Медикаментозная терапия включает такие препараты, как:
- обезболивающее;
- глюкокортикоиды;
- витамины группы В;
- антиоксиданты;
- сосудорасширяющие;
- средства, ускоряющие метаболизм и улучшающие микроциркуляцию крови.
Терапия лекарственными препаратами направлена на восстановление функций нервов, улучшение проводимости нервных волокон и скорости передачи сигналов центральной нервной системе.
Лечение следует проводить длительными курсами, которые не стоит прерывать, хоть и эффект от них проявляется не сразу. Чтобы устранить болевые ощущения и расстройство сна, назначают следующие медикаменты:
- антидепрессанты;
- противосудорожные;
- препараты, купирующие аритмию;
- обезболивающие.
Для избавления от боли используют нестероидные противовоспалительные препараты. Но стоит помнить, что применять их можно только короткий промежуток времени, так как длительное употребление может привести к повреждению слизистой оболочки желудочно-кишечного тракта.
К физиотерапевтическим методам лечения аксональной полинейропатии относятся:
- терапия магнитными волнами;
- грязелечение;
- электростимуляция;
- иглоукалывание;
- лечебный массаж;
- физкультура;
- ультрафонофорез;
- гальванотерапия.
Именно лечебная физкультура позволяет сохранить работоспособность мышечных тканей и поддерживать конечности в нужном положении. Регулярные занятия спортом вернут мышцам тонус, гибкость и увеличат амплитуду движений до нормальной.
Прогноз
Если заболевание обнаружено на ранней стадии и комплексно лечится квалифицированными специалистами, то прогноз для жизни и здоровья пациента более чем благоприятный. Стоит вести правильный образ жизни, рацион должен быть богат витаминами и минералами, необходимыми для правильного функционирования организма.
Если долгое время игнорировать болезнь и не предпринимать никаких действий, результат будет плачевным вплоть до полного паралича.
Профилактика
Пациент в обязательном порядке должен совершать профилактические мероприятия, которые помогут избежать рецидива или возникновения опасного заболевания. Они включают в себя обогащение рациона витаминами, регулярный контроль уровня сахара в крови, полный отказ от табакокурения, наркотических веществ и алкогольных напитков.
В целях профилактики болезни рекомендуется:
- носить удобную обувь, которая не пережимает стопу, ухудшая кровоток;
- регулярно осматривать обувь, чтобы избежать образования грибка;
- исключить пешие прогулки на длительные расстояния;
- не стоять долгое время на одном месте;
- мыть ноги прохладной водой или делать контрастные ванночки, что помогает улучшить циркуляцию крови в организме.
Пострадавшим в стадии ремиссии категорически запрещается принимать лекарственные препараты без согласования с лечащим врачом. Важно своевременно лечить воспалительные заболевания, соблюдать меры предосторожности при работе с токсическими веществами, которые оказывают пагубное воздействие на организм, регулярно выполнять лечебные физические упражнения.
https://ru.wikipedia.org/wiki/%D0%90%D0%BA%D1%81%D0%BE%D0%BD
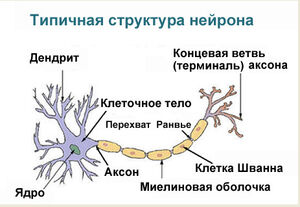
Нейрон состоит из одного аксона, тела и нескольких дендритов,
Аксон (греч. ἀξον — ось) — нервное волокно, длинная, вытянутая часть нервной клетки (нейрона), отросток или нейрит, элемент, который проводит электрические импульсы далеко от тела нейрона (сомы).
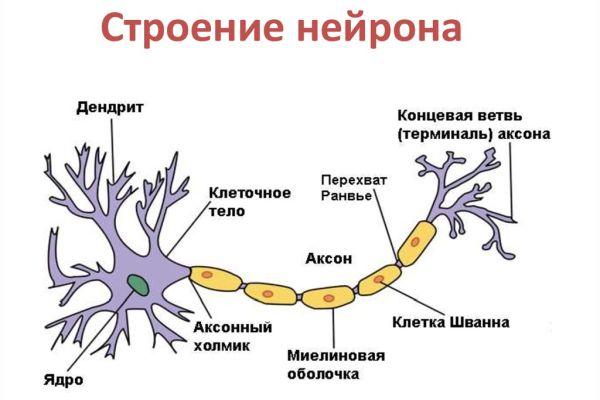
Строение нейрона
Нейрон состоит из одного аксона, тела и нескольких дендритов, в зависимости от числа которых нервные клетки делятся на униполярные, биполярные, мультиполярные. Передача нервного импульса происходит от дендритов (или от тела клетки) к аксону. Если аксон в нервной ткани соединяется с телом следующей нервной клетки, такой контакт называется аксо-соматическим, с дендритами — аксо-дендритический, с другим аксоном — аксо-аксональный (редкий тип соединения, встречается в ЦНС, участвует в обеспечении тормозных рефлексов).
В месте соединения аксона с телом нейрона находится аксонный холмик — именно здесь происходит преобразование постсинаптического потенциала нейрона в нервные импульсы, для чего требуется совместная работа натриевых, кальциевых и как минимум трех типов калиевых каналов.
Питание и рост аксона зависят от тела нейрона: при перерезке аксона его периферическая часть отмирает, а центральная сохраняет жизнеспособность. При диаметре в несколько микрон длина аксона может достигать у крупных животных 1 метра и более (например, аксоны, идущие от нейронов спинного мозга в конечности). У многих животных (кальмаров, рыб, кольчатых червей, форонид, ракообразных) встречаются гигантские аксоны толщиной в сотни мкм (у кальмаров — до 2-3 мм). Обычно такие аксоны отвечают за проведение сигналов к мышцам. обеспечивающим «реакцию бегства» (втягивание в норку, быстрое плавание и др.). При прочих равных условиях с увеличением диаметра аксона увеличивается скорость проведения по нему нервных импульсов.
В протоплазме аксона — аксоплазме — имеются тончайшие волоконца — нейрофибриллы, а также микротрубочки, митохондрии и агранулярная(гладкая)эндоплазматическая сеть. В зависимости от того, покрыты ли аксоны миелиновой (мякотной) оболочкой или лишены её, они образуют мякотные или безмякотные нервные волокна.
Миелиновая оболочка аксонов имеется только у позвоночных. Её образуют «накручивающиеся» на аксон специальные шванновские клетки, между которыми остаются свободные от миелиновой оболочки участки — перехваты Ранвье. Только на перехватах присутствуют потенциал-зависимые натриевые каналы и заново возникает потенциал действия. При этом нервный импульс распространяется по миелинизированным волокнам ступенчато, что в несколько раз повышает скорость его распространения.
Концевые участки аксона — терминали — ветвятся и контактируют с другими нервными, мышечными или железистыми клетками. На конце аксона находится синаптическое окончание — концевой участок, контактирующий с клеткой-мишенью. Вместе с постсинаптической мембраной клетки-мишени синаптическое окончание образует синапс. Через синапсы передаётся возбуждение.[1]
Анатомия
Аксоны — в действительности первичные линии передачи сигналов нервной системы, и как связки они помогают составлять нервные волокна. Индивидуальные аксоны являются микроскопическими в диаметре (типично 1 мкм в сечении), но могут достигать нескольких метров. Самые длинные аксоны в человеческом теле, например, аксоны седалищного нерва, которые простираются от позвоночника к большому пальцу ноги. Эти волокна единственной ячейки седалищного нерва могут увеличиться до метра или еще длинее.[2]
У позвоночных животных, аксоны многих нейронов вложены в ножны в миелине, который сформирован любым из двух типов глиальных ячеек: Ячейки Schwann ensheathing периферийные нейроны и oligodendrocytes изолирование таковых из центральной нервной системы. По myelinated волокнам нерва, промежутки в ножнах, известных, поскольку узлы Ranvier происходят в равномерно-раздельных интервалах. Myelination имеют очень быстрый способ электрического распространения импульса, названного скачкообразным. Demyelination аксоны, который вызывает множество неврологических признаков, типичных для заболевания под названием «рассеянный склероз». Аксоны некоторой ветви нейронов, формирующие имущественные залоги аксона, могут быть разделены на множество меньших ветвей, названных telodendria. По ним bifurcated импульс распространяются одновременно, для сигнализиции больше, чем одной ячейки другую ячейку.
Физиология
Физиология может быть описана Моделью Hodgkin-Huxley, распространённой на позвоночных животных в уравнениях Frankenhaeuser-Huxley. Периферийные волокна нерва могут быть классифицированы на основанные, на аксонально-скоростные проводимости, mylenation, размеры волокна и т.д. Например, есть медленное проведение unmyelinated С fibers волокна и более быстрое проведение myelinated Aδ fibers волокна. Более сложное математическое моделирование проводится сегодня. Есть несколько типов сенсорных — таких как motorfibers. Другие волокна, не упомянутые в матеоиале — например, волокна автономной нервной системы
Двигательная функция
В таблице паказаны моторные нейроны, которые имеют два вида волокон:
| Тип | Классификация | Диаметр | Миелин | Скорость проводимости | Связанные мускульные волокна |
|---|---|---|---|---|---|
| α | Aα | 13-20 мкм | Yes | 80-120 m/s | Extrafusal muscle fibers |
| γ | Aγ | 5-8 мкм | Yes | 4-24 m/s[3][4] | Intrafusal muscle fibers |
Сенсорная функция
Различные сенсорные рецепторы возбуждаются различными типами волокон нерва. Proprioceptors возбуждены типом Ia, Ib и II сенсорными волокнами, механорецепторы — типом II и III сенсорными волокнами и типом nociceptors и thermoreceptors.
| Типы | Классификация | Диаметр | Миелин | Скорость проводимости | Связанные сенсорные рецепторы |
|---|---|---|---|---|---|
| Ia | Aα | 13-20 мкм | Yes | 80-120 m/s | Primary receptors of muscle spindle |
| Ib | Aα | 13-20 мкм | Yes | 80-120 m/s | Golgi tendon organ |
| II | Aβ | 6-12 мкм | Yes | 33-75 m/s | Secondary receptors of muscle spindle All cutaneous mechanoreceptors |
| III | Aδ | 1-5 мкм | Thin | 3-30 m/s | Free nerve endings of touch and pressure Nociceptors of neospinothalamic tract Cold thermoreceptors |
| IV | C | 0.2-1.5 мкм | No | 0.5-2.0 m/s | Nociceptors of paleospinothalamic tract Warmth receptors |
Автономная функция
Автономная нервная система имеет два вида периферийных волокон:
| Typы | Классификация | Диаметр | Миелин[5] | Скорость проводимости |
|---|---|---|---|---|
| preganglionic fibers | B | 1-5 мкм | Yes | 3-15 m/s |
| postganglionic fibers | C | 0.2-1.5 мкм | No | 0.5-2.0 m/s |
Рост и развитие аксона
Нейрон
Рост аксонов происходит через их окружающую среду, в виде конуса роста, который находится в наконечнике аксона. Конус роста имеет широкий лист как расширение, названное lamellipodia, которое содержат выпячивания, названные filopodia. Filopodia — механизм, представляющий процесс придержки поверхностей. Он анализирует ближайшую окружающую среду. Актин играет главную роль в подвижности этой системы. Окружающие среды с высокими уровнями молекул прилипания ячейки или «КУЛАКА» создают идеальную окружающую среду для аксонального роста. Это, кажется, обеспечивает «липкую» поверхность для аксонов, для раста вперед. Примеры КУЛАКА, определенного для нервных систем включают: N-КУЛАК, neuroglial КУЛАК или NgCAM, ПОМЕТЬТЕ 1, МЭГ, и DCC, все из которых — часть суперсемьи иммуноглобулина. Другой набор молекул звонковый, внеклеточные матричные молекулы прилипания также обеспечивают липкое основание для аксонов, чтобы расти вперед. Примеры этих молекул включают laminin, fibronectin, tenascin, и perlecan. Некоторые из них — поверхность, привязанная к ячейкам и таким образом действуют, как короткие аттрактанты диапазона или repellents. Другие — difusible лиганды и таким образом могут долго сохранять эффекты диапазона.
Ячейки звонковые, ячейки указательного столба помогают в руководстве ростом аксона нейронала. Эти ячейки — типично другой, иногда незрелый, нейроны.
История
Часть первой внутриклеточной регистрации в нервной системе была сделана в конце 1930-ых учёными K. Капуста и H. Куртис. Алан Ходгкин и Эндрю Хакслей также использовали аксон гиганта кальмара (1939), и в 1952 они получили полное количественное описание действия ионного основания потенциала, введя формулировку Модели Hodgkin-Huxley. Ходгкину и Хакслей, были предтавлены совместно на паолучение Нобелевской премии по этой работе в 1963. Формулы, детализирующие аксональную проводимость были расширены на позвоночных животных в уравнениях Frankenhaeuser-Huxley. Erlanger и Gasser ранее развивали систему классификации для периферийного[5] волокна нерва, основанные на аксональной скорости проводимости, myelination, размере волокна и т.д. Даже и сейчас наше понимание биохимического процесса распространения действия потенциала продвинулось, и теперь он включает много деталей об индивидуальных каналах иона.
Рана
Основная статья: Рана
На серьёзном уровне, рана нерва может быть описана как neuropraxia, axonotmesis, или neurotmesis. Сотрясение мозга считают умеренной формой разбросанной аксональной раны [6].
См. также
- Сенсорные нервы
- Сенсорный рецептор
- Нейрон
- Аксональный поиск пути
- Аксональный транспорт
- Аксон-рефлекс
- Конус роста
- Дендрит
- Валлерова дегенерация — при разрыве аксона
Примечания
- ↑ http://en.wikipedia.org/wiki/Axon
- ↑ DNA From The Beginning, section 6: Genes are real things., «Amination» section, final slide
- ↑ Andrew BL, Part NJ (1972) Properties of fast and slow motor units in hind limb and tail muscles of the rat. Q J Exp Physiol Cogn Med Sci 57:213-225.
- ↑ Russell NJ (1980) Axonal conduction velocity changes following muscle tenotomy or deafferentation during development in the rat. J Physiol 298:347-360.
- ↑ pp.187-9 ISBN 0-19-858527-6
- ↑ eMedicine — Traumatic Brain Injury: Definition, Epidemiology, Pathophysiology : Article by Segun T Dawodu, MD, FAAPMR, FAANEM, CIME, DipMI(RCSed)
Гистология: Нервная ткань |
|
|---|---|
| Нейроны (Серое вещество) |
Сома · Аксон (Аксонный холмик, Терминаль аксона, Аксоплазма, Аксолемма, Нейрофиламенты) Дендрит (Вещество Ниссля, Дендритный шипик, Апикальный дендрит, Базальный дендрит) типы: Биполярные нейроны · Псевдополярные нейроны · Мультиполярные нейроны · Пирамидальный нейрон · Клетка Пуркинье · Гранулярная клетка |
| Афферентный нерв/ Сенсорный нерв/ Сенсорный нейрон |
GSA · GVA · SSA · SVA · Нервные волокна (Мышечные веретёна (Ia), Нервно-сухожильное веретено, II or Aβ, Aδ-волокна, C-волокна) |
| Эфферентный нерв/ Моторный нерв/ Моторный нейрон |
GSE · GVE · SVE · Верхний моторный нейрон · Нижний моторный нейрон (α мотонейроны, γ мотонейроны) |
| Синапс |
Нейропиль · Синаптический пузырек · Нервно-мышечный синапс · Электрический синапс · Интернейрон (Клетки Реншоу) |
| Сенсорный рецептор |
Чувствительное тельце Мейснера · Нервное окончание Меркеля · Тельца Пачини · Окончание Руффини · Нервномышечное веретено · Свободное нервное окончание · Обонятельный нейрон · Фоторецепторные клетки · Волосковые клетки · Вкусовая луковица |
| Нейроглия |
Астроциты (Радиальная глия) · Олигодендроглиоциты · Клетки эпендимы (Танициты) · Микроглия |
| Миелин (Белое вещество) |
CNS: Олигодендроцит PNS: Клетки Шванна · Невролемма · Перехват Ранвье/Межузловой сегмент · Насечка миелина |
| Соединительная ткань |
Эпиневрий · Периневрий · Эндоневрий · Нервные пучки · Оболочки мозга |
Нервная система состоит из нейронов (специфических клеток, имеющих отростки) и нейроглии (она заполняет пространство между нервными клетками в ЦНС). Главное отличие между ними заключается в направлении передачи нервного импульса. Дендриты – это принимающие ответвления, по ним сигнал идет к телу нейрона. Передающие клетки – аксоны – проводят сигнал от сомы к принимающим. Это могут быть не только отростки нейрона, но и мышцы.
Отличия аксонов и дендритов
Какова же разница между ними? Рассмотрим.
- Дендрит нейрона короче передающего отростка.
- Аксон всего один, принимающих ответвлений может быть много.
- Дендриты сильно ветвятся, а передающие отростки начинают разделяться ближе к концу, образуя синапс.
- Дендриты истончаются по мере удаления от тела нейрона, толщина аксонов практически неизменна по всей длине.
- Аксоны покрыты миелиновой оболочкой, состоящей из липидных и белковых клеток. Она выполняет роль изолятора и защищает отросток.
Поскольку нервный сигнал передается в виде электрического импульса, клеткам необходима изоляция. Её функции выполняет миелиновая оболочка. Она имеет мельчайшие разрывы, способствующие более быстрой передаче сигнала. Дендриты – это безоболочечные отростки.
Определение
Мозговое вещество – высокоорганизованная структура, образованная нервными клетками, от которых отходят аксоны. Из нервных клеток состоит мозговая ткань. Аксон в переводе с греческого означает «ось» – это такой отросток, элемент мозгового вещества, который обеспечивает взаимодействие между клетками разного типа (нейроны, клетки иннервируемых органов), что ассоциируется с тонким, четким управлением работой органов и систем. Функции ткани ЦНС:
- Воспринимает раздражения, преобразуя их в импульсы.
- Поддерживает передачу импульсов от управляющих отделов мозга к исполнительным органам.
- Формирует ответную реакцию на раздражающее воздействие.
- Обеспечивает взаимодействие в работе систем и органов, поддерживает интеграцию структурных единиц организма.
- Обеспечивает взаимосвязь организма с внешней средой.
Согласно определению в биологии, аксон (англ. axon) – удлиненный отросток, по которому идут импульсы от тела нейрона к другим нервным клеткам и структурным элементам всех тканей организма. Мозговая ткань в период внутриутробного развития образуется из нервной пластины. Края пластинки прогибаются, что приводит к формированию валиков и желобка. В результате смыкания краев валиков возникает нервная трубка – основа ЦНС.
Дифференциация клеток, образующих трубку, приводит к появлению нейробластов и спонгиобластов. Первые служат основой для формирования нейронов, вторые – для образования нейроглии. Нейроны (анат.) – основные структурные элементы мозгового вещества. Они характеризуются отсутствием функции деления, что приводит к постепенному уменьшению их численности. Тело нейрона состоит из ядра и цитоплазмы. В зависимости от типа нейронов меняется геометрическая форма тела, которая бывает круглая, овальная, пирамидальная и другая.
Цитоскелет, состоящий из микротрубочек и нейрофибриллов, обеспечивает опорную и трофическую функцию. Цитоскелет поддерживает форму нейрона, обеспечивает транспорт веществ и органелл. От тела ответвляются отростки – единичный аксон и множественные дендриты. Аксон нейрона почти не ветвится, иногда образует коллатеральные (обходные) сегменты. Концевые сегменты (окончания) разветвляются, называются терминали.
Терминали взаимосвязаны с окончаниями других нейронов и с клетками, образующими паренхиму (ткань) рабочих органов – мышц, желез. Количество дендритов варьируется от 1 до нескольких. Тонкие ответвления дендритов оканчиваются небольшими шипами, где сосредоточены терминали аксональных отростков многих тысяч других клеток. Дендриты воспринимают раздражения или потенциалы действия от других клеток и передают их по волокнам к телу своего нейрона.
Рост аксона зависит от особенностей строения и жизнедеятельности нейрона, который поддерживает функцию питания отростка. К примеру, если перерезать аксональный ствол, сегмент, связанный с телом, остается жизнеспособным и продолжает деятельность, участок, утративший связь с телом, отмирает. Аксоны образуют нервы, что предполагает сложную структурно-морфологическую организацию ЦНС.
Синапс
Место, в котором происходит контакт между ответвлениями нейронов или между аксоном и принимающей клеткой (например, мышечной), называется синапсом. В нем может участвовать всего по одному ответвлению от каждой клетки, но чаще всего контакт происходит между несколькими отростками. Каждый вырост аксона может контактировать с отдельным дендритом.
Сигнал в синапсе может передаваться двумя способами:
- Электрическим. Это происходит только в случае, когда ширина синаптической щели не превышает 2 нм. Благодаря такому маленькому разрыву импульс проходит через него, не задерживаясь.
- Химическим. Аксоны и дендриты вступают в контакт благодаря разнице потенциалов в мембране передающего отростка. С одной ее стороны частицы имеют положительный заряд, с другой – отрицательный. Это обусловлено разной концентрацией ионов калия и натрия. Первые находятся внутри мембраны, вторые – снаружи.
При прохождении заряда увеличивается проницаемость мембраны, и натрий входит в аксон, а калий выходит из него, восстанавливая потенциал.
Сразу после контакта отросток становится невосприимчивым к сигналам, через 1 мс способен к передаче сильных импульсов, через 10 мс возвращается в исходное состояние.
Дендриты – это принимающая сторона, передающая импульс от аксона телу нервной клетки.
Особенности, характерные для типичных дендритов и аксонов
⇐ ПредыдущаяСтр 3 из 14Следующая ⇒
| Дендриты | Аксоны |
| От тела нейрона отходит несколько дендритов | У нейрона имеется только один аксон |
| Длина редко превышает 700 мкм | Длина может достигать 1 м |
| По мере удаления от тела клетки диаметр быстро уменьшается | Диаметр сохраняется на значительном расстоянии |
| Образовавшиеся в результате деления ветви локализуются возле тела | Терминали располагаются далеко от тела клетки |
| Имеются шипики | Шипики отсутствуют |
| Не содержат синаптических пузырьков | Содержат в большом числе синаптические пузырьки |
| Содержат рибосомы | Рибосомы могут обнаруживаться в незначительном числе |
| Лишены миелиновой оболочки | Часто окружены миелиновой оболочкой |
Терминали дендритов чувствительных нейронов образуют чувствительные окончания. Основной функцией дендритов является получение информации от других нейронов. Дендриты проводят информацию к телу клетки, а затем к аксонному холмику.
Аксон. Аксоны образуют нервные волокна, по которым передается информация от нейрона к нейрону или к эффекторному органу. Совокупность аксонов образует нервы.
Общепринято подразделение аксонов на три категории: А, В и С. Волокна группы А и В являются миелинизированными, а С – лишены миелиновой оболочки. Диаметр волокон группы А, которые составляют большинство коммуникаций центральной нервной системы, варьирует от 1 до 16 мкм, а скорость проведения импульсов равна их диаметру, умноженному на 6. Волокна типа А подразделяются на Аa, Аb, Аl, Аs. Волокна Аb, Аl, Аs имеют меньший диаметр, чем волокна Аa, меньшую скорость проведения и более длительный потенциал действия. Волокна Аb и Аs являются преимущественно чувствительными волокнами, которые проводят возбуждение от различных рецепторов в ЦНС. Волокна Аl – это волокна, которые проводят возбуждение от клеток спинного мозга к интрафузальным мышечным волокнам. В-волокна являются характерными для преганглионарных аксонов вегетативной нервной системы. Скорость проведения 3-18 м/с, диаметр 1-3 мкм, продолжительность потенциала действия 1-2 мс, нет фазы следовой деполяризации, а есть длительная фаза гиперполяризации (более 100 мс). Диаметр С-волокон от 0,3 до 1,3 мкм, и скорость проведения импульсов в них несколько меньше величины диаметра, умноженного на 2, и равняется 0,5-3 м/с. Длительность потенциала действия этих волокон составляет 2 мс, отрицательный следовой потенциал равняется 50-80 мс, а положительный следовой потенциал – 300-1000 мс. Большинство С-волокон являются постганглионарными волокнами вегетативной нервной системы. В миелинизированных аксонах скорость проведения импульсов выше, чем в немиелизированных.
Аксон содержит аксоплазму. У крупных нервных клеток ей принадлежит около 99% всей цитоплазмы нейрона. Цитоплазма аксонов содержит микротрубочки, нейрофиламенты, митохондрии, агранулярный эндоплазматический ретикулум, везикулы и мультивезикулярные тела. В разных частях аксона существенно меняются количественные отношения между этими элементами.
У аксонов, как миелинизированных, так и немиелизированных, есть оболочка – аксолемма.
В зоне синаптического контакта мембрана получает ряд дополнительных цитоплазматических соединений: плотные выступы, ленты, субсинаптическая сеть и др.
Начальный участок аксона (от его начала до того места, где наступает сужение до диаметра аксона) носит название аксонного холмика. От этого места и появления миелиновой оболочки простирается начальный сегмент аксона. В немиелинизированных волокнах эта часть волокна определяется с трудом, а некоторые авторы считают, что начальный сегмент присущ только тем аксонам, которые покрыты миелиновой оболочкой. Он отсутствует, например, у клеток Пуркинье в мозжечке.
В месте перехода аксонного холмика в начальный сегмент аксона под аксолеммой появляется характерный электронноплотный слой, состоящий из гранул и фибрилл, толщиной 15 нм. Этот слой не связан с плазматической мембраной, а отделен от нее промежутками до 8 нм.
В начальном сегменте по сравнению с телом клетки резко уменьшается количество рибосом. Остальные компоненты цитоплазмы начального сегмента – нейрофиламенты, митохондрии, везикулы – переходят из аксонного холмика сюда, не изменяясь ни по внешнему виду, ни по взаиморасположению. На начальном сегменте аксона описаны аксо-аксональные синапсы.
Часть аксона, покрытая миелиновой оболочкой, обладает только ей присущими функциональными свойствами, которые связаны с проведением нервных импульсов с большой скоростью и без декремента (затухания) на значительные расстояния. Миелин является продуктом жизнедеятельности нейроглии. Проксимальной границей у миелинизированного аксона служит начало миелиновой оболочки, а дистальной – утрата ее. Далее следуют более или менее длинные терминальные отделы аксона. В этой части аксона отсутствует гранулярный эндоплазматический ретикулум и очень редко встречаются рибосомы. Как в центральных отделах нервной системы, так и на периферии аксоны окружены отростками глиальных клеток.
Миелинизированная оболочка имеет сложное строение. Ее толщина варьирует от долей до 10 мкм и более. Каждая из концентрически расположенных пластинок состоит из двух наружных плотных слоев, образующих главную плотную линию, и двух светлых бимолекулярных слоев липидов, разделенных промежуточной осмиофильной линией. Промежуточная линия аксонов периферической нервной системы представляет собой соединение наружных поверхностей плазматических мембран шванновской клетки. Каждый аксон сопровождается большим числом шванновских клеток. Место, где шванновские клетки граничат между собой, лишено миелина и называется перехватом Ранвье. Между длиной межперехватного участка и скоростью проведения нервных импульсов есть прямая зависимость.
Перехваты Ранвье составляют сложную структуру миелинизированных волокон и играют важную функциональную роль в проведении нервного возбуждения.
Протяженность перехвата Ранвье миелинизированных аксонов периферических нервов находится в пределах 0,4-0,8 мкм, в центральной нервной системе перехват Ранвье достигает 14 мкм. Длина перехватов довольно легко изменяется под действием различных веществ. В области перехватов, помимо отсутствия миелиновой оболочки, наблюдаются значительные изменения структуры нервного волокна. Диаметр крупных аксонов, например, уменьшается наполовину, мелкие аксоны изменяются меньше. Аксолемма имеет обычно неправильные контуры, и под ней лежит слой электронноплотного вещества. В перехвате Ранвье могут быть синаптические контакты как с прилежащими к аксону дендритами (аксо-дендритические), так и с другими аксонами.
Коллатерали аксонов. С помощью коллатералей происходит распространение нервных импульсов на большее или меньшее число последующих нейронов.
Аксоны могут делиться дихотомически, как, например, у зернистых клеток мозжечка. Очень часто встречается магистральный тип ветвления аксонов (пирамидные клетки коры мозга, корзинчатые клетки мозжечка). Коллатерали пирамидных нейронов могут быть возвратными, косоидущими и горизонтальными. Горизонтальные ответвления пирамид простираются иногда на 1-2 мм, объединяя пирамидные и звездчатые нейроны своего слоя. От горизонтально распространяющегося (в поперечном направлении к длинной оси извилины мозга) аксона корзинчатой клетки образуются многочисленные коллатерали, которые заканчиваются сплетениями на телах крупных пирамидных клеток. Подобные аппараты, так же как и окончания на клетках Реншоу в спинном мозге, являются субстратом для осуществления процессов торможения.
Коллатерали аксонов могут служить источником образования замкнутых нейронных цепей. Так, в коре больших полушарий все пирамидные нейроны имеют коллатерали, которые принимают участие во внутрикорковых связях. За счет существования коллатералей обеспечивается в процессе ретроградной дегенерации сохранность нейрона в том случае, если повреждается основная ветвь его аксона.
Терминали аксонов. К терминалям относятся дистальные участки аксонов. Они лишены миелиновой оболочки. Протяженность терминалей значительно варьирует. На светооптическом уровне показано, что терминали могут быть либо одиночными и иметь форму булавы, сетевидной пластинки, колечка, либо множественными и походить на кисть, чашевидную, моховидную структуру. Размер всех этих образований изменяется от 0,5 до 5 мкм и более.
Тонкие разветвления аксонов в местах контакта с другими нервными элементами нередко имеют веретеновидные или бусинковидные расширения. Как показали электронно-микроскопические исследования, именно в этих участках имеются синаптические соединения. Одна и та же терминаль дает возможность одному аксону устанавливать контакт с множеством нейронов (например, параллельные волокна в коре головного мозга) (рис. 1.2).
Функции нервных волокон
Распространение возбуждения в нервных волокнах.Изменения мембранного потенциала, вызываемые электрическим током, подразделяются на пассивные и активные.
Пассивные, или электротонические, изменения мембранного потенциала определяются физическими (электрическими) параметрами как самой мембраны, так и всей клетки (волокна) в целом.
Пассивные сдвиги мембранного потенциала возникают при действии на возбудимые образования электрического тока любой силы, формы или направления. Однако если при гиперполяризующем (анодном) и слабом деполяризующем (катодном) токах пассивные изменения потенциала могут наблюдаться в чистом (неосложненном) виде, то при близких к порогу и сверхпороговых деполяризующих стимулах они сопровождаются активными сдвигами потенциала: локальным ответом и потенциалом действия, связанными с изменениями ионной проницаемости мембраны.
Пассивные свойства мембраны и всего волокна в целом в значительной мере определяют условия возникновения и распространения возбуждения в нервном волокне.
Исследования показывают, что в однородно поляризуемом, однородном участке нервного волокна изменения мембранного потенциала при приложении прямоугольного толчка гиперполяризующего или слабого деполяризующего тока нарастают по экспоненте:
,
где RC = τ
– постоянная времени мембраны, т.е. время, в течение которого потенциал нарастает до 63% от своей конечной величины. При выключении тока потенциал возвращается к исходному уровню по экспоненте с той же постоянной времени
τ
. Такие изменения мембранного потенциала принято называть пассивными или электротоническими, в отличие от активных, связанных с повышением или снижением ионных проводимостей мембраны.
Подобные изменения наблюдаются на сферических клетках (на соме). Описание цилиндрической клетки, в частности аксона, более сложно. В этом случае уже нельзя считать внутренний проводник эквипотенциальным по всей длине. Внешний проводник можно считать эквипотенциальным за счет увеличения объема внеклеточной жидкости. Потенциал на такой мембране зависит не только от времени включения тока, но и от расстояния х
по отношению к месту приложения тока:
,
где а
– радиус волокна,
R
– удельное сопротивление аксоплазмы,
CМ
и
RМ
– емкость и сопротивление на единицу площади мембраны. Левая часть уравнения описывает плотность тока через каждую точку мембраны, которая равна сумме плотностей емкостного ()и омического () токов, стоящих в правой части уравнения.
Через длительное время (намного большего постоянной времени t = RМ CМ
) после включения импульса емкость мембраны полностью зарядится и емкостный ток станет равным нулю. Уравнение примет вид:
.
Его решение:
,
где V0
– потенциал в начале кабеля (
х
= 0),
l
– постоянная длины волокна.
Постоянная длины характеризует крутизну затухания потенциала вдоль волокна. Чем больше l
, тем дальше по волокну проходит сигнал. Скорость электротонического распространения пропорциональна удвоенной величине константы длины волокна
l
и обратно пропорциональна постоянной времени
t = RМ CМ
. Величина
l
может быть выражена через сопротивление мембраны
RМ
, сопротивление внутренней среды – аксоплазмы
Ri
и диаметра волокна
d
:
.
Кабельные свойства нервных волокон оказывают существенное влияние не только на развитие электротонических потенциалов, но и на характер активных ответов – величину порога, амплитуду, крутизну нарастания и длительность потенциала действия.
В настоящее время можно считать строго доказанным, что проведение потенциала действия (ПД) вдоль нервного волокна осуществляется с помощью локальных токов, возникающих между возбужденным и покоящимся участками мембраны. Локальный ток изменяет величину мембранного потенциала покоя в покоящемся участке до критического уровня деполяризации, что и является причиной возникновения потенциала действия.
Многочисленными исследованиями было показано, что скорость проведения пропорциональна постоянной длины волокна l
и обратно пропорциональна постоянной времени мембраны
t
(Чайлохян Л.М., 1962). Поскольку в безмякотных нервных волокнах
l
пропорциональна квадратному корню из диаметра волокна
,
скорость проведения при прочих равных условиях также пропорциональна корню квадратному из диаметра волокна.
В миелинизированных нервных волокнах проведение происходит сальтаторно – от перехвата Ранвье к перехвату Ранвье. Длина межперехватного участка примерно пропорциональна диаметру волокна, поэтому скорость проведения в этих волокнах пропорциональна не корню квадратному из диаметра волокна, а просто его диаметру.
Принято считать, что скорость проведения зависит от величины так называемого фактора безопасности (гарантийности) Ф
, т.е. отношения амплитуды распространяющегося ПД к пороговому потенциалу. Пороговый потенциал – это та величина, на которую нужно изменить мембранный потенциал, чтобы достичь критического уровня деполяризации.
,
где Vs
– амплитуда ПД,
Vt
– пороговый потенциал.
При Ф = Vt
распространения возбуждения нет. Для аксона краба это отношение равно 7.
Было показано, что пороговый потенциал Vt
находится в тесной зависимости от чувствительности системы натриевой проницаемости мембраны к деполяризации. Чем выше эта чувствительность, т.е. чем на большую величину повышается
PNa
и, соответственно, натриевый входящий ток
INa
при данном сдвиге потенциала, тем ниже порог, и наоборот. Изменение состояния системы калиевой проницаемости на величину порогового потенциала практически не оказывает влияния. Точно так же очень мало влияет на пороговый потенциал проводимость токов «утечки». При постоянном потенциале покоя фактор безопасности должен возрастать при воздействиях на нервное волокно, которые повышают чувствительность натриевой системы к деполяризации, например, снижение концентрации ионов кальция в окружающей среде. Значительное снижение фактора безопасности вызывают агенты, усиливающие исходную инактивацию натриевой системы или уменьшающие натриевую проводимость, поскольку в этом случае амплитуда потенциала действия падает, а пороговый потенциал растет. Такие изменения проведения возбуждения наблюдал Тасаки (1957) и другие исследователи при воздействии на нервное волокно анестетиков и наркотиков в малых концентрациях, недостаточных для полного подавления потенциала действия.
Сложное влияние на фактор безопасности оказывает уровень потенциала покоя. Кратковременная подпороговая деполяризация мембраны, не изменяющая существенным образом критического потенциала и амплитуды потенциала действия, повышает фактор безопасности, так как Vt = Eo – Ek
. При сильной же деполяризации амплитуда спайка падает, критический потенциал растет, поэтому фактор безопасности уменьшается.
Наряду с фактором безопасности существенное влияние на скорость проведения возбуждения оказывает крутизна восходящей фазы распространяющегося потенциала действия. Крутизна этой фазы зависит как от пассивных, так и активных свойств мембраны.
Примерно 1/3 восходящей фазы распространяющегося ПД связана с пассивной деполяризацией мембраны нервного волокна током локальной цепи. Скорость же этой деполяризации при данной силе локального тока определяется постоянной времени мембраны t = RM CM
. Чем эта величина меньше, тем быстрее нарастает деполяризация и, следовательно, круче поднимается спайк. Инактивация натриевой системы, или снижение проницаемости для натрия (активные свойства мембраны), резко уменьшает крутизну восходящей фазы. Таким образом, при большинстве воздействий изменения скорости нарастания восходящей фазы ПД по своему направлению совпадают с изменениями фактора безопасности.
Согласно теории локальных токов, амплитуда распространяющегося потенциала действия Vs
, в отличие от мембранного спайка, зависит не только от ЭДС возбужденной мембраны
Е
, но и от соотношения входных сопротивлений возбужденного
R1
и невозбужденного (сопротивление нагрузки
R2
) участков волокна:
. (1)
Чем отношение выше, тем в большей мере амплитуда распространяющегося ПД приближается к величине Е
, тем, следовательно, выше фактор безопасности, и наоборот. Из чего вытекает, что снижение сопротивления мембраны (повышение ее ионной проводимости) при критической деполяризации не только ведет к возникновению спайка, но и способствует увеличению фактора безопасности, а значит, и скорости проведения.
Из формулы (1) ясно, что при проведении возбуждения по геометрически неоднородным возбудимым проводникам амплитуда распространяющегося спайка должна существенно зависеть от того, насколько близко находится возбужденный в данный момент участок волокна к месту его ветвления или расширения.
При расширении нервного волокна, например, в месте перехода его в тело клетки или в области ветвления аксона, суммарная площадь сечения волокон и общая площадь их мембраны увеличивается, а следовательно, R2
падает. Уменьшение
R2
снижает фактор безопасности и, соответственно, скорость проведения. При некоторых условиях уменьшение
R2
может привести к полному блокированию нервного импульса.
Расчеты показали, что потенциал действия легко проходит трехкратное расширение, с трудом пятикратное и полностью блокируется при шестикратном. Причиной развития блока является резкое снижение амплитуды распространяющегося ПД вблизи области расширения волокна.
Трофическая функция нервных волокон.Трофической функцией обладают афферентные и эфферентные волокна.
Афферентные нервы обладают двумя нейротрофическими, неимпульсными функциями. Можно различить прямое морфогенетическое и трофическое влияние на периферические органы и регуляторную функцию с обратной связью, зависящую, вероятно, от внутриаксональных центростремительных импульсов. Нейротрофическое морфогенетическое влияние доказано наличием: а) зависимости структуры вкусовых почек от вкусовых нервов; б) стимулирования регенерации конечности у амфибий чувствительными нервами посредством специфического, стимулирующего рост вещества немедиаторной природы; в) дифференцировки и поддержания рецепторов. После деафферентации в некоторых органах развиваются трофические нарушения. Первичный «трофический» нейрон для мышцы – это нейрон моторный. Нельзя забывать также, что во всех нервах проходят эфферентные адренергические волокна, вкоторых нейросекреты (катехоламины) транспортируются аксоплазматическим током к периферическим органам.
Аксональный транспорт.Описаны две системы аксонального транспорта – медленный, со скоростью 1-3 мм/день, и быстрый, со скоростью примерно 400 мм/день.
Аксональный транспорт поддерживает непрерывность аксона и синаптических мембран и восстанавливает белки, гликопротеины, ферменты и другие вещества, исчезающие в ходе локального расщепления, экзоцитоза в синаптическую щель и ретроградной миграции к нейрону. Все это происходит благодаря быстрому транспорту, на который не оказывают влияния процессы возбуждения. Транспорт продолжается после блокады потенциалов действия и не повышается при усиленной активности нерва. Аксональный транспорт осуществляется в обоих направлениях; центростремительный ток контролирует, по-видимому, синтез белков в нейроне и играет также роль «сигнала» для хроматолиза после аксотомии. Различные вещества, ферменты, передатчики и макромолекулы передвигаются в аксоне с разной скоростью.
Аксоплазматический транспорт можно зарегистрировать по накоплению веществ после нарушения непрерывности аксона и по наблюдению за продвижением меченых соединений после введения их в нейрон.
Белки, синтезируемые в теле клетки, синаптические медиаторные вещества и низкомолекулярные факторы спускаются по аксону к нервной терминали вместе с клеточными органеллами, в частности митохондриями. Для большинства веществ и органелл обнаружен ретроградный транспорт (по аксону к телу клетки): вирус полиомиелита, вирус герпеса, столбнячный токсин, а также ферменты – пероксидаза хрена, которая широко используется в нейроанатомии в качестве маркиратора. Ретроградный транспорт, видимо, является главным фактором регуляции синтеза белка в клетке. После перерезки аксона через несколько дней в соме начинается хроматолиз, что свидетельствует о нарушении синтеза белка. Быстрый аксонный транспорт зависит от достаточного снабжения метаболической энергии. Возможность транспорта создают микротрубочки диаметром 25 мкм, состоящие из белка тубулина, и некоторые нейрофибриллы, состоящие из белка актина, образующие транспортные нити. Транспортные нити скользят вдоль микротрубочек. При этом они взаимодействуют с выступами микротрубочек, происходит расщепление АТФ, которое и обеспечивает энергию для транспорта. Более медленно транспортируются крупные белки. Но считают, что сам транспортный механизм не является более медленным, однако вещества время от времени попадают в клеточные компартменты, которые не участвуют в транспорте. Медленный ток имеет, по-видимому, также отношение к аксональному росту. Аксоплазматический ток прекращается колхицином, что объясняется влиянием этого вещества на микротрубочки.
Физиология синапсов
Синапс (от греч. synapsis) обозначает соединение, связь – это специализированная зона контакта между нейронами или нейронами и другими возбудимыми образованиями, обеспечивающая передачу возбуждения с сохранением, изменением или исчезновением ее информационного значения. Данный термин был предложен Ч. Шеррингтоном (1897) для обозначения функционального контакта между нейронами. Справедливости ради нужно отметить, что еще в 60-х годах XIX столетия И.М. Сеченов подчеркивал, что вне межклеточной связи нельзя объяснить происхождение даже самых простых рефлексов.
Синапсы различают: 1) по их местоположению; 2) по способу передачи сигналов.
1) По местоположению выделяют синапсы центральные и периферические. Центральные синапсы – это синапсы, которые осуществляют контакт между нейронами в центральной нервной системе. К ним относятся аксо-аксональные синапсы, аксо-дендритические, аксо-соматические, дендро-дендритические (обнаружены гистологически; функциональное значение не вполне ясно). Центральные синапсы классифицируют также по знаку их действия – возбуждающие и тормозные. Кроме того, распространено деление синапсов по тому медиатору (передатчику), который осуществляет посредничество: адренергические синапсы, холинергические синапсы и др.
К периферическим синапсам относят нервно-мышечные, синапсы вегетативных ганглиев (синапсы, образованные преганглионарными и постганглионарными волокнами).
2) По способу передачи синапсы классифицируются как химические и электрические.
Для всех этих образований характерно наличие пресинаптической мембраны, синаптической щели (10-50 нм), постсинаптической мембраны. Пресинаптическая мембрана является мембраной пресинаптического окончания отростка нейрона (чаще всего аксона).
У человека и высших позвоночных животных наибольшее распространение получили химические синапсы. Химические синапсы в пресинаптическом окончании содержат везикулы с медиатором, химическим передатчиком. Ширина синаптической щели в среднем составляет 20 нм. На постсинаптической мембране содержатся рецепторы к данному медиатору, ферменты, разрушающие данный медиатор. Таким образом, постсинаптическая мембрана является рецепторной частью синапса, ею может быть специфически дифференцированный участок дендрита, тела нейрона и его аксона.
В электрическом синапсе не вырабатывается медиатор. Синаптическая щель несколько меньше, чем у химического синапса (2-4 нм). В синаптической щели между пре- и постсинаптической мембранами имеются белковые мостики-каналы шириной 1-2 нм, где движутся ионы и небольшие молекулы. Это способствует более низкому, чем у пресинаптической мембраны, сопротивлению постсинаптической мембраны. Поэтому возбуждение от пресинаптической мембраны к постсинаптической мембране в электрических синапсах передается электрическим путем, т.е. осуществляется эфаптическая передача. В отличие от химических синапсов, электрические синапсы отличаются большей скоростью проведения возбуждения, высокой надежностью передачи, возможностью двустороннего проведения.
Электрические синапсы обнаружены у крыс в вестибулярном ядре продолговатого мозга, в структурах дыхательного центра продолговатого мозга (при этом обсуждается их роль в механизмах автоматического ритмогенеза дыхания); у кошки электрические синапсы обнаружены между нейронами нижних олив, в структурах таламуса, между фоторецепторами сетчатки и горизонтальными клетками у рыб и др.
Но все-таки наибольшее распространение в процессе эволюции получили химические синапсы. Это обусловлено рядом свойств этих образований, которые имеют большое значение в организации деятельности нервной системы (рис. 1.4).
Рис. 1.4.
Синапс (рисунок взят из книги: Мозг / под ред. П.В. Симонова. М.: Мир, 1984)
⇐ Предыдущая3Следующая ⇒
Рекомендуемые страницы:
Функционирование нервной системы
Нормальное функционирование нервной системы зависит от передачи импульса и химических процессов в синапсе. Не менее важную роль играет создание нервных связей. Способность к обучению присутствует у людей именно благодаря возможности организма формировать новые соединения между нейронами.
Любое новое действие на стадии изучения требует постоянного контроля со стороны мозга. По мере его освоения образуются новые нейронные связи, со временем действие начинает выполняться автоматически (например, умение ходить).
Дендриты – это передающие волокна, составляющие примерно треть всей нервной ткани организма. Благодаря их взаимодействию с аксонами люди имеют возможность обучаться.

ДАП, зачастую, ведет к коме, в результате которой человек может перейти в вегетативное состояние.
Диффузия головного мозга чаще происходит с молодыми людьми, которые попадают в дорожно-транспортные происшествия, становятся жертвами драк и избиений с повреждением головного мозга, а также детьми, у которых и кома намного глубже, и неврологические нарушения грубее.
Вариант этой ЧМТ был впервые описан в 1956 за рубежом, а само название появилось в 1982 году. Состояние при ДАП тяжелое, протекающее в длительной коме, которая сразу возникает после травмы и характеризуется длительным течением.
Аксоны, поврежденные или разорванные в результате ЧМТ, и мелкие кровоизлияния равномерно распределяются по церебральным структурам, при этом нарушается иннервация всех зависимых органов. Самые распространенные места повреждений:
- ствол мозга;
- белое вещество;
- мозольное тело;
- волокна перивентрикулярные.
Диффузная травма головного мозга – это всегда серьезнейшее состояние с перспективой перехода в вегетативное состояние, нередок и смертельный исход.
Причины и морфология ДАП
Самые распространенные причины ЧМТ при ДАП:
- сильный ушиб о лобовые стекла в ДТП;
- падение;
- удар тяжелым предметом;
- синдром сотрясения у детей, при котором мозг подвергается сильному ушибу впоследствии резкой тряски, а также избиения, падения.
Синдром ДАП является результатом ушибов, вызванных угловым ускорением головы. При этом может и не быть прямого столкновения с объектом травмы.
Вследствие этого у некоторых пациентов не наблюдается переломов черепа и других видимых ранений, что несколько затрудняет диагностику. Статистика говорит о том, что именно повреждение по косой ведет к повреждению аксонов и возникновению ДАП.
Морфологически для этой травмы характерны три следующих очага повреждения:
- головной мозг;
- мозольное тело;
- стволовой мозг и диффузно распределенные разрывы.
Первые два очаговых признака – макроскопические, которые располагаются в виде гематомы до пяти мм, выглядящие как надорванная ткань с окровавленными краями. Через несколько дней после ЧМТ, очаг пигментируется и затем рубцуется. Рана в мозолистом теле может разрешиться образованием сосудистой кисты.
Аксональные нарушения при травме
Особенности клинической картины
Кома при диффузном повреждении головного мозга продолжается до трех недель и проявляется следующими симптомами:
- рефлекс зрачка нарушается;
- происходит паралич взгляда;
- дыхательный ритм меняется;
- повышается тонус мышц;
- появляется парез ног и рук;
- диагностируется гипертония;
- появляется фебрильная или субфебрильная температура и другие вегетативные расстройства.
Когда пациент с ДАП выходит из комы, он оказывается в вегетативном состоянии со следующими симптомами:
- глаза открываются на раздражители или самостоятельно;
- взгляд не сконцентрирован и не следует за движущимися предметами.
Вегетативное состояние, сопровождающееся нарушением рефлексов и симптомами разъединения функций мозговых полушарий, может продолжаться, в среднем, от нескольких дней до нескольких лет. Чем больше нахождение в нем, тем скорее появляются такие признаки полиневропатии, как:
- ослабление кистей рук;
- хаотическое движение мышц;
- расстройства нейротрофики;
- учащение пульса;
- отеки;
- тахипноэ и др.
После выхода из вегетативного состояния личность выпадает. Основные признаки нарушений после выхода:
- экстрапирамидные расстройства;
- расстройства психики, проявляющиеся отсутствием интереса к окружающей пациента действительности, агрессия, амнезия, слабоумие.
Степени поражения
Диффузное аксональное повреждение головного мозга бывает трех степеней тяжести:
- легкой – продолжительность комы от 6 до 24 часов, ЧМТ незначительна;
- средней– кома больше 24 часов, но черепно-мозговая травма умеренная;
- тяжелой – длительная кома, поражения значительные, происходит сдавливание мозга.
Тяжелая степень характеризуется массовым повреждением аксонов, которое приводят к кровоизлияниям в мозг. ДАП при этом может приводить к коме, продолжающейся годами и летальному исходу.
Начальное состояние мозга после выхода из такой комы восстановить не представляется возможным, единицы вернулись к более-менее нормальной жизни после таких повреждений.
Постановка диагноза
Диагноз диффузное поражение головного мозга ставится после компьютерной томографии, результаты которой в остром периоде отличаются увеличением объема мозговых полушарий, уменьшением или сдавливанием боковых расстояний и основания мозга. В белом веществе, стволе и мозолистом теле находятся мелкие кровоизлияния.
При обследовании наблюдается молниеносное развитие признаков ДАП и дегенерации.
ЭЭГ при синдроме ДАП выявляет изменения в подкорке и стволе мозга, диэнцефальный синдром. В анализе крови отмечается резкое повышение серотонина, значительное уменьшение дофамина и скачок адреналина, что предполагает терапию, направленную на снижение симпатико-адреналиновых симптомов.
В результате КТ определяют повышено внутричерепное давление или, наоборот, понижено либо отсутствует. В таком случае подключают датчик. Если на КТ отток ликвора в норме, то и внутричерепное давление будет в норме.

Поддержка состояния пострадавшего
После диффузной травмы головного мозга нередко диагностируются субдуральные ликворные скопления над большими полушариями мозга, которые в дальнейшем рассасываются, удалять хирургически их не надо.
Аксональное повреждение головного мозга чаще всего лечится консервативно. Нейрохирургическая операция проводится при сочетании разрывов и повреждений аксонов с очаговыми повреждениями, усиливающими сдавливание и провоцирующими гидроцефальный синдром.
В коме пациента подключают к ИВЛ, кормят парентерально и вводят следующие лекарства:
- для установления правильного кислотно-щелочного и водно-электролитного баланса;
- ноотропные и вазоактивные;
- устраняющие гипертензию или гипотонию;
- антибиотики для исключения сопутствующих инфекций.
Для возобновления психэмоциональной сферы вводят прием психостимуляторов.
После выхода из комы:
- вводят ноотропы и сосудистые лекарства для нормализации и улучшения состояния ЦНС, ноотропы также важны для последующей реабилитации;
- назначают препараты для улучшения метаболизма и биостимуляторы;
- проводят лечебную физкультуру для профилактики парезов;
- пациент занимается с логопедом.
Гормональные препараты при ДАП не назначают по ненадобности. После операции, если она все же состоялась (произошло сдавление головного мозга при сопутствующих травмах), вводят препараты, препятствующие образованию отеков, сосудистые средства, ноотропы, антихолинэстеразные, психотропные (во избежание развития агрессии и депрессии) и нейромедиаторы.
В период восстановления проводится такая же терапия, как и после выхода из комы.
Исход тяжелой травмы и ее последствия
Прогноз и последствия диффузного аксонального повреждения зависит от степени поражения аксонов головного мозга и тяжести вторичных признаков, таких как повышенное внутричерепное давление, гипергидроз, разбухание мозговых оболочек, психические нарушения, развитие слабоумия и т. д.
Исход также зависит от того как помогают лечебные методы, направленные на ликвидацию последствий ДАП – вторичные повреждения и осложнения.
Прогноз предполагает, что чем больше человек находился в коматозном состоянии, тем более риск развития неблагоприятных поражений, вплоть до летального исхода. Шансов на восстановление будет также минимум.

Но, к сожалению, чаще у выживших людей последующее течение синдрома ДАП может идти по двум сценариям:
- выход из коматозного состояния;
- переход в вегетативное состояние.
При первом варианте глаза больного открываются, и происходит слежение за предметами и фиксация взгляда на объекте. Это может иметь как спонтанный выход, так и направляемый организованными раздражителями, звуком и болевыми манипуляциями.
Затем пациент восстанавливает сознание, выполняет обращенные к нему просьбы, словесный багаж расширяется, он начинает общаться. Неврологические патологии при этом медленно регрессируют.
У больных, которые вышли из вегетативного состояния, развиваются экстрапирамидальные симптомы, сопровождающиеся психическими нарушениями (слабоумие, лабильность настроения, аспонтанность, спутанность сознания). При втором варианте летальный исход через определенное время неизбежен из-за истощения нейромедиаторов и соматических осложнений.
Современные исследования подтверждают регенерацию аксонов у детей и молодых людей, у которых мозг еще не завершил формирование. Происходит восстановление неврологических и психических процессов. При продолжительной коме оно проблематично, инвалидизация гарантирована.