Нейромедиаторы
Нейромедиаторы или нейротрансмиттеры — это химические молекулы, высвобождаемые нейронами. Они обеспечивают передачу сообщений от одного нейрона к другому в синапсах.
нейротрансмиттеры, нейромодуляторы
Нейротрансмиттеры были обнаружены в 1921 году биологом Отто Лоуи, который позже получил Нобелевскую премию за свою работу. До этого считалось, что межнейронная коммуникация (между нейронами) является результатом электрической коммуникации. Лоуи обнаружил, что эта концепция ошибочна, показывая, что нейроны взаимодействуют друг с другом посредством высвобождения химических веществ, называемых нейротрансмиттерами. С 1921 года по сегодняшний день было обнаружено более 60 различных типов нейротрансмиттеров.
Нейротрансмиттеры играют важную роль в нейронной коммуникации. Они являются химическими посланниками, которые передают сообщения между нервными клетками (нейронами) и другими клетками вашего тела, влияя на все, от настроения до непроизвольных движений. Этот процесс обычно называют нейротрансмиссией или синаптической передачей.
Хорошее функционирование нейротрансмиттеров обеспечивает нам стабильное функционирование нервной системы.

Как работают нейротрансмиттеры
Чтобы отправлять сообщения по всему телу, нейроны должны передавать сигналы для связи друг с другом. Но между ними нет физической связи, только место контакта между двумя нервными клетками, которое называется синапсом.
Чтобы связаться со следующей клеткой, нейрон посылает сигнал через синапс путем диффузии нейромедиатора.
Нейротрансмиттеры влияют на нейроны тремя способами: они могут быть возбудителями, ингибиторами или модуляторами. Излучатель возбуждения генерирует в рецепторном нейроне сигнал, называемый потенциалом действия. Тормозящий передатчик предотвращает это. Нейромодуляторы регулируют группы нейронов.
Некоторые нейротрансмиттеры, такие как дофамин, в зависимости от рецепторов, создают как возбуждающий, так и тормозящий эффекты.
Типы нейромедиаторов и их функции
Вот наиболее важные нейромедиаторы и роли, которые они выполняют:
-
Ацетилхолин. Основные функции ацетилхолина и механизмы его действия: среди различных типов нейромедиаторов ацетилхолин является нейромедиатором, ответственным за стимуляцию мышц. Он отвечает за активацию двигательных нейронов, а также участвует в различных областях мозга, связанных с обучением, памятью или возбуждением. Кроме того, ацетилхолин считается союзником в борьбе с неврологическими нарушениями.
Основная функция ацетилхолина — улучшить когнитивные навыки. Это основа функции воспоминаний, способности к концентрации и логического рассуждения. Он также отвечает за переход из состояния бдительности в состояние сна.
Ацетилхолин локализован в различных частях центральной нервной системы, а также в синапсах желез и мышц.
-
Дофамин. Он связан с удовольствием и чувством расслабления.

Среди основных функций дофамина — регуляция памяти, обучения, и он играет важную роль в принятии решений. Мотивация и любопытство также связаны с этим нейромедиатором.
Дофамин отвечает за регулирование эмоций удовольствия. Если мы регулярно употребляем никотин или алкоголь, они повышают уровень дофамина в нашем организме, вызывая это чувство удовольствия и расслабления.
Этот нейромедиатор находится в вегетативной нервной системе.
-
Норадреналин. Также известен как гормон стресса из-за его двойной роли, как гормона и как нейромедиатора. Это тип нейромедиатора, который имеет возбуждающую функцию, отвечающую за активацию симпатической нервной системы. Он участвует в поведении «бей или беги» в ответ на стресс.
Норадреналин связан с частотой сердечных сокращений и участвует в процессах внимания мозга и решения проблем. Среди его функций — также регулирование состояния физического и психического возбуждения.
Этот тип нейромедиатора локализован в основном в центральной нервной системе, а также в определенных областях симпатической области вегетативной нервной системы.
-
Гамма-аминомасляная кислота (ГАМК). Этот нейромедиатор выполняет тормозящую функцию нервной системы, предотвращая перевозбуждение, чтобы избежать таких реакций, как беспокойство или страх. Алкоголь и наркотики могут влиять на этот нейромедиатор, создавая ощущение субъективного контроля. Это самый распространенный возбуждающий нейротрансмиттер (75%) в центральной нервной системе.
ГАМК играет важную роль в контроле двигательной активности и зрения, поведения и реакции на стресс. Кроме того, это важный союзник в борьбе с тревогой. Он находится в головном мозге и коре больших полушарий.
-
Серотонин. Он также известен как гормон счастья. То есть, он выполняет две функции в нашем организме: как гормон и как нейротрансмиттер.
Серотонин играет важную роль в процессе пищеварения, в регуляции тепла тела, а также имеет большое влияние на сексуальное желание. Этот нейромедиатор присутствует в различных областях центральной нервной системы.
-
Глутамат. Он связан с нейромедиатором ГАМК и наиболее распространен в центральной нервной системе. Как ни парадоксально, избыток глутамата оказывает токсическое действие на наш организм, приводя к гибели нейронов.
Этот тип нейромедиатора связан с функциями памяти и обучения, а также с более сложными когнитивными функциями. Таким образом, дисбаланс этого нейромедиатора может вызывать нейродегенеративные патологии.
Глутамат находится в различных областях центральной нервной системы.
-
Болезнь Альцгеймера и болезнь Паркинсона связаны с дефицитом ацетилхолина. У пациентов, страдающих болезнью Альцгеймера, в головном мозге наблюдается потеря ацетилхолина до 90%.
-
Дофамин связан с синдромом дефицита внимания с гиперактивностью (СДВГ), поскольку дефицит этого нейротрансмиттера вызывает проблемы с концентрацией. Дофамин также связан с биполярными расстройствами в их маниакальной и гипоманиакальной фазах. Шизофрения и болезнь Паркинсона также связаны с этим нейромедиатором. В случае шизофрении из-за избытка, а в случае болезни Паркинсона из-за недостатка дофамина в двигательных областях, вызывающего неконтролируемый тремор.
-
Дефицит норадреналина связан с депрессивными расстройствами. Стресс имеет тенденцию истощать наши резервы, в то время как некоторые наркотики, такие как амфетамины или лекарства, резко повышают его уровень. Низкий уровень норадреналина снижает сексуальный аппетит.
-
Когда уровни ГАМК низкие, наше тело может страдать от тревожных расстройств, а его полное отсутствие связано с эпилептическими эпизодами. Низкий уровень ГАМК может вызывать мании и панические атаки.
-
Дефицит серотонина в нашем организме связан с такими заболеваниями, как депрессия, обсессивно-компульсивное расстройство (ОКР), а также с агрессией, наркоманией, расстройствами пищевого поведения и бессонницей.
-
Слишком низкий уровень глутамата связан с заболеваниями двигательных нейронов. Основное сопутствующее заболевание — это эксайтотоксичность, процесс, при котором нейроны серьезно повреждаются или разрушаются из-за чрезмерной активности. Эксайтотоксичность связана с апатией, а она — с нейродегенеративными заболеваниями, такими как болезнь Хантингтона, болезнь Альцгеймера и болезнь Паркинсона. Высокий уровень глутамата в нашем организме связан с эпилептическими эпизодами..
- Николлс Дж.Г., Мартин А.Р., Валлас Б.Дж., Фукс П.А. От нейрона к мозгу.
- Хухо Ф. Нейрохимия.
- Болдырев А.А., Ещенко Н.Д., Илюха В.А., Кяйвяряйнен Е.И. Нейрохимия.
- Каменская М.А., Каменский А.А. Основы нейробиологии.
Нейромедиаторы и заболевания

Миллиарды молекул нейротрансмиттеров постоянно работают, чтобы поддерживать работу мозга и управлять всем, от дыхания до сердцебиения и способности концентрироваться.
Многие нейротрансмиттеры связаны с рядом заболеваний:

Интересуетесь антивозрастной
и превентивной медициной?

Чтобы стать лучшим — учитесь
у лучших!
Эксперты со всего мира станут вашими наставниками
на пути изучение Anti-Age Expert. Подробнее
Список литературы
Статьи по теме
01.07.2021
Аминокислоты: свойства и польза
Аминокислоты – это группа из 22 органических соединений, которые выполняют функцию «строительных блоков» белков, причем как для растений, так и для животных. Какую роль они играют в организме человека и могут ли аминокислоты помочь в борьбе со старением?
16.06.2021
Мелатонин: гормон сна и долгой жизни
Мелатонин – это естественный гормон, который мозг выделяет в ответ на изменение освещения. Он помогает регулировать внутренние часы организма, сигнализируя о том, что пора ложиться спать.
Согласно растущему количеству исследований, гормон сна также может помочь в борьбе с симптомами менопаузы, облегчить боль и укрепить здоровье сердца и иммунитет.
20.04.2021
Роль нейромедиаторов в антивозрастной терапии
Молодой и стремительно реагирующий даже в зрелом возрасте мозг — одна из главных целей антивозрастной медицины. Ведь старение во многом связано с ухудшением когнитивных функций и потерей жизнеспособности нашего “центра управления”.
Разбираемся, что такое нейромедиаторы и какие вещества к ним относятся, а также почему ученые считают, что в будущем ожидается открытие новых.
Приветствуем в блоге Nooteria Labs. Мы производим комплексные добавки и подробно рассказываем о том, как они работают.
Сегодня речь пойдет о том, что такое нейромедиаторы, как именно они действуют в нервной системе и можно ли повлиять извне на процесс их синтеза.
Сила эмоций, мотивация к поступкам, выбор, запоминание информации – в процессе любых наших чувств и действий в организме работают нейромедиаторы, биологически активные химические вещества, которые передают сигналы между нервными клетками.
Открытие нейромедиаторов
О том, как происходит взаимодействие нейронов между собой, ученые задумывались еще в начале XX века. За исследования нервной системы в 1906 году была вручена Нобелевская премия двум исследователям: ее получили испанский врач Сатьяго Рамон-и-Кахаль и итальянский врач Камилло Гольджи. Причем мнения у ученых были противоположными: первый считал, что передача сигналов между нейронами происходит с помощью химических веществ, а второй – что с помощью электричества.
В середине XX века, с появлением современных электронных микроскопов, была сделана электронная фотография химического синапса – взаимодействия между нейронами.
На ней видны пузырьки-везикулы с нейромедиаторами – особыми химическими веществами. Было установлено, что с их помощью происходит передача импульсов между клетками, таким образом, подтвердилась первая теория. При этом электрические синапсы тоже бывают, но они занимают около 10 % случаев всех взаимодействий. Кроме того, встречаются синапсы смешанного типа.
После этого открытия сложилась нейронная теория строения нервной системы, где за единицу нервной ткани принимается нейрон, а синапс называется контактом между ними или с другими клетками организма.
Механика действия
В нервной системе находится огромное множество нервных клеток. Между собой эти клетки сообщаются с помощью специальных отростков – аксонов и дендритов. Между отростками есть микроскопические зазоры, которые называются синаптической щелью.
Синтез медиаторов происходит в клетке, затем в пузырьках-везикулах они движутся в окончание аксона и там попадают в синаптическую щель, соединяясь с молекулой-рецептором. После этого нейромедиаторы активируют рецепторы следующего нейрона. Такие рецепторы для каждого медиатора существуют свои, как ключи для замка.
После того, как рецепторы активированы, нейромедиатор разрушается или возвращается обратно в клетку, что называется обратным захватом. Каждую секунду миллиарды нейронов посылают друг другу сообщения, образуя огромное множество соединений.
Вспомогательную роль при этом играют специальные белки – какие-то участвуют в синтезе, другие в доставке, третьи – в процессе активации.
Когда нейромедиатор освобождается в синаптическую щель, происходит ряд биологических реакций. Сигналы передаются по сети нейронов, запуская процесс функционирования органа, движение мышц и многое другое. Передача импульса позволяет нервной системе соединяться с другими системами организма и контролировать их.
Эти процессы происходят с огромной скоростью и точностью, помогая реализации всех функций мозга.
Виды нейромедиаторов и их влияние
Нейромедиаторы делятся на несколько типов:
— По типу передачи нервного импульса в синапсе они могут быть химическими, электрическими и смешанными.
— По влиянию на клетку – возбуждающими и тормозными. Первые способствуют генерации электрических импульсов в нервных клетках, а вторые напротив, препятствуют возникновению нервных импульсов в нейронах.
— По типу используемого медиатора: холинэргическими (ацетилхолин), аминэргическими (адреналин, норадреналин, дофамин, серотонин и другие); аминокислотными (различные аминокислоты); пептидэргическими (нейропептиды — белки); пуринэргическими (производные аденозина).
То есть в роли нейромедиатора могут выступать и пептиды, и гормоны, и аминокислоты. Возникает закономерный вопрос — что считать нейромедиатором?
Существуют конкретные критерии, по которым то или иное вещество можно считать нейромедиатором:
— Оно должно синтезироваться и накапливаться в нейронах,
— После выделения оказывать специфическое действие на нейрон,
— Разрушаться в синаптической щели или возвращаться в клетку путем обратного захвата,
— При искусственном введении вещество должно оказывать тот же эффект, как и при естественном синтезе.
Рассмотрим подробнее одни из самых распространенных нейромедиаторов и их действие.
Глутамат – самый распространенный возбуждающий медиатор центральной нервной системы, вырабатывается во время стресса. От количества глутамата зависит способность усваивать новую информацию;
Гамма-аминомасляная кислота (ГАМК) – самый распространенный тормозной медиатор, нивелирует излишнее возбуждение. Улучшает память и продуктивность мышления;
Дофамин – отвечает за мотивацию, участвует в формировании чувства удовольствия, имеет взаимосвязь с принятием решений;
Серотонин – влияет на эмоциональную устойчивость, хорошее настроение. Для его синтеза нужны аминокислота триптофан и глюкоза;
Глицин – нормализует состояние нервной системы, улучшает работоспособность, способствует концентрации внимания.
Адреналин – нейромедиатор стресса, за короткое время влияет на скорость и силу;
Норадреналин – влияет на принятие быстрых решений, активизируется в экстремальных условиях;
Окситоцин – формирует уровень привязанности, доверительные отношения, эмоциональность. Вырабатывается при контакте с близкими людьми;
Эндорфин – имеет антистрессовое и обезболивающее действие, ускоряет процессы регенерации.
Это только часть из известных в настоящее время нейромедиаторов, ученые считают, что со временем будет открыто еще множество новых – ведь такую роль могут брать на себя различные вещества. Некоторые нейромедиаторы при этом обнаруживаются случайно, другие – путем систематического поиска.
Значение нейромедиаторов сложно переоценить в балансе неврологического и психического здоровья. Они играют важную роль для функционирования нервной системы и организма в целом, недостаток какого-либо из них может вызывать различные нарушения.
Улучшение синтеза
Нейромедиаторы вырабатываются организмом постоянно, но есть некоторые факторы, которые улучшают их выработку. Стимуляция синтеза позволит получить больше той самой базы для эффективной и быстрой передачи импульсов, а значит, в перспективе и улучшения работы нервной системы в целом.
Безусловно, существуют специфические условия для того или иного нейромедиатора. Но в целом можно сказать, что для хорошего функционирования полезны тренировки – интеллектуальные и физические, но при этом без переутомления, поскольку слишком большие нагрузки будут вызывать нарушение баланса.
На синтез многих нейромедиаторов будет влиять сбалансированное питание – с достаточным количеством аминокислот.
Однако регулировать уровень нейромедиаторов обычными продуктами может быть сложно. За счет приема специальных добавок можно добиться того же эффекта быстрее и эффективнее. В их числе лецитин, ноотропные комплексы, витамины группы В, ацетил L-карнитин и многие другие. Эти компоненты позволяют восполнить недостаток необходимых организму веществ и дать основу для эффективной работы.
Кстати, именно прямое влияние на нейромедиаторы лежит в основе нашего флагманского продукта MindBooster. Ключевой компонент в его составе DMAE (диметиламиноэтанол) приводит к увеличению синтеза одного из главных нейромедиаторов – ацетилхолина, о котором рассказывали в отдельной статье нашего блога.
Благодаря такому влиянию веществ и могут использоваться формулировки вроде «работать эффективнее» или «меньше уставать» – комплекс работает на улучшение выработки ацетилхолина, поставляя организму важные вещества, которые помогают мозгу справляться с большими нагрузками.
—
Если вам нравится наш контент, будем рады видеть вас среди подписчиков в группах Telegram и ВК. Там мы рассказываем самое интересное про механики работы нервной системы и мозга простым языком.
Как неврологи понимают эмоции
Прежде чем мы начнем говорить о том, как и какие вещества управляют нашими эмоциями, обозначим оптику, через которую мы будем их рассматривать. Наиболее полным кажется когнитивно-поведенческий подход. Именно его называют золотым стандартом современной психотерапии [1].
Когнитивно-поведенческий подход, работающий с неосознанными установками и поведенческими реакциями, выделяет 3 уровня:
-
Реактивный. Это уровень базовых, или витальных, эмоций, которые в том или ином виде существуют у всех позвоночных. У ребенка они проявляются уже в первые дни жизни. Они направляют нас к полезным стимулам вроде еды и помогают избежать тех, что причиняют вред. Реактивный уровень обеспечивается глубинными структурами мозга, которые у детей еще не контролируются корой. Ребенок отчаянно плачет, когда мама выходит из комнаты, и не успокаивается, пока его не возьмут на руки.
-
Повседневный. Этот уровень нужен для социальных взаимодействий. К примеру, нам приятнее иметь дело с человеком, проявляющим эмпатию и интерес. Это значит, что даже деловая коммуникация, основанная на понимании эмоционального состояния другого и искреннем интересе, будет гораздо более эффективной. Такие эмоции не требуют обдумывания: мы испытываем их, понимаем, что они значат, но делаем это инстинктивно.
-
Рефлексивный. Связан с мышлением. Такое есть только у человека, и этим мы обязаны префронтальной коре и лобным долям мозга — центрам, благодаря которым мы можем оценивать свое поведение и управлять им. Рефлексивный уровень связан с безопасностью, но, в отличие от реактивных эмоций, это — осознанное ощущение наличия или отсутствия опасности. У детей рефлексивные эмоции появляются только около 3–4 лет. Поэтому маленькому ребенку не объяснишь, что человек в белом халате всего лишь посмотрит, красное ли у него горло. Ребенок помнит, что однажды кто-то в белом халате сделал ему укол, а значит, снова будет больно. С другой стороны, даже те взрослые, кто чувствуют себя некомфортно в темноте, все-таки понимают, что их страх иррационален и у себя в спальне бояться совершенно нечего.
Какие структуры мозга отвечают за эмоции и реакции
Поговорим о том, где и как рождаются наши эмоции и реакции. Для этого заглянем в глубь человеческого мозга [2].
- Таламус. Является координирующей структурой. Его функция в том, чтобы переводить воспринятое извне — грохот, прикосновение, вспышку света — в нервный импульс.
- Миндалевидное тело, или амигдала. Если угодно, это наша тревожная кнопка. У детей до 3–4 лет амигдала функционирует независимо от коры. Генетическая предрасположенность к тревожности как раз обусловлена работой миндалевидного тела. Оно также отвечает за выражение эмоций, память и обучение.
- Гиппокамп. Это наша книга памяти, пишущаяся на основе полученного опыта. Эта структура хранит информацию, извлекает ее и помогает разобраться, как вести себя в аналогичных обстоятельствах в следующий раз. Каждый знает, что замешательство — первичная реакция на всё новое. Это как раз обусловлено тем, что гиппокамп просто не может отыскать ту или иную ситуацию в предыдущих записях.
- Префронтальная кора лобных долей. Необходима для сознательной оценки происходящего. Как мы уже отметили, префронтальная кора не работает полноценно у детей до 3–4 лет.
- Гипоталамус. Отвечает за такие вегетативные проявления, как сердцебиение, потоотделение и другие. Покраснели, услышав неудобный вопрос? Всё просто: сработал гипоталамус.

Рассмотрим теперь, как эти структуры работают при появлении приятного или, напротив, нежелательного раздражителя. Схема зависит от силы стимула. Если он резок и силен, импульс передается немедленно по пути таламус — амигдала — гипоталамус. Если же стимул недостаточно силен и не воспринимается как опасный сию же секунду, мы наблюдаем другую маршрутизацию: таламус — префронтальная кора — гиппокамп — гипоталамус. Здесь за счет включения таких компонентов, как сознательная оценка и сличение ситуации с предыдущим опытом, реагирование носит отложенный характер. То есть мы не действуем немедленно, но анализируем разные модели поведения, выбирая наиболее адекватную.
Что такое нейромедиаторы
Нейромедиаторы мозга как раз те вещества, что обеспечивают работу описанных механизмов. Без них нервные импульсы не могли бы передаваться четко, не формировались бы нервные пути.
Рассмотрим механизм нейромедиаторов. В нервной ткани есть множество синапсов — мельчайших образований, соединяющих нейроны. Внутри клетки нейромедиаторы компактно упакованы в специальные синаптические пузырьки. При возбуждении пузырьки лопаются и, высвобождаясь за пределы клетки, эти вещества попадают в синаптическую щель — контактное межклеточное пространство. Оттуда их молекулы попадают на рецепторы следующего нейрона в цепи. Так импульс распространяется по волокну, формируя нервный путь.
Этот способ генерации нервных импульсов называют химическим. Когда-то давно существовала теория, что они передаются и распространяются только с помощью электрических синапсов, то есть без участия специальных веществ. По мере развития нейронауки стало очевидно, что электрическая передача не самая эффективная. Во-первых, она крайне неточная, так как возбуждение распространяется неизбирательно, на все нейроны вокруг. С другой стороны, разряд, проходя по нервному волокну, затухает. Действие нейромедиаторов, напротив, точное и идет без потерь [3].
Классификация нейромедиаторов
Традиционно выделяют три группы нейромедиаторов:
- тормозные
- возбуждающие
- модулирующие
Как несложно догадаться, в первую входят вещества, которые угнетают активность соседних нейронов. Роль нейромедиаторов возбуждающего типа, напротив, состоит в активизации нервных клеток. Что касается третьей группы, то они изменяют восприимчивость нейронов к тормозным или возбуждающим влияниям.
С точки зрения химической структуры, можно говорить о самых разных видах нейромедиаторов, например:
- Аминокислоты (глутамат и ГАМК)
- Пептиды (окситоцин и эндорфины)
- Моноамины (серотонин, адреналин, норадреналин, дофамин, гистамин и др.)
Функции нейромедиаторов
Кажется логичным разделить эти вещества на 2 большие группы: способствующие и препятствующие хранению и извлечению информации.
Нейромедиаторы, способствующие хранению и извлечению информации
Благодаря им мы реагируем на стимул — пугаемся, злимся, радуемся. Эти реакции возникают на основе опыта, и память играет здесь ключевое значение.
Глутамат
Больше всего в мозге именно его: он необходим для каждого нового процесса. Так, благодаря выделению глутамата мозг запоминает, что звук хрустнувшего кресла связан с падением. В следующий раз, услышав этот звук, мы рефлекторно сделаем попытку привстать. Чем ярче событие, тем больше его выделяется.
В этом свете не кажется таким удивительным, что некоторые люди наступают на одни и те же грабли, выбирают одни и те же модели поведения, похожих партнеров и так далее. В таких случаях коррекция поведения требует большой работы и часто нужна помощь психотерапевта. Цель психотерапии здесь — сломать старые глутаматные цепочки и сформировать новые.
Норадреналин
Блокирует кору в момент стресса. Его задача — сообщить нам: «Не думай — спасайся!». Предположим, за вами погналась собака. Вряд ли вы будете задумываться о том, кто бегает быстрее — вы или собака. Скорее, вы просто побежите вперед.
Этот моноамин также обеспечивает точность нахождения информации и подавляет страх. Вероятно, вы слышали рассказы, как под воздействием сильного стресса, например при внезапном пожаре или спасаясь от преследования, люди выпрыгивали из окон, ничего себе не сломав. Конечно, нейромедиаторы организма тут ни при чем: этим людям повезло и высота, скорее всего, была низкой. Однако норадреналин, возможно, помог им сориентироваться и правильно оценить, из какого окна лучше выпрыгнуть и куда и как приземлиться.
Кортизол
Усиливает действие норадреналина и повышает возбудимость миндалины, адаптируя организм к режиму сверхтревоги. Если вы когда-нибудь слышали выражение «море по колено», знайте: это про кортизол. В таком состоянии мы готовы сразиться с противником гораздо сильнее нас. Библейский богатырь Самсон, по легенде, разорвал пасть льву. Вероятно, успеху этой схватки легендарный Самсон был обязан этому моноамину.

Кортизол интересен тем, что способен искажать работу гиппокампа, нашей книги памяти, в том числе преуменьшая значимость события в прошлом. На этом свойстве основан его обратный эффект: когда его уровень высок, извлечение информации затруднено.
Дофамин
Это наша основа внимательности и восприимчивости к окружающей среде. Говорят, у страха глаза велики — это как раз результат работы дофаминовой системы. Представьте себе, что идете ночью через темный лес или кладбище и слышите за спиной шаги. Типичная норадреналиновая реакция в этой ситуации — бежать, в то время как дофаминовая — замереть и прислушаться.
Он также обеспечивает мотивацию и контроль деятельности на пути к цели. Допустим, вы мечтаете о красивом мышечном рельефе, ведь впереди пляжный сезон. Сейчас вечер, и вы счастливы, что сделали столько-то подходов в зале. При этом завтра вы готовы установить новый рекорд — и всё ради одной цели. Если так, вас стоит поздравить: от недостатка дофамина вы не страдаете, а вашей мотивации можно позавидовать.
Нейромедиаторы, препятствующие хранению и извлечению информации
Эти вещества дают то, что можно определить как счастье в моменте. Счастливые часов, как известно, не наблюдают, и всё благодаря им.
Серотонин
Моноамин, снижающий потребность в информации. Здесь можно вспомнить ту легкую усталость после какого-нибудь приятного занятия, например секса. Разве в этом состоянии хочется скролить новостную ленту?
Это же действие очень наглядно как побочный эффект при терапии тревожных расстройств и депрессий с помощью СИОЗС (селективных ингибиторов обратного захвата серотонина). Как мы уже сказали, если серотонин повышается, пациенту хорошо здесь и сейчас. Правда, иногда в таком состоянии уходит не только тревога, но и мотивация: не чувствуется никакой необходимости выходить за пределы того, что называют зоной комфорта. Вспоминается случай, когда СИОЗС принесли облегчение тревожному пациенту, который тогда усиленно готовился к экзаменам. Но возникла другая проблема: пациент забросил подготовку и не мог заставить себя заниматься. Разумеется, препарат пришлось сменить. Такое иногда встречается, но этого не стоит бояться: подобрать другой СИОЗС вполне реально.
Еще серотонин опосредует то, что называют объективным взглядом со стороны. Предположим, начальник был с нами резок. Конечно, мы расстроимся, но мы также можем посмотреть на случившееся иначе. «Ах, да, — вспоминается нам, — он же недавно развелся с женой». Как ни в чем не бывало мы продолжаем работать дальше и уже почти не злимся на начальника.
Эндорфины
Как и серотонин, снижают бдительность. А еще блокируют передачу болевых импульсов и вызывают эйфорию. Здесь можно упомянуть любопытное состояние, знакомое, например, участникам спортивных марафонов. Эффект состоит в том, что в определенный момент спортсмен перестает чувствовать усталость и боль и испытывает нечто сродни легкому опьянению. Это состояние, известное также как эйфория бегуна, развивается вследствие выброса эндорфинов.
Гамма-аминомасляная кислота
Это вещество — главный тормозной нейромедиатор в центральной нервной системе. Ее основная функция — предотвратить перевозбуждение. Препараты вроде Феназепама, иногда применяемые в терапии тревоги, воздействуют как раз на систему ГАМК, вызывая ощущение спокойствия и безопасности.
Как нейромедиаторы связаны с заболеваниями
Низкий уровень серотонина ассоциируется с подавленным настроением. Такие пациенты часто испытывают сложности с засыпанием, а, проснувшись, не ощущают бодрости. Им трудно радоваться привычным вещам, они сосредоточены на проблемах и пытаются найти пути их решения. От них окружающие часто слышат что-то вроде «У меня никогда ничего не получается» или «Только у меня всё плохо».
Нехватка серотонина лежит в основе тревожных расстройств. При его недостатке и дисбалансе других нейроаминов у пациентов развивается депрессия — механизм, известный в науке как моноаминовая теория депрессии [4].

Снижение норадреналина приводит к возникновению хронического болевого синдрома, когда боль мучит на протяжении месяцев. Это связано с тем, что при столь длительном сохранении боли норадреналин истощается, и тогда даже незначительный раздражитель вызывает полноценный болевой синдром.
Низкий норадреналин дает в перспективе снижение серотонина и, возможно, ассоциированные с этим депрессии.
Излишек дофамина провоцирует возбуждение. Известно, что с этим связаны шизофрения, бредовые расстройства, а также биполярное расстройство в стадии мании, когда на смену депрессивному эпизоду приходит период двигательного и психического возбуждения. В этом состоянии пациент видит или слышит то, чего нет. Ему вдруг начинает казаться, что он находится под воздействием человека, который, возможно, даже не знает о его существовании.
Он также влияет на качество движения, обеспечивая координацию и плавность, и опосредует двигательные автоматизмы вроде тех, что позволяют нам не задумываясь переставлять ноги при ходьбе или завязывать шнурки. Снижение дофамина дает болезнь Паркинсона. У таких больных заметно дрожание конечностей, высокий мышечный тонус и замедленные движения. Избыток, напротив, проявляется в навязчивых бесконтрольных движениях.
Еще дофаминовая система отвечает за формирование зависимостей. Психоактивные вещества изменяют физиологию мотивации, обеспечивая положительное подкрепление в виде эйфории, которая наступает после употребления. Любопытно, что дофаминовая основа есть и в других зависимостях, например цифровой. Доказано, что последняя связана с ростом дофаминовых рецепторов на фоне высокого норадреналина и низкого серотонина.
Говоря о зависимостях, нельзя не упомянуть гамма-аминомасляную кислоту. Алкоголь воздействует на систему ГАМК, что дает ощущение некоторого спокойствия. Это именно тот эффект, который имеют в виду те, кто говорят, что алкоголь помогает им снять стресс. Проблема в том, что ГАМК-рецепторы «устают» при избыточной стимуляции. Так возникает потребность в увеличении дозы и развивается алкоголизм.
Выводы
-
Когнитивно-поведенческая терапия выделяет 3 уровня эмоций: реактивный (биологический), повседневный (социальный) и рефлексивный (осознанный). В них задействованы разные отделы мозга: от более простых с эволюционной точки зрения до более сложных.
-
К ключевым структурам, обеспечивающим эмоции и реакции, относят таламус, миндалевидное тело, гиппокамп, префронтальную кору и гипоталамус. Важным является тот факт, что эмоции опосредованы памятью и прошлым опытом, но могут также формироваться без участия коры.
-
Функционирование указанных выше структур и уровней как единого целого возможно благодаря системам нейромедиаторов — биологически активных веществ, точно и эффективно передающих нервные импульсы.
-
Нейромедиаторы классифицируют по разным основаниям. Например, по действию (тормозные, возбуждающие и модулирующие) и по химическому составу (аминокислоты, пептиды, моноамины и др.).
-
Говоря об участии основных нейромедиаторов в управлении эмоциями и реакциями, удобно делить их на 2 группы: те, что способствуют хранению и извлечению информации, и те, что этому препятствуют.
-
Низкий серотонин провоцирует тревожные расстройства и депрессии. Недостаток норадреналина тоже может приводить к депрессиям. Он же участвует в формировании хронического болевого синдрома. Заболевания, ассоциированные с дофамином, возникают как на фоне его снижения (болезнь Паркинсона), так и при его повышении (бредовые расстройства, шизофрения, биполярное расстройство в фазе мании). Кроме того, дофаминовая система участвует в формировании зависимостей, а алкогольная зависимость также связана с системой ГАМК.
Клиника Наше Время — место, где вам помогут. Записывайтесь на прием, чтобы получить консультацию невролога и подобрать лечение.
Источники
David D., Cristea I., Hofmann S. G. Why cognitive behavioral therapy is the current gold standard of psychotherapy // Front Psychiatry. — 2018; 9:4.
Дуус П. Топический диагноз в неврологии. Анатомия. Физиология. Клиника // ИПЦ «Вазар Ферро». — Москва, 1996; 199–248.
Purves D., Augustine G.J., Fitzpatrick D., et al., editors. What defines a neurotransmitter? // Neuroscience. 2nd edition. Sunderland (MA): Sinauer Associates. — 2001.
Deakin J. The role of serotonin in depression and anxiety // European Psychiatry. — 1998; 13(2):57–63.
For an introduction to concepts and terminology used in this article, see Chemical synapse.
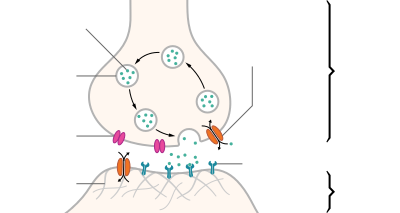
| Structure of a typical chemical synapse |
|---|
|
Postsynaptic Voltage- Synaptic Neurotransmitter Receptor Neurotransmitter Axon terminal Synaptic cleft Dendrite |
A neurotransmitter is a signaling molecule secreted by a neuron to affect another cell across a synapse. The cell receiving the signal, or target cell, may be another neuron, but could also be a gland or muscle cell.[1]
Neurotransmitters are released from synaptic vesicles into the synaptic cleft where they are able to interact with neurotransmitter receptors on the target cell. The neurotransmitter’s effect on the target cell is determined by the receptor it binds. Many neurotransmitters are synthesized from simple and plentiful precursors such as amino acids, which are readily available and often require a small number of biosynthetic steps for conversion.
Neurotransmitters are essential to the function of complex neural systems. The exact number of unique neurotransmitters in humans is unknown, but more than 100 have been identified.[2] Common neurotransmitters include glutamate, GABA, acetylcholine, glycine and norepinephrine.
Mechanism and cycle[edit]
Synthesis[edit]
Neurotransmitters are generally synthesized in neurons and are made up of, or derived from, precursor molecules that are found abundantly in the cell. Classes of neurotransmitters include amino acids, monoamines, and peptides. Monoamines are synthesized by altering a single amino acid. For example, the precursor of serotonin is the amino acid tryptophan. Peptide transmitters, or neuropeptides, are protein transmitters that often are released together with other transmitters to have a modulatory effect.[3] Purine neurotransmitters, like ATP, are derived from nucleic acids. Other neurotransmitters are made up of metabolic products like nitric oxide and carbon monoxide.[citation needed]
| Examples | |
|---|---|
| Amino Acid | glycine, glutamate |
| Monoamines | serotonin, epinephrine, dopamine |
| Peptides | substance P, opioids |
| Purines | ATP, GTP |
| Other | nitric oxide, carbon monoxide |
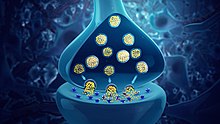
Synaptic vesicles containing neurotransmitters
Storage[edit]
Neurotransmitters are generally stored in synaptic vesicles, clustered close to the cell membrane at the axon terminal of the presynaptic neuron. However, some neurotransmitters, like the metabolic gases carbon monoxide and nitric oxide, are synthesized and released immediately following an action potential without ever being stored in vesicles.[4]
Release[edit]
Generally, a neurotransmitter is released at the presynaptic terminal in response to an electrical signal called an action potential in the presynaptic neuron. However, low level ‘baseline’ release also occurs without electrical stimulation. Neurotransmitters are released into and diffuse across the synaptic cleft, where they bind to specific receptors on the membrane of the postsynaptic neuron.[5]
Receptor interaction[edit]
After being released into the synaptic cleft, neurotransmitters diffuse across the synapse where they are able to interact with receptors on the target cell. The effect of the neurotransmitter is dependent on the identity of the target cell’s receptors present at the synapse. Depending on the receptor, binding of neurotransmitters may cause excitation, inhibition, or modulation of the postsynaptic neuron. See below for more information.[citation needed]
Elimination[edit]
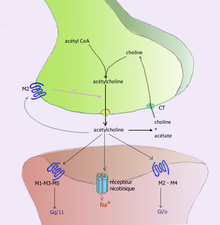
Acetylcholine is cleaved in the synaptic cleft into acetic acid and choline
In order to avoid continuous activation of receptors on the post-synaptic or target cell, neurotransmitters must be removed from the synaptic cleft.[6] Neurotransmitters are removed through one of three mechanisms:
- Diffusion – neurotransmitters drift out of the synaptic cleft, where they are absorbed by glial cells. These glial cells, usually astrocytes, absorb the excess neurotransmitters. In the glial cell, neurotransmitters are broken down by enzymes or pumped back into
- Enzyme degradation – proteins called enzymes break the neurotransmitters down.
- Reuptake – neurotransmitters are reabsorbed into the pre-synaptic neuron. Transporters, or membrane transport proteins, pump neurotransmitters from the synaptic cleft back into axon terminals (the presynaptic neuron) where they are stored for reuse.
For example, acetylcholine is eliminated by having its acetyl group cleaved by the enzyme acetylcholinesterase; the remaining choline is then taken in and recycled by the pre-synaptic neuron to synthesize more acetylcholine.[7] Other neurotransmitters are able to diffuse away from their targeted synaptic junctions and are eliminated from the body via the kidneys, or destroyed in the liver. Each neurotransmitter has very specific degradation pathways at regulatory points, which may be targeted by the body’s regulatory system or medication. Cocaine blocks a dopamine transporter responsible for the reuptake of dopamine. Without the transporter, dopamine diffuses much more slowly from the synaptic cleft and continues to activate the dopamine receptors on the target cell.[8]
Discovery[edit]
Until the early 20th century, scientists assumed that the majority of synaptic communication in the brain was electrical. However, through histological examinations by Ramón y Cajal, a 20 to 40 nm gap between neurons, known today as the synaptic cleft, was discovered. The presence of such a gap suggested communication via chemical messengers traversing the synaptic cleft, and in 1921 German pharmacologist Otto Loewi confirmed that neurons can communicate by releasing chemicals. Through a series of experiments involving the vagus nerves of frogs, Loewi was able to manually slow the heart rate of frogs by controlling the amount of saline solution present around the vagus nerve. Upon completion of this experiment, Loewi asserted that sympathetic regulation of cardiac function can be mediated through changes in chemical concentrations. Furthermore, Otto Loewi is credited with discovering acetylcholine (ACh) – the first known neurotransmitter.[9]
Identification[edit]
There are four main criteria for identifying neurotransmitters:[citation needed]
- The chemical must be synthesized in the neuron or otherwise be present in it.
- When the neuron is active, the chemical must be released and produce a response in some targets.
- The same response must be obtained when the chemical is experimentally placed on the target.
- A mechanism must exist for removing the chemical from its site of activation after its work is done.
However, given advances in pharmacology, genetics, and chemical neuroanatomy, the term «neurotransmitter» can be applied to chemicals that:
- Carry messages between neurons via influence on the postsynaptic membrane.
- Have little or no effect on membrane voltage, but have a common carrying function such as changing the structure of the synapse.
- Communicate by sending reverse-direction messages that affect the release or reuptake of transmitters.
The anatomical localization of neurotransmitters is typically determined using immunocytochemical techniques, which identify the location of either the transmitter substances themselves or of the enzymes that are involved in their synthesis. Immunocytochemical techniques have also revealed that many transmitters, particularly the neuropeptides, are co-localized, that is, a neuron may release more than one transmitter from its synaptic terminal.[10] Various techniques and experiments such as staining, stimulating, and collecting can be used to identify neurotransmitters throughout the central nervous system.[11]
Actions[edit]
Neurons form elaborate networks through which nerve impulses – action potentials – travel. Each neuron has as many as 15,000 connections with neighboring neurons.[citation needed]
Neurons do not touch each other (except in the case of an electrical synapse through a gap junction); instead, neurons interact at contact points called synapses: a junction within two nerve cells, consisting of a miniature gap within which impulses are carried by a neurotransmitter. A neuron transports its information by way of a nerve impulse called an action potential. When an action potential arrives at the synapse’s presynaptic terminal button, it may stimulate the release of neurotransmitters. These neurotransmitters are released into the synaptic cleft to bind onto the receptors of the postsynaptic membrane and influence another cell, either in an inhibitory or excitatory way. The next neuron may be connected to many more neurons, and if the total of excitatory influences minus inhibitory influences is great enough, it will also «fire». That is to say, it will create a new action potential at its axon hillock, releasing neurotransmitters and passing on the information to yet another neighboring neuron.[citation needed]
Modulation[edit]
A neurotransmitter may have an excitatory, inhibitory or modulatory effect on the target cell. The effect is determined by the receptors the neurotransmitter interacts with at the post-synaptic membrane. Neurotransmitter influences trans-membrane ion flow either to increase (excitatory) or to decrease (inhibitory) the probability that the cell with which it comes in contact will produce an action potential. Synapses containing receptors with excitatory effects are called Type I synapses, while Type II synapses contain receptors with inhibitory effects.[12] Thus, despite the wide variety of synapses, they all convey messages of only these two types. The two types are different appearance and are primarily located on different parts of the neurons under its influence.[13] Receptors with modulatory effects are spread throughout all synaptic membranes and binding of neurotransmitters sets in motion signaling cascades that help the cell regulate its function.[14] Binding of neurotransmitters to receptors with modulatory effects can have many results. For example, it may result in an increase or decrease in sensitivity to future stimulus by recruiting more or less receptors to the synaptic membrane.
Type I (excitatory) synapses are typically located on the shafts or the spines of dendrites, whereas type II (inhibitory) synapses are typically located on a cell body. In addition, Type I synapses have round synaptic vesicles, whereas the vesicles of type II synapses are flattened. The material on the presynaptic and post-synaptic membranes is denser in a Type I synapse than it is in a type II, and the type I synaptic cleft is wider. Finally, the active zone on a Type I synapse is larger than that on a Type II synapse.
The different locations of type I and type II synapses divide a neuron into two zones: an excitatory dendritic tree and an inhibitory cell body. From an inhibitory perspective, excitation comes in over the dendrites and spreads to the axon hillock to trigger an action potential. If the message is to be stopped, it is best stopped by applying inhibition on the cell body, close to the axon hillock where the action potential originates. Another way to conceptualize excitatory–inhibitory interaction is to picture excitation overcoming inhibition. If the cell body is normally in an inhibited state, the only way to generate an action potential at the axon hillock is to reduce the cell body’s inhibition. In this «open the gates» strategy, the excitatory message is like a racehorse ready to run down the track, but first, the inhibitory starting gate must be removed.[15]
Neurotransmitter actions[edit]
As explained above, the only direct action of a neurotransmitter is to activate a receptor. Therefore, the effects of a neurotransmitter system depend on the connections of the neurons that use the transmitter, and the chemical properties of the receptors.
- Glutamate is used at the great majority of fast excitatory synapses in the brain and spinal cord. It is also used at most synapses that are «modifiable», i.e. capable of increasing or decreasing in strength. Modifiable synapses are thought to be the main memory-storage elements in the brain. Excessive glutamate release can overstimulate the brain and lead to excitotoxicity causing cell death resulting in seizures or strokes.[16] Excitotoxicity has been implicated in certain chronic diseases including ischemic stroke, epilepsy, amyotrophic lateral sclerosis, Alzheimer’s disease, Huntington disease, and Parkinson’s disease.[17]
- GABA is used at the great majority of fast inhibitory synapses in virtually every part of the brain. Many sedative/tranquilizing drugs act by enhancing the effects of GABA.[18] Correspondingly, glycine is the inhibitory transmitter in the spinal cord.
- Acetylcholine was the first neurotransmitter discovered in the peripheral and central nervous systems. It activates skeletal muscles in the somatic nervous system and may either excite or inhibit internal organs in the autonomic system.[11] It is distinguished as the transmitter at the neuromuscular junction connecting motor nerves to muscles. The paralytic arrow-poison curare acts by blocking transmission at these synapses. Acetylcholine also operates in many regions of the brain, but using different types of receptors, including nicotinic and muscarinic receptors.[19]
- Dopamine has a number of important functions in the brain; this includes regulation of motor behavior, pleasures related to motivation and also emotional arousal. It plays a critical role in the reward system; Parkinson’s disease has been linked to low levels of dopamine and schizophrenia has been linked to high levels of dopamine.[20]
- Serotonin is a monoamine neurotransmitter. Most is produced by and found in the intestine (approximately 90%), and the remainder in central nervous system neurons. It functions to regulate appetite, sleep, memory and learning, temperature, mood, behaviour, muscle contraction, and function of the cardiovascular system and endocrine system. It is speculated to have a role in depression, as some depressed patients are seen to have lower concentrations of metabolites of serotonin in their cerebrospinal fluid and brain tissue.[21]
- Norepinephrine which is synthesized in the central nervous system and sympathetic nerves, modulates the responses of the autonomic nervous system, the sleep patterns, focus and alertness. It is synthesized from tyrosine.
- Epinephrine which is also synthesized from tyrosine is released in the adrenal glands and the brainstem. It plays a role in sleep, with one’s ability to become and stay alert, and the fight-or-flight response.
Types[edit]
There are many different ways to classify neurotransmitters. Dividing them into amino acids, peptides, and monoamines is sufficient for some classification purposes.[22]
Major neurotransmitters:
- Amino acids: glutamate,[23] aspartate, D-serine, gamma-Aminobutyric acid (GABA),[nb 1] glycine
- Gasotransmitters: nitric oxide (NO), carbon monoxide (CO), hydrogen sulfide (H2S)
- Monoamines:
- Catecholamines: dopamine (DA), norepinephrine (noradrenaline, NE), epinephrine (adrenaline)
- Indolamines: serotonin (5-HT, SER), melatonin
- histamine
- Trace amines: phenethylamine, N-methylphenethylamine, tyramine, 3-iodothyronamine, octopamine, tryptamine, etc.
- Peptides: oxytocin, somatostatin, substance P, cocaine and amphetamine regulated transcript, opioid peptides[24]
- Purines: adenosine triphosphate (ATP), adenosine
- Others: acetylcholine (ACh), anandamide, etc.
In addition, over 100 neuroactive peptides have been found, and new ones are discovered regularly.[25][26] Many of these are co-released along with a small-molecule transmitter. Nevertheless, in some cases, a peptide is the primary transmitter at a synapse. Beta-Endorphin is a relatively well-known example of a peptide neurotransmitter because it engages in highly specific interactions with opioid receptors in the central nervous system.
Single ions (such as synaptically released zinc) are also considered neurotransmitters by some,[27] as well as some gaseous molecules such as nitric oxide (NO), carbon monoxide (CO), and hydrogen sulfide (H2S).[28] The gases are produced in the neural cytoplasm and are immediately diffused through the cell membrane into the extracellular fluid and into nearby cells to stimulate production of second messengers. Soluble gas neurotransmitters are difficult to study, as they act rapidly and are immediately broken down, existing for only a few seconds.
The most prevalent transmitter is glutamate, which is excitatory at well over 90% of the synapses in the human brain.[23] The next most prevalent is gamma-Aminobutyric Acid, or GABA, which is inhibitory at more than 90% of the synapses that do not use glutamate. Although other transmitters are used in fewer synapses, they may be very important functionally: the great majority of psychoactive drugs exert their effects by altering the actions of some neurotransmitter systems, often acting through transmitters other than glutamate or GABA. Addictive drugs such as cocaine and amphetamines exert their effects primarily on the dopamine system. The addictive opiate drugs exert their effects primarily as functional analogs of opioid peptides, which, in turn, regulate dopamine levels.
List of neurotransmitters, peptides, and gaseous signaling molecules[edit]
| Category | Name | Abbreviation | Metabotropic | Ionotropic |
|---|---|---|---|---|
| Small: Amino acids (Arg) | Arginine | Arg, R | α2-Adrenergic receptors, imidazoline receptors | NMDA receptors |
| Small: Amino acids | Aspartate | Asp, D | – | NMDA receptors |
| Small: Amino acids | Glutamate | Glu, E | Metabotropic glutamate receptors | NMDA receptors, kainate receptors, AMPARs |
| Small: Amino acids | Gamma-aminobutyric acid | GABA | GABAB receptors | GABAA receptors, GABAA-ρ receptors |
| Small: Amino acids | Glycine | Gly, G | – | NMDA receptors, glycine receptors |
| Small: Amino acids | D-serine | Ser, S | – | NMDA receptors |
| Small: Acetylcholine | Acetylcholine | ACh | Muscarinic acetylcholine receptors | Nicotinic acetylcholine receptors |
| Small: Monoamine (Phe/Tyr) | Dopamine | DA | Dopamine receptors, trace amine-associated receptor 1[29][30] | – |
| Small: Monoamine (Phe/Tyr) | Norepinephrine (noradrenaline) | NE, NAd | Adrenergic receptors | – |
| Small: Monoamine (Phe/Tyr) | Epinephrine (adrenaline) | Epi, Ad | Adrenergic receptors | – |
| Small: Monoamine (Trp) | Serotonin (5-hydroxytryptamine) | 5-HT | Serotonin receptors (all except 5-HT3) | 5-HT3 |
| Small: Monoamine (His) | Histamine | H | Histamine receptors | – |
| Small: Trace amine (Phe) | Phenethylamine | PEA | Human trace amine-associated receptors: hTAAR1, hTAAR2 | – |
| Small: Trace amine (Phe) | N-methylphenethylamine | NMPEA | hTAAR1 | – |
| Small: Trace amine (Phe/Tyr) | Tyramine | TYR | hTAAR1, hTAAR2 | – |
| Small: Trace amine (Phe/Tyr) | octopamine | Oct | hTAAR1 | – |
| Small: Trace amine (Phe/Tyr) | Synephrine | Syn | hTAAR1 | – |
| Small: Trace amine (Trp) | Tryptamine | hTAAR1, various serotonin receptors | – | |
| Small: Trace amine (Trp) | N-methyltryptamine | NMT | hTAAR1, various serotonin receptors | – |
| Lipid | Anandamide | AEA | Cannabinoid receptors | – |
| Lipid | 2-Arachidonoylglycerol | 2-AG | Cannabinoid receptors | – |
| Lipid | 2-Arachidonyl glyceryl ether | 2-AGE | Cannabinoid receptors | – |
| Lipid | N-Arachidonoyl dopamine | NADA | Cannabinoid receptors | TRPV1 |
| Lipid | Virodhamine | Cannabinoid receptors | – | |
| Small: Purine | Adenosine | Ado | Adenosine receptors | – |
| Small: Purine | Adenosine triphosphate | ATP | P2Y receptors | P2X receptors |
| Small: Purine | Nicotinamide adenine dinucleotide | β-NAD | P2Y receptors | P2X receptors |
| Category | Name | Abbreviation | Metabotropic | Ionotropic |
|---|---|---|---|---|
| Bombesin-like peptides | Bombesin | BBR1-2-3 | – | |
| Bombesin-like peptide | Gastrin releasing peptide | GRP | – | – |
| Bombesin-like peptide | Neuromedin B | NMB | Neuromedin B receptor | – |
| Bradykinins | Bradykinin | B1, B2 | – | |
| Calcitonin/CGRP family | Calcitonin | Calcitonin receptor | – | |
| Calcitonin/CGRP family | Calcitonin gene-related peptide | CGRP | CALCRL | – |
| Corticotropin-releasing factors | Corticotropin-releasing hormone | CRH | CRHR1 | – |
| Corticotropin-releasing factors | Urocortin | CRHR1 | – | |
| Galanins | Galanin | GALR1, GALR2, GALR3 | – | |
| Galanins | Galanin-like peptide | GALR1, GALR2, GALR3 | – | |
| Gastrins | Gastrin | Cholecystokinin B receptor | – | |
| Gastrins | Cholecystokinin | CCK | Cholecystokinin receptors | – |
| Granins | Chromogranin A | ChgA | – | – |
| Melanocortins | Adrenocorticotropic hormone | ACTH | ACTH receptor | – |
| Melanocortins | Proopiomelanocortin | POMC | Melanocortin 4 receptor | – |
| Melanocortins | Melanocyte-stimulating hormones | MSH | Melanocortin receptors | – |
| Neurohypophyseals | Vasopressin | AVP | Vasopressin receptors | – |
| Neurohypophyseals | Oxytocin | OT | Oxytocin receptor | – |
| Neurohypophyseals | Neurophysin I | – | – | |
| Neurohypophyseals | Neurophysin II | – | – | |
| Neurohypophyseals | Copeptin | – | – | |
| Neuromedins | Neuromedin U | NmU | NmUR1, NmUR2 | – |
| Neuropeptide B/W | Neuropeptide B | NPB | NPBW1, NPBW2 | – |
| Neuropeptide B/W | Neuropeptide S | NPS | Neuropeptide S receptors | – |
| Neuropeptide Y | Neuropeptide Y | NY | Neuropeptide Y receptors | – |
| Neuropeptide Y | Pancreatic polypeptide | PP | – | – |
| Neuropeptide Y | Peptide YY | PYY | – | – |
| Opioids | Enkephalins | δ-Opioid receptor | – | |
| Opioids | Dynorphins | κ-Opioid receptor | – | |
| Opioids | Neoendorphins | κ-Opioid receptor | – | |
| Opioids | Endorphins | μ-Opioid receptors | – | |
| Opioids | Endomorphins | μ-Opioid receptors | – | |
| Opioids | Morphine | μ-Opioid receptors | – | |
| Opioids | Nociceptin/orphanin FQ | N/OFQ | Nociceptin receptors | – |
| Orexins | Orexin A | OX-A | Orexin receptors | – |
| Orexins | Orexin B | OX-B | Orexin receptors | – |
| Parathyroid hormone family | Parathyroid hormone-related protein | PTHrP | – | – |
| RFamides | Kisspeptin | KiSS | GPR54 | – |
| RFamides | Neuropeptide FF | NPFF | NPFF1, NPFF2 | – |
| RFamides | Prolactin-releasing peptide | PrRP | PrRPR | – |
| RFamides | Pyroglutamylated RFamide peptide | QRFP | GPR103 | – |
| Secretins | Secretin | Secretin receptor | – | |
| Secretins | Motilin | Motilin receptor | – | |
| Secretins | Glucagon | Glucagon receptor | – | |
| Secretins | Glucagon-like peptide-1 | GLP-1 | Glucagon-like peptide 1 receptor | – |
| Secretins | Glucagon-like peptide-2 | GLP-2 | Glucagon-like peptide 2 receptor | – |
| Secretins | Vasoactive intestinal peptide | VIP | Vasoactive intestinal peptide receptors | – |
| Secretins | Growth hormone–releasing hormone | GHRH | Growth hormone–releasing hormone receptor | – |
| Secretins | Pituitary adenylate cyclase-activating peptide | PACAP | ADCYAP1R1 | – |
| Somatostatins | Somatostatin | Somatostatin receptors | – | |
| Tachykinins | Neurokinin A | – | – | |
| Tachykinins | Neurokinin B | – | – | |
| Tachykinins | Substance P | – | – | |
| Tachykinins | Neuropeptide K | – | – | |
| Other | Agouti-related peptide | AgRP | Melanocortin receptor – | |
| Other | N-Acetylaspartylglutamate | NAAG | Metabotropic glutamate receptor 3 (mGluR3) | – |
| Other | Cocaine- and amphetamine-regulated transcript | CART | Unknown Gi/Go-coupled receptor[31] | – |
| Other | Gonadotropin-releasing hormone | GnRH | GnRHR | – |
| Other | Thyrotropin-releasing hormone | TRH | TRHR | – |
| Other | Melanin-concentrating hormone | MCH | MCHR 1,2 | – |
| Category | Name | Abbreviation | Metabotropic | Ionotropic |
|---|---|---|---|---|
| Gaseous signaling molecule | Nitric oxide | NO | Soluble guanylyl cyclase | – |
| Gaseous signaling molecule | Carbon monoxide | CO | – | Heme bound to potassium channels |
| Gaseous signaling molecule | Hydrogen sulfide | H2S | – | – |
Brain neurotransmitter systems [edit]
Neurons expressing certain types of neurotransmitters sometimes form distinct systems, where activation of the system affects large volumes of the brain, called volume transmission. Major neurotransmitter systems include the noradrenaline (norepinephrine) system, the dopamine system, the serotonin system, and the cholinergic system, among others. Trace amines have a modulatory effect on neurotransmission in monoamine pathways (i.e., dopamine, norepinephrine, and serotonin pathways) throughout the brain via signaling through trace amine-associated receptor 1.[32][33] A brief comparison of these systems follows:
| System | Pathway origin and projections | Regulated cognitive processes and behaviors |
|---|---|---|
| Noradrenaline system [34][35][36][37][38][39] |
Noradrenergic pathways:
|
|
| Dopamine system [36][37][38][40][41][42] |
Dopaminergic pathways:
|
|
| Histamine system [37][38][43] |
Histaminergic pathways:
|
|
| Serotonin system [34][36][37][38][44][45][46] |
Serotonergic pathways:
Caudal nuclei (CN):
Rostral nuclei (RN):
|
|
| Acetylcholine system [34][36][37][38][47] |
Cholinergic pathways:
Forebrain cholinergic nuclei (FCN):
Striatal tonically active cholinergic neurons (TAN)
Brainstem cholinergic nuclei (BCN):
|
|
| Adrenaline system [48][49] |
Adrenergic pathways:
|
|
Drug effects[edit]
Understanding the effects of drugs on neurotransmitters comprises a significant portion of research initiatives in the field of neuroscience. Most neuroscientists involved in this field of research believe that such efforts may further advance our understanding of the circuits responsible for various neurological diseases and disorders, as well as ways to effectively treat and someday possibly prevent or cure such illnesses.[50][medical citation needed]
Drugs can influence behavior by altering neurotransmitter activity. For instance, drugs can decrease the rate of synthesis of neurotransmitters by affecting the synthetic enzyme(s) for that neurotransmitter. When neurotransmitter syntheses are blocked, the amount of neurotransmitters available for release becomes substantially lower, resulting in a decrease in neurotransmitter activity. Some drugs block or stimulate the release of specific neurotransmitters. Alternatively, drugs can prevent neurotransmitter storage in synaptic vesicles by causing the synaptic vesicle membranes to leak. Drugs that prevent a neurotransmitter from binding to its receptor are called receptor antagonists. For example, drugs used to treat patients with schizophrenia such as haloperidol, chlorpromazine, and clozapine are antagonists at receptors in the brain for dopamine. Other drugs act by binding to a receptor and mimicking the normal neurotransmitter. Such drugs are called receptor agonists. An example of a receptor agonist is morphine, an opiate that mimics effects of the endogenous neurotransmitter β-endorphin to relieve pain. Other drugs interfere with the deactivation of a neurotransmitter after it has been released, thereby prolonging the action of a neurotransmitter. This can be accomplished by blocking re-uptake or inhibiting degradative enzymes. Lastly, drugs can also prevent an action potential from occurring, blocking neuronal activity throughout the central and peripheral nervous system. Drugs such as tetrodotoxin that block neural activity are typically lethal.
Drugs targeting the neurotransmitter of major systems affect the whole system, which can explain the complexity of action of some drugs. Cocaine, for example, blocks the re-uptake of dopamine back into the presynaptic neuron, leaving the neurotransmitter molecules in the synaptic gap for an extended period of time. Since the dopamine remains in the synapse longer, the neurotransmitter continues to bind to the receptors on the postsynaptic neuron, eliciting a pleasurable emotional response. Physical addiction to cocaine may result from prolonged exposure to excess dopamine in the synapses, which leads to the downregulation of some post-synaptic receptors. After the effects of the drug wear off, an individual can become depressed due to decreased probability of the neurotransmitter binding to a receptor. Fluoxetine is a selective serotonin re-uptake inhibitor (SSRI), which blocks re-uptake of serotonin by the presynaptic cell which increases the amount of serotonin present at the synapse and furthermore allows it to remain there longer, providing potential for the effect of naturally released serotonin.[51] AMPT prevents the conversion of tyrosine to L-DOPA, the precursor to dopamine; reserpine prevents dopamine storage within vesicles; and deprenyl inhibits monoamine oxidase (MAO)-B and thus increases dopamine levels.
| Drug | Interacts with: | Receptor Interaction: | Type | Effects |
|---|---|---|---|---|
| Botulinum Toxin (Botox) | Acetylcholine | – | Antagonist | Blocks Acetylcholine release in PNS
Prevents muscle contractions |
| Black Widow Spider Venom | Acetylcholine | – | Agonist | Promotes acetylcholine release in PNS
Stimulates muscle contractions |
| Neostigmine | Acetylcholine | – | – | Interferes with acetylcholinerase activity
Increases effects of ACh at receptors Used to treat myasthenia gravis |
| Nicotine | Acetylcholine | Nicotinic (skeletal muscle) | Agonist | Increases ACh activity
Increases attention Reinforcing effects |
| d-tubocurarine | Acetylcholine | Nicotinic (skeletal muscle) | Antagonist | Decreases activity at receptor site |
| Curare | Acetylcholine | Nicotinic (skeletal muscle) | Antagonist | Decreases ACh activity
Prevents muscle contractions |
| Muscarine | Acetylcholine | Muscarinic (heart and smooth muscle) | Agonist | Increases ACh activity
Toxic |
| Atropine | Acetylcholine | Muscarinic (heart and smooth muscle) | Antagonist | Blocks pupil constriction
Blocks saliva production |
| Scopolamine (Hyoscine) | Acetylcholine | Muscarinic (heart and smooth muscle) | Antagonist | Treats motion sickness and postoperative nausea and vomiting |
| AMPT | Dopamine/norepinephrine | – | – | Inactivates tyrosine hydroxylase and inhibits dopamine production |
| Reserpine | Dopamine | – | – | Prevents storage of dopamine and other monoamines in synaptic vesicles
Causes sedation and depression |
| Apomorphine | Dopamine | D2 Receptor (presynaptic autoreceptors/postsynaptic receptors) | Antagonist (low dose)/Direct agonist (high dose) | Low dose: blocks autoreceptors
High dose: stimulates postsynaptic receptors |
| Amphetamine | Dopamine/norepinephrine | – | Indirect agonist | Releases dopamine, noradrenaline, and serotonin
Blocks reuptake[32][33] |
| Methamphetamine | Dopamine/norepinephrine | – | – | Releases dopamine and noradrenaline
Blocks reuptake |
| Methylphenidate | Dopamine | – | – | Blocks reuptake
Enhances attention and impulse control in ADHD |
| Cocaine | Dopamine | – | Indirect Agonist | Blocks reuptake into presynapse
Blocks voltage-dependent sodium channels Can be used as a topical anesthetic (eye drops) |
| Deprenyl | Dopamine | – | Agonist | Inhibits MAO-B
Prevents destruction of dopamine |
| Chlorpromazine | Dopamine | D2 Receptors | Antagonist | Blocks D2 receptors
Alleviates hallucinations |
| MPTP | Dopamine | – | – | Results in Parkinson like symptoms |
| PCPA | Serotonin (5-HT) | – | Antagonist | Disrupts serotonin synthesis by blocking the activity of tryptophan hydroxylase |
| Ondansetron | Serotonin (5-HT) | 5-HT3 receptors | Antagonist | Reduces side effects of chemotherapy and radiation
Reduces nausea and vomiting |
| Buspirone | Serotonin (5-HT) | 5-HT1A receptors | Partial Agonist | Treats symptoms of anxiety and depression |
| Fluoxetine | Serotonin (5-HT) | supports 5-HT reuptake | SSRI | Inhibits reuptake of serotonin
Treats depression, some anxiety disorders, and OCD[51] Common examples: Prozac and Sarafem |
| Fenfluramine | Serotonin (5-HT) | – | – | Causes release of serotonin
Inhibits reuptake of serotonin Used as an appetite suppressant |
| Lysergic acid diethylamide | Serotonin (5-HT) | Post-synaptic 5-HT2A receptors | Direct Agonist | Produces visual perception distortions
Stimulates 5-HT2A receptors in forebrain |
| Methylenedioxymethamphetamine (MDMA) | Serotonin (5-HT)/ norepinphrine | – | – | Stimulates release of serotonin and norepinephrine and inhibits the reuptake
Causes excitatory and hallucinogenic effects |
| Strychnine | Glycine | – | Antagonist | Causes severe muscle spasms[53] |
| Diphenhydramine | Histamine | Crosses blood brain barrier to cause drowsiness | ||
| Tetrahydrocannabinol (THC) | Endocannabinoids | Cannabinoid (CB) receptors | Agonist | Produces analgesia and sedation
Increases appetite Cognitive effects |
| Rimonabant | Endocannabinoids | Cannabinoid (CB) receptors | Antagonist | Suppresses appetite
Used in smoking cessation |
| MAFP | Endocannabinoids | – | – | Inhibits FAAH
Used in research to increase cannabinoid system activity |
| AM1172 | Endocannabinoids | – | – | Blocks cannabinoid reuptake
Used in research to increase cannabinoid system activity |
| Anandamide (endogenous) | – | Cannabinoid (CB) receptors; 5-HT3 receptors | – | Reduce nausea and vomiting |
| Caffeine | Adenosine | Adenosine receptors | Antagonist | Blocks adenosine receptors
Increases wakefulness |
| PCP | Glutamate | NMDA receptor | Indirect Antagonist | Blocks PCP binding site
Prevents calcium ions from entering neurons Impairs learning |
| AP5 | Glutamate | NMDA receptor | Antagonist | Blocks glutamate binding site on NMDA receptor
Impairs synaptic plasticity and certain forms of learning |
| Ketamine | Glutamate | NMDA receptor | Antagonist | Used as anesthesia
Induces trance-like state, helps with pain relief and sedation |
| NMDA | Glutamate | NMDA receptor | Agonist | Used in research to study NMDA receptor
Ionotropic receptor |
| AMPA | Glutamate | AMPA receptor | Agonist | Used in research to study AMPA receptor
Ionotropic receptor |
| Allyglycine | GABA | – | – | Inhibits GABA synthesis
Causes seizures |
| Muscimol | GABA | GABA receptor | Agonist | Causes sedation |
| Bicuculine | GABA | GABA receptor | Antagonist | Causes Seizures |
| Benzodiazepines | GABA | GABAA receptor | Indirect agonists | Anxiolytic, sedation, memory impairment, muscle relaxation |
| Barbiturates | GABA | GABAA receptor | Indirect agonists | Sedation, memory impairment, muscle relaxation |
| Alcohol | GABA | GABA receptor | Indirect agonist | Sedation, memory impairment, muscle relaxation |
| Picrotoxin | GABA | GABAA receptor | Indirect antagonist | High doses cause seizures |
| Tiagabine | GABA | – | Antagonist | GABA transporter antagonist
Increase availability of GABA Reduces the likelihood of seizures |
| Moclobemide | Norepinephrine | – | Agonist | Blocks MAO-A to treat depression |
| Idazoxan | Norepinephrine | alpha-2 adrenergic autoreceptors | Agonist | Blocks alpha-2 autoreceptors
Used to study norepinephrine system |
| Fusaric acid | Norepinephrine | – | – | Inhibits activity of dopamine beta-hydroxylase which blocks the production of norepinephrine
Used to study norepinephrine system without affecting dopamine system |
| Opiates (Opium, morphine, heroin, and oxycodone) | Opioids | Opioid receptor[54] | Agonists | Analgesia, sedation, and reinforcing effects |
| Naloxone | Opioids | – | Antagonist | Reverses opiate intoxication or overdose symptoms (i.e. problems with breathing) |
Agonists[edit]
|
This section needs expansion with: coverage of full agonists and their distinction from partial agonist and inverse agonist.. You can help by adding to it. (August 2015) |
An agonist is a chemical capable of binding to a receptor, such as a neurotransmitter receptor, and initiating the same reaction typically produced by the binding of the endogenous substance.[55] An agonist of a neurotransmitter will thus initiate the same receptor response as the transmitter. In neurons, an agonist drug may activate neurotransmitter receptors either directly or indirectly. Direct-binding agonists can be further characterized as full agonists, partial agonists, inverse agonists.[56][57]
Direct agonists act similar to a neurotransmitter by binding directly to its associated receptor site(s), which may be located on the presynaptic neuron or postsynaptic neuron, or both.[58] Typically, neurotransmitter receptors are located on the postsynaptic neuron, while neurotransmitter autoreceptors are located on the presynaptic neuron, as is the case for monoamine neurotransmitters;[32] in some cases, a neurotransmitter utilizes retrograde neurotransmission, a type of feedback signaling in neurons where the neurotransmitter is released postsynaptically and binds to target receptors located on the presynaptic neuron.[59][note 1] Nicotine, a compound found in tobacco, is a direct agonist of most nicotinic acetylcholine receptors, mainly located in cholinergic neurons.[54] Opiates, such as morphine, heroin, hydrocodone, oxycodone, codeine, and methadone, are μ-opioid receptor agonists; this action mediates their euphoriant and pain relieving properties.[54]
Indirect agonists increase the binding of neurotransmitters at their target receptors by stimulating the release or preventing the reuptake of neurotransmitters.[58] Some indirect agonists trigger neurotransmitter release and prevent neurotransmitter reuptake. Amphetamine, for example, is an indirect agonist of postsynaptic dopamine, norepinephrine, and serotonin receptors in each their respective neurons;[32][33] it produces both neurotransmitter release into the presynaptic neuron and subsequently the synaptic cleft and prevents their reuptake from the synaptic cleft by activating TAAR1, a presynaptic G protein-coupled receptor, and binding to a site on VMAT2, a type of monoamine transporter located on synaptic vesicles within monoamine neurons.[32][33]
Antagonists[edit]
An antagonist is a chemical that acts within the body to reduce the physiological activity of another chemical substance (as an opiate); especially one that opposes the action on the nervous system of a drug or a substance occurring naturally in the body by combining with and blocking its nervous receptor.[60]
There are two main types of antagonist: direct-acting Antagonist and indirect-acting Antagonists:
- Direct-acting antagonist- which takes up space present on receptors which are otherwise taken up by neurotransmitters themselves. This results in neurotransmitters being blocked from binding to the receptors. The most common is called Atropine.
- Indirect-acting antagonist- drugs that inhibit the release/production of neurotransmitters (e.g., Reserpine).
Drug antagonists[edit]
An antagonist drug is one that attaches (or binds) to a site called a receptor without activating that receptor to produce a biological response. It is therefore said to have no intrinsic activity. An antagonist may also be called a receptor «blocker» because they block the effect of an agonist at the site. The pharmacological effects of an antagonist, therefore, result in preventing the corresponding receptor site’s agonists (e.g., drugs, hormones, neurotransmitters) from binding to and activating it. Antagonists may be «competitive» or «irreversible».
A competitive antagonist competes with an agonist for binding to the receptor. As the concentration of antagonist increases, the binding of the agonist is progressively inhibited, resulting in a decrease in the physiological response. High concentration of an antagonist can completely inhibit the response. This inhibition can be reversed, however, by an increase of the concentration of the agonist, since the agonist and antagonist compete for binding to the receptor. Competitive antagonists, therefore, can be characterized as shifting the dose–response relationship for the agonist to the right. In the presence of a competitive antagonist, it takes an increased concentration of the agonist to produce the same response observed in the absence of the antagonist.
An irreversible antagonist binds so strongly to the receptor as to render the receptor unavailable for binding to the agonist. Irreversible antagonists may even form covalent chemical bonds with the receptor. In either case, if the concentration of the irreversible antagonist is high enough, the number of unbound receptors remaining for agonist binding may be so low that even high concentrations of the agonist do not produce the maximum biological response.[61]
Precursors[edit]
While intake of neurotransmitter precursors does increase neurotransmitter synthesis, evidence is mixed as to whether neurotransmitter release and postsynaptic receptor firing is increased. Even with increased neurotransmitter release, it is unclear whether this will result in a long-term increase in neurotransmitter signal strength, since the nervous system can adapt to changes such as increased neurotransmitter synthesis and may therefore maintain constant firing.[65][unreliable medical source?] Some neurotransmitters may have a role in depression and there is some evidence to suggest that intake of precursors of these neurotransmitters may be useful in the treatment of mild and moderate depression.[65][unreliable medical source?][66]
Catecholamine and trace amine precursors[edit]
L-DOPA, a precursor of dopamine that crosses the blood–brain barrier, is used in the treatment of Parkinson’s disease. For depressed patients where low activity of the neurotransmitter norepinephrine is implicated, there is only little evidence for benefit of neurotransmitter precursor administration. L-phenylalanine and L-tyrosine are both precursors for dopamine, norepinephrine, and epinephrine. These conversions require vitamin B6, vitamin C, and S-adenosylmethionine. A few studies suggest potential antidepressant effects of L-phenylalanine and L-tyrosine, but there is much room for further research in this area.[65][unreliable medical source?]
Serotonin precursors[edit]
Administration of L-tryptophan, a precursor for serotonin, is seen to double the production of serotonin in the brain. It is significantly more effective than a placebo in the treatment of mild and moderate depression.[65][unreliable medical source?] This conversion requires vitamin C.[21] 5-hydroxytryptophan (5-HTP), also a precursor for serotonin, is more effective than a placebo.[65][unreliable medical source?]
Diseases and disorders[edit]
Diseases and disorders may also affect specific neurotransmitter systems. The following are disorders involved in either an increase, decrease, or imbalance of certain neurotransmitters.
Dopamine:
For example, problems in producing dopamine (mainly in the substantia nigra) can result in Parkinson’s disease, a disorder that affects a person’s ability to move as they want to, resulting in stiffness, tremors or shaking, and other symptoms. Some studies suggest that having too little or too much dopamine or problems using dopamine in the thinking and feeling regions of the brain may play a role in disorders like schizophrenia or attention deficit hyperactivity disorder (ADHD). Dopamine is also involved in addiction and drug use, as most recreational drugs cause an influx of dopamine in the brain (especially opioid and methamphetamines) that produces a pleasurable feeling, which is why users constantly crave drugs.
Serotonin:
Similarly, after some research suggested that drugs that block the recycling, or reuptake, of serotonin seemed to help some people diagnosed with depression, it was theorized that people with depression might have lower-than-normal serotonin levels. Though widely popularized, this theory was not borne out in subsequent research.[67] Therefore, selective serotonin reuptake inhibitors (SSRIs) are used to increase the amounts of serotonin in synapses.
Glutamate:
Furthermore, problems with producing or using glutamate have been suggestively and tentatively linked to many mental disorders, including autism, obsessive–compulsive disorder (OCD), schizophrenia, and depression.[68] Having too much glutamate has been linked to neurological diseases such as Parkinson’s disease, multiple sclerosis, Alzheimer’s disease, stroke, and ALS (amyotrophic lateral sclerosis).[69]
CAPON Binds Nitric Oxide Synthase, Regulating NMDA Receptor–Mediated Glutamate Neurotransmission
Neurotransmitter imbalance[edit]
Generally, there are no scientifically established «norms» for appropriate levels or «balances» of different neurotransmitters. It is in most cases pragmatically impossible to even measure levels of neurotransmitters in a brain or body at any distinct moments in time. Neurotransmitters regulate each other’s release, and weak consistent imbalances in this mutual regulation were linked to temperament in healthy people.[70][71][72][73][74] Strong imbalances or disruptions to neurotransmitter systems have been associated with many diseases and mental disorders. These include Parkinson’s, depression, insomnia, Attention Deficit Hyperactivity Disorder (ADHD), anxiety, memory loss, dramatic changes in weight and addictions. Chronic physical or emotional stress can be a contributor to neurotransmitter system changes. Genetics also plays a role in neurotransmitter activities. Apart from recreational use, medications that directly and indirectly interact with one or more transmitter or its receptor are commonly prescribed for psychiatric and psychological issues. Notably, drugs interacting with serotonin and norepinephrine are prescribed to patients with problems such as depression and anxiety—though the notion that there is much solid medical evidence to support such interventions has been widely criticized.[75] Studies shown that dopamine imbalance has an influence on multiple sclerosis and other neurological disorders.[76]
See also[edit]
- BK channel#Cellular level
- Kiss-and-run fusion
- Natural neuroactive substance
- Neuroendocrine
- Neuroendocrinology
- Neuropsychopharmacology
- Neurotransmission
- Neurotransmitter analog
- Neurotransmitter release
- Neural pathway
- Neuromodulation
Notes[edit]
- ^ In the central nervous system, anandamide other endocannabinoids utilize retrograde neurotransmission, since their release is postsynaptic, while their target receptor, cannabinoid receptor 1 (CB1), is presynaptic.[59] The cannabis plant contains Δ9-tetrahydrocannabinol, which is a direct agonist at CB1.[59]
- ^ GABA is a non-proteinogenic amino acid
References[edit]
- ^ Lodish H, Berk A, Zipursky SL (2000). «Section 21.4 Neurotransmitters, Synapses, and Impulse Transmission». Molecular Cell Biology (4th ed.). New York: W. H. Freeman.
- ^ Cuevas J (1 January 2019). «Neurotransmitters and Their Life Cycle». Reference Module in Biomedical Sciences. Elsevier. doi:10.1016/b978-0-12-801238-3.11318-2. ISBN 978-0-12-801238-3.
- ^ Purves D, Augustine GJ, Fitzpatrick D, Katz LC, LaMantia AS, McNamara JO, Williams SM (2001). «Peptide Neurotransmitters». Neuroscience (2nd ed.).
- ^ Sanders KM, Ward SM (January 2019). «Nitric oxide and its role as a non-adrenergic, non-cholinergic inhibitory neurotransmitter in the gastrointestinal tract». British Journal of Pharmacology. 176 (2): 212–227. doi:10.1111/bph.14459. PMC 6295421. PMID 30063800.
- ^ Elias LJ, Saucier DM (2005). Neuropsychology: Clinical and Experimental Foundations. Boston: Pearson.
- ^ Chergui K, Suaud-Chagny MF, Gonon F (October 1994). «Nonlinear relationship between impulse flow, dopamine release and dopamine elimination in the rat brain in vivo». Neuroscience. 62 (3): 641–645. doi:10.1016/0306-4522(94)90465-0. PMID 7870295. S2CID 20465561.
- ^ Thapa S, Lv M, Xu H (30 November 2017). «Acetylcholinesterase: A Primary Target for Drugs and Insecticides». Mini Reviews in Medicinal Chemistry. 17 (17): 1665–1676. doi:10.2174/1389557517666170120153930. PMID 28117022.
- ^ Vasica G, Tennant CC (September 2002). «Cocaine use and cardiovascular complications». The Medical Journal of Australia. 177 (5): 260–262. doi:10.5694/j.1326-5377.2002.tb04761.x. PMID 12197823. S2CID 18572638.
- ^ Saladin, Kenneth S. Anatomy and Physiology: The Unity of Form and Function. McGraw Hill. 2009 ISBN 0-07-727620-5
- ^ Breedlove SM, Watson NV (2013). Biological psychology : an introduction to behavioral, cognitive, and clinical neuroscience (Seventh ed.). Sunderland, MA: Sinauer Associates. ISBN 978-0878939275.
- ^ a b Whishaw B, Kolb IQ (2014). An introduction to brain and behavior (4th ed.). New York, NY: Worth Publishers. pp. 150–151. ISBN 978-1429242288.
- ^ Peters A, Palay SL (December 1996). «The morphology of synapses». Journal of Neurocytology. 25 (12): 687–700. doi:10.1007/BF02284835. PMID 9023718. S2CID 29365393.
- ^ Shier D, Butler J, Lewis R (5 January 2015). Hole’s human anatomy & physiology (Fourteenth ed.). New York, NY. ISBN 978-0-07-802429-0. OCLC 881146319.
- ^ Di Chiara G, Morelli M, Consolo S (June 1994). «Modulatory functions of neurotransmitters in the striatum: ACh/dopamine/NMDA interactions». Trends in Neurosciences. 17 (6): 228–233. doi:10.1016/0166-2236(94)90005-1. PMID 7521083. S2CID 32085555.
- ^ Whishaw B, Kolb IQ (2014). An introduction to brain and behavior (4th ed.). New York, NY: Worth Publishers. ISBN 978-1429242288.
- ^ Gross L (November 2006). ««Supporting» players take the lead in protecting the overstimulated brain». PLOS Biology. 4 (11): e371. doi:10.1371/journal.pbio.0040371. PMC 1609133. PMID 20076484.
- ^ Yang JL, Sykora P, Wilson DM, Mattson MP, Bohr VA (August 2011). «The excitatory neurotransmitter glutamate stimulates DNA repair to increase neuronal resiliency». Mechanisms of Ageing and Development. 132 (8–9): 405–11. doi:10.1016/j.mad.2011.06.005. PMC 3367503. PMID 21729715.
- ^ Orexin receptor antagonists a new class of sleeping pill, National Sleep Foundation.
- ^ «Acetylcholine Receptors». Ebi.ac.uk. Retrieved 25 August 2014.
- ^ Schacter, Gilbert and Weger. Psychology.United States of America.2009.Print.
- ^ a b University of Bristol. «Introduction to Serotonin». Retrieved 15 October 2009.
- ^ Prasad BV (2020). Examining Biological Foundations of Human Behavior. United States of America: IGI Global. p. 81. ISBN 978-1799-8286-17.
- ^ a b Sapolsky R (2005). «Biology and Human Behavior: The Neurological Origins of Individuality, 2nd edition». The Teaching Company.
see pages 13 & 14 of Guide Book
- ^ Snyder SH, Innis RB (1979). «Peptide neurotransmitters». Annual Review of Biochemistry. 48: 755–82. doi:10.1146/annurev.bi.48.070179.003543. PMID 38738.
- ^ Corbière A, Vaudry H, Chan P, Walet-Balieu ML, Lecroq T, Lefebvre A, et al. (18 September 2019). «Strategies for the Identification of Bioactive Neuropeptides in Vertebrates». Frontiers in Neuroscience. 13: 948. doi:10.3389/fnins.2019.00948. PMC 6759750. PMID 31619945.
- ^ Fricker LD, Devi LA (May 2018). «Orphan neuropeptides and receptors: Novel therapeutic targets». Pharmacology & Therapeutics. 185: 26–33. doi:10.1016/j.pharmthera.2017.11.006. PMC 5899030. PMID 29174650.
- ^ Kodirov SA, Takizawa S, Joseph J, Kandel ER, Shumyatsky GP, Bolshakov VY (October 2006). «Synaptically released zinc gates long-term potentiation in fear conditioning pathways». Proceedings of the National Academy of Sciences of the United States of America. 103 (41): 15218–23. Bibcode:2006PNAS..10315218K. doi:10.1073/pnas.0607131103. PMC 1622803. PMID 17005717.
- ^ «International Symposium on Nitric Oxide – Dr. John Andrews – MaRS». MaRS. Archived from the original on 14 October 2014.
- ^ «Dopamine: Biological activity». IUPHAR/BPS guide to pharmacology. International Union of Basic and Clinical Pharmacology. Retrieved 29 January 2016.
- ^ Grandy DK, Miller GM, Li JX (February 2016). ««TAARgeting Addiction»—The Alamo Bears Witness to Another Revolution: An Overview of the Plenary Symposium of the 2015 Behavior, Biology and Chemistry Conference». Drug and Alcohol Dependence. 159: 9–16. doi:10.1016/j.drugalcdep.2015.11.014. PMC 4724540. PMID 26644139.
TAAR1 is a high-affinity receptor for METH/AMPH and DA
- ^ Lin Y, Hall RA, Kuhar MJ (October 2011). «CART peptide stimulation of G protein-mediated signaling in differentiated PC12 cells: identification of PACAP 6-38 as a CART receptor antagonist». Neuropeptides. 45 (5): 351–8. doi:10.1016/j.npep.2011.07.006. PMC 3170513. PMID 21855138.
- ^ a b c d e Miller GM (January 2011). «The emerging role of trace amine-associated receptor 1 in the functional regulation of monoamine transporters and dopaminergic activity». Journal of Neurochemistry. 116 (2): 164–76. doi:10.1111/j.1471-4159.2010.07109.x. PMC 3005101. PMID 21073468.
- ^ a b c d Eiden LE, Weihe E (January 2011). «VMAT2: a dynamic regulator of brain monoaminergic neuronal function interacting with drugs of abuse». Annals of the New York Academy of Sciences. 1216 (1): 86–98. Bibcode:2011NYASA1216…86E. doi:10.1111/j.1749-6632.2010.05906.x. PMC 4183197. PMID 21272013.
VMAT2 is the CNS vesicular transporter for not only the biogenic amines DA, NE, EPI, 5-HT, and HIS, but likely also for the trace amines TYR, PEA, and thyronamine (THYR) … [Trace aminergic] neurons in mammalian CNS would be identifiable as neurons expressing VMAT2 for storage, and the biosynthetic enzyme aromatic amino acid decarboxylase (AADC).
- ^ a b c Malenka RC, Nestler EJ, Hyman SE (2009). «Chapter 6: Widely Projecting Systems: Monoamines, Acetylcholine, and Orexin». In Sydor A, Brown RY (eds.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York: McGraw-Hill Medical. p. 155. ISBN 9780071481274.
Different subregions of the VTA receive glutamatergic inputs from the prefrontal cortex, orexinergic inputs from the lateral hypothalamus, cholinergic and also glutamatergic and GABAergic inputs from the laterodorsal tegmental nucleus and pedunculopontine nucleus, noradrenergic inputs from the locus ceruleus, serotonergic inputs from the raphe nuclei, and GABAergic inputs from the nucleus accumbens and ventral pallidum.
- ^ Malenka RC, Nestler EJ, Hyman SE (2009). «Chapter 6: Widely Projecting Systems: Monoamines, Acetylcholine, and Orexin». In Sydor A, Brown RY (eds.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York: McGraw-Hill Medical. pp. 145, 156–157. ISBN 9780071481274.
Descending NE fibers modulate afferent pain signals. … The locus ceruleus (LC), which is located on the floor of the fourth ventricle in the rostral pons, contains more than 50% of all noradrenergic neurons in the brain; it innervates both the forebrain (eg, it provides virtually all the NE to the cerebral cortex) and regions of the brainstem and spinal cord. … The other noradrenergic neurons in the brain occur in loose collections of cells in the brainstem, including the lateral tegmental regions. These neurons project largely within the brainstem and spinal cord. NE, along with 5HT, ACh, histamine, and orexin, is a critical regulator of the sleep-wake cycle and of levels of arousal. … LC firing may also increase anxiety …Stimulation of β-adrenergic receptors in the amygdala results in enhanced memory for stimuli encoded under strong negative emotion … Epinephrine occurs in only a small number of central neurons, all located in the medulla. Epinephrine is involved in visceral functions, such as control of respiration.
- ^ a b c d Rang HP (2003). Pharmacology. Edinburgh: Churchill Livingstone. pp. 474 for noradrenaline system, page 476 for dopamine system, page 480 for serotonin system and page 483 for cholinergic system. ISBN 978-0-443-07145-4.
- ^ a b c d e Iwańczuk W, Guźniczak P (2015). «Neurophysiological foundations of sleep, arousal, awareness and consciousness phenomena. Part 1». Anaesthesiology Intensive Therapy. 47 (2): 162–7. doi:10.5603/AIT.2015.0015. PMID 25940332.
The ascending reticular activating system (ARAS) is responsible for a sustained wakefulness state. … The thalamic projection is dominated by cholinergic neurons originating from the pedunculopontine tegmental nucleus of pons and midbrain (PPT) and laterodorsal tegmental nucleus of pons and midbrain (LDT) nuclei [17, 18]. The hypothalamic projection involves noradrenergic neurons of the locus coeruleus (LC) and serotoninergic neurons of the dorsal and median raphe nuclei (DR), which pass through the lateral hypothalamus and reach axons of the histaminergic tubero-mamillary nucleus (TMN), together forming a pathway extending into the forebrain, cortex and hippocampus. Cortical arousal also takes advantage of dopaminergic neurons of the substantia nigra (SN), ventral tegmenti area (VTA) and the periaqueductal grey area (PAG). Fewer cholinergic neurons of the pons and midbrain send projections to the forebrain along the ventral pathway, bypassing the thalamus [19, 20].
- ^ a b c d e Malenka RC, Nestler EJ, Hyman SE (2009). «Chapter 12: Sleep and Arousal». In Sydor A, Brown RY (eds.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York, USA: McGraw-Hill Medical. p. 295. ISBN 9780071481274.
The ARAS is a complex structure consisting of several different circuits including the four monoaminergic pathways … The norepinephrine pathway originates from the locus ceruleus (LC) and related brainstem nuclei; the serotonergic neurons originate from the raphe nuclei within the brainstem as well; the dopaminergic neurons originate in ventral tegmental area (VTA); and the histaminergic pathway originates from neurons in the tuberomammillary nucleus (TMN) of the posterior hypothalamus. As discussed in Chapter 6, these neurons project widely throughout the brain from restricted collections of cell bodies. Norepinephrine, serotonin, dopamine, and histamine have complex modulatory functions and, in general, promote wakefulness. The PT in the brain stem is also an important component of the ARAS. Activity of PT cholinergic neurons (REM-on cells) promotes REM sleep. During waking, REM-on cells are inhibited by a subset of ARAS norepinephrine and serotonin neurons called REM-off cells.
- ^ Rinaman L (February 2011). «Hindbrain noradrenergic A2 neurons: diverse roles in autonomic, endocrine, cognitive, and behavioral functions». American Journal of Physiology. Regulatory, Integrative and Comparative Physiology. 300 (2): R222-35. doi:10.1152/ajpregu.00556.2010. PMC 3043801. PMID 20962208.
- ^ Malenka RC, Nestler EJ, Hyman SE (2009). «Chapter 6: Widely Projecting Systems: Monoamines, Acetylcholine, and Orexin». In Sydor A, Brown RY (eds.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York: McGraw-Hill Medical. pp. 147–148, 154–157. ISBN 9780071481274.
Neurons from the SNc densely innervate the dorsal striatum where they play a critical role in the learning and execution of motor programs. Neurons from the VTA innervate the ventral striatum (nucleus accumbens), olfactory bulb, amygdala, hippocampus, orbital and medial prefrontal cortex, and cingulate cortex. VTA DA neurons play a critical role in motivation, reward-related behavior, attention, and multiple forms of memory. … Thus, acting in diverse terminal fields, dopamine confers motivational salience («wanting») on the reward itself or associated cues (nucleus accumbens shell region), updates the value placed on different goals in light of this new experience (orbital prefrontal cortex), helps consolidate multiple forms of memory (amygdala and hippocampus), and encodes new motor programs that will facilitate obtaining this reward in the future (nucleus accumbens core region and dorsal striatum). … DA has multiple actions in the prefrontal cortex. It promotes the «cognitive control» of behavior: the selection and successful monitoring of behavior to facilitate attainment of chosen goals. Aspects of cognitive control in which DA plays a role include working memory, the ability to hold information «on line» in order to guide actions, suppression of prepotent behaviors that compete with goal-directed actions, and control of attention and thus the ability to overcome distractions. … Noradrenergic projections from the LC thus interact with dopaminergic projections from the VTA to regulate cognitive control. …
- ^ Calipari ES, Bagot RC, Purushothaman I, Davidson TJ, Yorgason JT, Peña CJ, et al. (March 2016). «In vivo imaging identifies temporal signature of D1 and D2 medium spiny neurons in cocaine reward». Proceedings of the National Academy of Sciences of the United States of America. 113 (10): 2726–31. Bibcode:2016PNAS..113.2726C. doi:10.1073/pnas.1521238113. PMC 4791010. PMID 26831103.
Previous work has demonstrated that optogenetically stimulating D1 MSNs promotes reward, whereas stimulating D2 MSNs produces aversion.
- ^ Ikemoto S (November 2010). «Brain reward circuitry beyond the mesolimbic dopamine system: a neurobiological theory». Neuroscience and Biobehavioral Reviews. 35 (2): 129–50. doi:10.1016/j.neubiorev.2010.02.001. PMC 2894302. PMID 20149820.
Recent studies on intracranial self-administration of neurochemicals (drugs) found that rats learn to self-administer various drugs into the mesolimbic dopamine structures–the posterior ventral tegmental area, medial shell nucleus accumbens and medial olfactory tubercle. … In the 1970s it was recognized that the olfactory tubercle contains a striatal component, which is filled with GABAergic medium spiny neurons receiving glutamatergic inputs form cortical regions and dopaminergic inputs from the VTA and projecting to the ventral pallidum just like the nucleus accumbens
Figure 3: The ventral striatum and self-administration of amphetamine - ^ Malenka RC, Nestler EJ, Hyman SE (2009). «Chapter 6: Widely Projecting Systems: Monoamines, Acetylcholine, and Orexin». In Sydor A, Brown RY (eds.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York: McGraw-Hill Medical. pp. 175–176. ISBN 9780071481274.
Within the brain, histamine is synthesized exclusively by neurons with their cell bodies in the tuberomammillary nucleus (TMN) that lies within the posterior hypothalamus. There are approximately 64000 histaminergic neurons per side in humans. These cells project throughout the brain and spinal cord. Areas that receive especially dense projections include the cerebral cortex, hippocampus, neostriatum, nucleus accumbens, amygdala, and hypothalamus. … While the best characterized function of the histamine system in the brain is regulation of sleep and arousal, histamine is also involved in learning and memory …It also appears that histamine is involved in the regulation of feeding and energy balance.
- ^ Malenka RC, Nestler EJ, Hyman SE (2009). «Chapter 6: Widely Projecting Systems: Monoamines, Acetylcholine, and Orexin». In Sydor A, Brown RY (eds.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York: McGraw-Hill Medical. pp. 158–160. ISBN 9780071481274.
[The] dorsal raphe preferentially innervates the cerebral cortex, thalamus, striatal regions (caudate-putamen and nucleus accumbens), and dopaminergic nuclei of the midbrain (eg, the substantia nigra and ventral tegmental area), while the median raphe innervates the hippocampus, septum, and other structures of the limbic forebrain. … it is clear that 5HT influences sleep, arousal, attention, processing of sensory information in the cerebral cortex, and important aspects of emotion (likely including aggression) and mood regulation. …The rostral nuclei, which include the nucleus linearis, dorsal raphe, medial raphe, and raphe pontis, innervate most of the brain, including the cerebellum. The caudal nuclei, which comprise the raphe magnus, raphe pallidus, and raphe obscuris, have more limited projections that terminate in the cerebellum, brainstem, and spinal cord.
- ^ Nestler EJ. «Brain Reward Pathways». Icahn School of Medicine at Mount Sinai. Nestler Lab. Retrieved 16 August 2014.
The dorsal raphe is the primary site of serotonergic neurons in the brain, which, like noradrenergic neurons, pervasively modulate brain function to regulate the state of activation and mood of the organism.
- ^ Marston OJ, Garfield AS, Heisler LK (June 2011). «Role of central serotonin and melanocortin systems in the control of energy balance». European Journal of Pharmacology. 660 (1): 70–9. doi:10.1016/j.ejphar.2010.12.024. PMID 21216242.
- ^ Malenka RC, Nestler EJ, Hyman SE (2009). «Chapter 6: Widely Projecting Systems: Monoamines, Acetylcholine, and Orexin». In Sydor A, Brown RY (eds.). Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York: McGraw-Hill Medical. pp. 167–175. ISBN 9780071481274.
The basal forebrain cholinergic nuclei are comprised the medial septal nucleus (Ch1), the vertical nucleus of the diagonal band (Ch2), the horizontal limb of the diagonal band (Ch3), and the nucleus basalis of Meynert (Ch4). Brainstem cholinergic nuclei include the pedunculopontine nucleus (Ch5), the laterodorsal tegmental nucleus (Ch6), the medial habenula (Ch7), and the parabigeminal nucleus (Ch8).
- ^ Guyenet PG, Stornetta RL, Bochorishvili G, Depuy SD, Burke PG, Abbott SB (August 2013). «C1 neurons: the body’s EMTs». American Journal of Physiology. Regulatory, Integrative and Comparative Physiology. 305 (3): R187-204. doi:10.1152/ajpregu.00054.2013. PMC 3743001. PMID 23697799.
- ^ Stornetta RL, Guyenet PG (March 2018). «C1 neurons: a nodal point for stress?». Experimental Physiology. 103 (3): 332–336. doi:10.1113/EP086435. PMC 5832554. PMID 29080216.
- ^ «Neuron Conversations: How Brain Cells Communicate». Brainfacts.org. Retrieved 2 December 2014.
- ^ a b Yadav VK, Ryu JH, Suda N, Tanaka KF, Gingrich JA, Schütz G, et al. (November 2008). «Lrp5 controls bone formation by inhibiting serotonin synthesis in the duodenum». Cell. 135 (5): 825–37. doi:10.1016/j.cell.2008.09.059. PMC 2614332. PMID 19041748.
- ^ Carlson, N. R., & Birkett, M. A. (2017). Physiology of Behavior (12th ed.). Pearson, pgs. 100–115. ISBN 978-0134080918
- ^ «CDC Strychnine | Facts about Strychnine | Public Health Emergency Preparedness& Response». emergency.cdc.gov. Retrieved 7 May 2018.
- ^ a b c «Neurotransmitters and Drugs Chart». Ocw.mit.edu. Retrieved 25 August 2014.
- ^ «Agonist – Definition and More from the Free Merriam-Webster Dictionary». Merriam-webster.com. Retrieved 25 August 2014.
- ^ Atack J., Lavreysen H. (2010) Agonist. In: Stolerman I.P. (eds) Encyclopedia of Psychopharmacology. Springer, Berlin, Heidelberg. https://doi.org/10.1007/978-3-540-68706-1_1565
- ^ Roth BL (February 2016). «DREADDs for Neuroscientists». Neuron. 89 (4): 683–94. doi:10.1016/j.neuron.2016.01.040. PMC 4759656. PMID 26889809.
- ^ a b Ries RK, Fiellin DA, Miller SC (2009). Principles of addiction medicine (4th ed.). Philadelphia: Wolters Kluwer/Lippincott Williams & Wilkins. pp. 709–710. ISBN 9780781774772. Retrieved 16 August 2015.
- ^ a b c Flores A, Maldonado R, Berrendero F (December 2013). «Cannabinoid-hypocretin cross-talk in the central nervous system: what we know so far». Frontiers in Neuroscience. 7: 256. doi:10.3389/fnins.2013.00256. PMC 3868890. PMID 24391536.
• Figure 1: Schematic of brain CB1 expression and orexinergic neurons expressing OX1 or OX2
• Figure 2: Synaptic signaling mechanisms in cannabinoid and orexin systems - ^ «Antagonist». Medical definition of Antagonist. Retrieved 5 November 2014.
- ^ Goeders NE (2001). «Antagonist». Encyclopedia of Drugs, Alcohol, and Addictive Behavior. Retrieved 2 December 2014.
- ^ Broadley KJ (March 2010). «The vascular effects of trace amines and amphetamines». Pharmacology & Therapeutics. 125 (3): 363–375. doi:10.1016/j.pharmthera.2009.11.005. PMID 19948186.
- ^ Lindemann L, Hoener MC (May 2005). «A renaissance in trace amines inspired by a novel GPCR family». Trends in Pharmacological Sciences. 26 (5): 274–281. doi:10.1016/j.tips.2005.03.007. PMID 15860375.
- ^ Wang X, Li J, Dong G, Yue J (February 2014). «The endogenous substrates of brain CYP2D». European Journal of Pharmacology. 724: 211–218. doi:10.1016/j.ejphar.2013.12.025. PMID 24374199.
- ^ a b c d e Meyers S (February 2000). «Use of neurotransmitter precursors for treatment of depression» (PDF). Alternative Medicine Review. 5 (1): 64–71. PMID 10696120. Archived from the original (PDF) on 5 August 2004.
- ^ van Praag HM (March 1981). «Management of depression with serotonin precursors». Biological Psychiatry. 16 (3): 291–310. PMID 6164407.
- ^ Healy D (April 2015). «Serotonin and depression». BMJ. 350: h1771. doi:10.1136/bmj.h1771. PMID 25900074. S2CID 38726584.
- ^ «NIMH Brain Basics». U.S. National Institutes of Health. Archived from the original on 29 October 2014. Retrieved 29 October 2014.
- ^ Bittigau P, Ikonomidou C (November 1997). «Glutamate in neurologic diseases». Journal of Child Neurology. 12 (8): 471–85. doi:10.1177/088307389701200802. PMID 9430311. S2CID 1258390.
- ^ Netter, P. (1991) Biochemical variables in the study of temperament. In Strelau, J. & Angleitner, A. (Eds.), Explorations in temperament: International perspectives on theory and measurement 147–161. New York: Plenum Press.
- ^ Trofimova I, Robbins TW (May 2016). «Temperament and arousal systems: A new synthesis of differential psychology and functional neurochemistry». Neuroscience and Biobehavioral Reviews. 64: 382–402. doi:10.1016/j.neubiorev.2016.03.008. hdl:11375/26202. PMID 26969100. S2CID 13937324.
- ^ Cloninger CR, Svrakic DM, Przybeck TR. A psychobiological model of temperament and character» Arch Gen Psychiatry 1993; 50:975-990.
- ^ Trofimova IN (2016). «The interlocking between functional aspects of activities and a neurochemical model of adult temperament.». In Arnold MC (ed.). Temperaments: Individual Differences, Social and Environmental Influences and Impact on Quality of Life. New York: Nova Science Publishers, Inc. pp. 77–147.
- ^ Depue RA, Morrone-Strupinsky JV (June 2005). «A neurobehavioral model of affiliative bonding: implications for conceptualizing a human trait of affiliation». The Behavioral and Brain Sciences. 28 (3): 313–50, discussion 350–95. doi:10.1017/s0140525x05000063. PMID 16209725.
- ^ Leo, J., & Lacasse, J. (10 October 2007). The Media and the Chemical Imbalance Theory of Depression. Retrieved 1 December 2014, from http://psychrights.org/articles/TheMediaandChemicalImbalanceTheoryofDepression.pdf
- ^ Dobryakova E, Genova HM, DeLuca J, Wylie GR (12 March 2015). «The dopamine imbalance hypothesis of fatigue in multiple sclerosis and other neurological disorders». Frontiers in Neurology. 6: 52. doi:10.3389/fneur.2015.00052. PMC 4357260. PMID 25814977.
External links[edit]
- Purves, Dale; Augustine, George J.; Fitzpatrick, David; Katz, Lawrence C.; LaMantia, Anthony-Samuel; McNamara, James O.; Williams, S. Mark (2001). «Chapter 6. Neurotransmitters». What Defines a Neurotransmitter?. Neuroscience (2nd ed.). Sunderland (MA): Sinauer Associates. ISBN 0-87893-742-0.
- Holz, Ronald W.; Fisher, Stephen K. (1999). «Chapter 10. Synaptic Transmission and Cellular Signaling: An Overview». In Siegel, George J; Agranoff, Bernard W; Albers, R Wayne; Fisher, Stephen K; Uhler, Michael D (eds.). Synaptic Transmission. Basic Neurochemistry: Molecular, Cellular and Medical Aspects (6th ed.). Philadelphia: Lippincott-Raven. ISBN 0-397-51820-X.
- Neurotransmitters and Neuroactive Peptides at Neuroscience for Kids website
Нейромедиаторы – это биологически активные химические вещества, посредством которых осуществляется передача электрического импульса от нервной клетки
Катехоламины влияют на важнейшие процессы в человеческом организме: уровень настроения, активность и работоспособность, скорость мышления, способность запоминать информацию и воспроизводить её, уровень агрессии и сексуальное поведение. Они адаптируют организм к стрессу: симпатоадреналовая система активизируется уже при подготовке к физической нагрузке и помогает легче перенести сдвиги внутренней среды.
Уровень катехоламинов наиболее высок у детей, поэтому у них нет проблем с активностью, запоминанием, быстрым переключением с одного занятия на другое, и настроение чаще всего хорошее. С возрастом синтез этих веществ замедляется, и чем старше становится человек, тем хуже у него настроение, ниже работоспособность и выше предрасположенность к депрессии.
Нарушения синтеза катехоламинов и их восприятия организмом ведут к серьёзным проблемам со здоровьем: артериальной гипертензии, тяжёлым депрессивным состояниям, в пожилом возрасте – к болезни Паркинсона. Нарушениями функционирования симпатоадреналовой системы объясняются развитие шизофрении и тяга к одурманивающим веществам – алкоголю, табаку, наркотикам.
Катехоламины взаимодействуют с особыми рецепторами на клеточной поверхности, которые называют адренорецепторами и делят на два вида: α- и β-адренорецепторы. Стимуляция α-адренорецепторов вызывает сужение сосудов, селезенки, расширение зрачков и т.д. Возбуждение β-адренорецепторов вызывает расширение сосудов, расслабление бронхов, учащение сердечных сокращений и т.д.
Адреналин:
Гормон, синтезирующийся хромаффинными клетками мозгового вещества надпочечников. Действие адреналина связано с влиянием на α- и β-адренорецепторы и во многом совпадает с эффектами возбуждения симпатических нервных волокон.
Действие адреналина увеличивает частоту сердечных сокращений, увеличивает артериальное давление, уменьшает отток крови к внутренним органам, увеличивает приток крови к скелетным мышцам, увеличивает уровень глюкозы в крови, заставляет печень и клетки мышц расщеплять гликоген и вырабатывать глюкозу и др.
Адреналин оказывает стимулирующее воздействие на ЦНС, хотя и слабо проникает через гематоэнцефалический барьер. Он повышает уровень бодрствования, психическую энергию и активность, вызывает психическую мобилизацию, реакцию ориентировки и ощущение тревоги, беспокойства или напряжения, генерируется при сильном волнении или большой физической нагрузке. Его называют “гормоном страха”.
Адреналин также оказывает выраженное противоаллергическое и противовоспалительное действие, тормозит высвобождение гистамина, серотонина, кининов и других медиаторов аллергии и воспаления из тучных клеток, понижает чувствительность тканей к этим веществам.
Адреналин вызывает повышение числа лейкоцитов в крови.
Также адреналин вызывает повышение числа и функциональной активности тромбоцитов, что, наряду со спазмом мелких капилляров, обуславливает гемостатическое (кровоостанавливающее) действие адреналина.
Норадреналин:
Представляет собой катехоламин, который продуцируют преимущественно постганглионарные клетки симпатической нервной системы и в меньшей степени — клетки мозгового слоя надпочечников, медиатор вегетативной нервной системы, действующий непосредственно в области пресинаптического окончания. Относится к числу наиболее важных нейромедиаторов мозга. Является предшественником адреналина. Также известен как “гормон ярости”.
Норадреналин является медиатором как голубоватого пятна ствола мозга, так и окончаний симпатической нервной системы. Количество норадренергических нейронов в ЦНС невелико (несколько тысяч), но у них весьма широкое поле иннервации в головном мозге.
Действие норадреналина связано с преимущественным влиянием на α-адренорецепторы. Норадреналин отличается от адреналина гораздо более сильным сосудосуживающим и прессорным действием, значительно меньшим стимулирующим влиянием на сокращения сердца, слабым действием на гладкую мускулатуру бронхов и кишечника, слабым влиянием на обмен веществ. Норадреналин в меньшей степени повышает потребность миокарда и других тканей в кислороде, чем адреналин.
Норадреналин принимает участие в регуляции артериального давления и периферического сосудистого сопротивления. Кардиотропное действие норадреналина связано с его стимулирующим влиянием на β-адренорецепторы сердца.
Дофамин:
Нейромедиатор, синтезирующийся в хромаффинных клетках специфических структур головного мозга, а также гормон, вырабатываемый мозговым веществом надпочечников и другими тканями (например, почками). Дофамин является предшественником норадреналина и адреналина в их биосинтезе.
Дофамин является одним из химических факторов внутреннего подкрепления (ФВП). Он выделяется при получении удовольствия и даже на стадии предвкушения. Как и у большинства таких факторов, у дофамина существуют наркотические аналоги, например, амфетамин, экстази, эфедрин.
В экстрапирамидной системе дофамин играет роль стимулирующего нейромедиатора, способствующего повышению двигательной активности, уменьшению двигательной заторможенности и скованности, снижению гипертонуса мышц. Физиологическими антагонистами дофамина в экстрапирамидной системе являются ацетилхолин и ГАМК. В гипоталамусе и гипофизе дофамин играет роль естественного тормозного нейромедиатора, угнетающего секрецию ряда гормонов.
Дофамин вызывает повышение сопротивления периферических сосудов. Он повышает систолическое артериальное давление. Также дофамин увеличивает силу сердечных сокращений. Увеличивается сердечный выброс. Частота сердечных сокращений увеличивается, но не так сильно, как под влиянием адреналина. Потребность миокарда в кислороде под влиянием дофамина повышается.
Дофамин уменьшает сопротивление почечных сосудов, увеличивает в них кровоток и почечную фильтрацию. Однако в больших концентрациях может вызывать сужение почечных сосудов. Также снижает скорость синтеза альдостерона в коре надпочечников, понижает секрецию ренина почками, повышает секрецию простагландинов тканью почек.
Дофамин тормозит перистальтику (волнообразное сокращение мышц) желудка и кишечника. В ЦНС дофамин стимулирует хеморецепторы триггерной зоны и рвотного центра и тем самым принимает участие в осуществлении акта рвоты.
Индоламины.
Серотонин:
5-гидрокситриптамин, 5-НТ — важный нейромедиатор и гормон. По химическому строению серотонин относится к биогенным аминам, классу триптаминов.
Серотонин играет роль нейромедиатора в ЦНС. Серотонинергические нейроны группируются в стволе мозга: в варолиевом мосту и ядрах шва. От моста идут нисходящие проекции в спинной мозг, нейроны ядер шва дают восходящие проекции к мозжечку, лимбической системе, базальным ганглиям, коре. Серотонин наряду с дофамином играет важную роль в механизмах регуляции гормональной функции гипофиза. Стимуляция серотонинергических путей, связывающих гипоталамус с гипофизом, вызывает увеличение секреции пролактина и некоторых других гормонов передней доли гипофиза. Серотонин участвует в регуляции сосудистого тонуса.
Серотонин влияет на мышечный тонус человека, быстроту реакции и настроение. Низкий уровень серотонина может привести к депрессии. Также от серотонина зависят болевые ощущения – если его уровень низок, даже лёгкий ушиб будет болезненным.
Серотонин играет важную роль в процессах свёртывания крови. Серотонин повышает функциональную активность тромбоцитов и их склонность к агрегации и образованию тромбов.
Серотонин участвует в процессах аллергии и воспаления. Он повышает проницаемость сосудов, усиливает хемотаксис и миграцию лейкоцитов в очаг воспаления, увеличивает содержание эозинофилов в крови, усиливает дегрануляцию тучных клеток и высвобождение других медиаторов аллергии и воспаления. Серотонин наряду с гистамином и простагландинами, раздражая рецепторы в тканях, играет роль в возникновении болевой импульсации из места повреждения или воспаления.
Также большое количество серотонина производится в кишечнике. Серотонин играет важную роль в регуляции моторики и секреции в желудочно-кишечном тракте, усиливая его перистальтику и секреторную активность.
Большое значение в диагностике уровня экскреции катехоламинов и серотонина играют их продукты метаболизма.
Продукты метаболизма катехоламинов и серотонина.
-Метанефрин, норметанефрин – и промежуточные метаболиты адреналина и норадреналина.
-Ванилилминдальная кислота (VМА)- основной метаболит адреналина и норадреналина.
-Гомованилиновая кислота (НVА)- основной метаболит дофамина.
-5-гидроксииндолуксусная кислота (5-НIАА)- основной метаболит серотонина.
Метаболиты отсрочено отображают факт повышения выработки катехоламинов, их повышенного метаболизма. Определяются в суточной моче.
Диагностическое значение определения уровня эндогенных катехоламинов, серотонина и их метаболитов.
Онкология.
n Феохромоцитома
Феохромоцитома: гормонально-активная опухоль (чаще доброкачественная, реже злокачественная) мозгового слоя надпочечников или хромафинной ткани вне надпочечников (параганглиома, ганглионеврома, нейробластома). В 75 % случаев феохромоцитома располагается в одном из надпочечников, чаще — в правом. В 10% случаев опухоль удается обнаружить в обоих надпочечниках. Остальные 15% опухолей располагаются вне надпочечников. В 10-20% случаев при исследовании опухоли можно выявить гистологические признаки злокачественного роста.
Как правило, феохромоцитома секретирует как адреналин, так и норадреналин, но преимущественно норадреналин. Некоторые опухоли секретируют только норадреналин или (реже) только адреналин. Очень редко преобладающим катехоламином является дофамин. Кроме катехоламинов феохромоцитома может продуцировать серотонин, АКТГ, соматостатин, опиоидные пептиды, кальцитонин, нейропептид Y (сильный вазоконстриктор) и др.
Клинические проявления.
Жалобы: головная боль, сердцебиение, раздражительность, потеря веса, боль в груди или в животе, тошнота, рвота, слабость и утомляемость.
Объективные признаки:
Изменения артериального давления (у 98% больных), стойкая артериальная гипертония, гипертонические кризы (могут сменяться артериальной гипотонией), ортостатическая гипотония, повышение артериального давления после незначительной физической нагрузки (например, после еды или дефекации) или физикального исследования (например, после пальпации живота), парадоксальное повышение артериального давления в ответ на некоторые гипотензивные средства, резкое повышение артериального давления при общей анестезии.
Другие признаки избытка катехоламинов: Потливость, тахикардия, аритмия, рефлекторная брадикардия, усиленный верхушечный толчок, бледность кожи лица и туловища, возбуждение, тревога, страх, гипертоническая ретинопатия, расширенные зрачки. Очень редко — экзофтальм, слезотечение, бледность или гиперемия склер (покраснение глаз), отсутствие реакции зрачка на свет, тремор, синдром Рейно или мраморность кожи; у детей иногда отек и цианоз кистей; влажная, холодная, липкая и бледная кожа рук и ног; «гусиная кожа», цианоз ногтевых лож.
Осложнения феохромоцитомы:
-Инфаркт миокарда
-Сердечная недостаточность
-Аритмия
-Тахикардия
-Падение артериального давления или остановка кровообращения во время введения в общую анестезию
-Шок
-Нарушение мозгового кровообращения
-Почечная недостаточность
-Гипертоническая энцефалопатия
-Ишемический колит
-Расслаивающая аневризма аорты
-У беременных: лихорадка, эклампсия, шок, смерть матери или плода
-и др.
У больных с феохромоцитомой концентрация катехоламинов в крови увеличивается в 10-100раз.
При этом:
-Феохромоцитомы надпочечникового происхождения: рост уровня и адреналина и норадреналина, а также их промежуточных и конечных метаболитов.
-Вненадпочечниковые опухоли (параганглиома, ганглионеврома, нейробластома и др.):повышается обычно только содержание норадреналина, норметанефрина.
Исследование уровня катехоламинов в динамике позволяет не только диагностировать феохромацитому, но и осуществлять контроль эффективности проводимой терапии:
-Радикальное удаление опухоли: всегда сопровождается быстрой нормализацией показателей,
-Рецидивирование процесса: приводит к повторному подъему концентрации катехоламинов в крови.
При исследовании катехоламинов информативным является не только определение их уровня в плазме крови, но и экскреция с мочой, а также определение в моче метаболитов катехоламинов. Однако необходимо отметить, что каждый из методов имеет свои недостатки:
Например, в крови происходит достаточно быстрая элиминация катехоламинов, и в идеале взятие крови для данного исследования следует производить в момент ярких клинических проявлений (гипертонический криз и др.), что на практике не всегда осуществимо.
Определение катехоламинов и их метаболитов в моче может быть не достаточно информативно, если у пациента наблюдается нарушении функции почек.
Поэтомунаиболее оптимальным является исследование адреналина, норадреналина и их промежуточных метаболитов (метанефрин, норметанефрин) в крови с одновременным определением экскреции катехоламинов и их конечных метаболитов (VМА)в моче.
Диагностическое значение уровня серотонина в онкологии:
Около 90% серотонина синтезируется и хранится в энтерохромаффинных клетках желудочно-кишечного тракта, откуда поступает в кровь и адсорбируется тромбоцитами, вызывая их агрегацию. Серотонин оказывает существенное влияние на эндокринную систему, воздействуя как на синтез гипоталамических факторов, так и на функционирование периферических желез внутренней секреции.
В клинической практике:
Определение уровня серотонина в крови наиболее информативно при злокачественных новообразованиях желудка, кишечника и легких, при которых данный показатель превышает норму в 5-10 раз. При этом в моче выявляется повышенное содержание продуктов метаболизма серотонина. После радикального оперативного лечения опухоли: происходит полная нормализация этих показателей, в связи с чем исследование уровня серотонина в крови и в суточной моче в динамике позволяет оценить эффективность проведенной терапии.
Рецидив процесса или метастазирование: повторное повышение уровня серотонина в крови и выделения метаболитов с мочой. Серотонин и 5-HIАА являются маркерами злокачественности.
Другими возможными причинами увеличения концентрации серотонина в крови и в моче являются медуллярный рак щитовидной железы, острая кишечная непроходимость, демпинг-синдром, муковисцедоз, острый инфаркт миокарда.
Кардиология.
Артериальная гипертензия.
Симпатическая часть ВНС является важнейшей системой регуляции системного артериального давления. Относится к кратковременным механизмам регуляции давления крови. Важность ВНС также определяется тем, что она влияет сразу на 2 параметра, определяющих величину АД – силу сердечных сокращений, то есть насосную функцию сердца, и тонус резистивных периферических сосудов.
Физиологическая действие катехоламинов на сердечно-сосудистую систему.
Основные причины повышения уровня адреналина и нор-адреналина |
Основные причины снижения уровня адреналина и нор-адреналина |
||
в крови |
в моче |
в крови |
в моче |
феохромацитома; -гипертонический криз; -стрессы; -нейробластома; -ганглионеврома; -гипогликемия; -острый инфаркт миокарда; -прием кофеина, этанола, теофиллина, резерпина, введение инсулина, кортизона |
-феохромацитома -гипертонические кризы, кроме диэнцефальных; — нейро- и ганглионейробластома; -длительные маниакально -депрессивные состояния; -острый период инфаркта миокарда; -любые заболевания, протекающие с выраженным болевым синдромом; -стрессы; -после введения инсулина, АКТГ, кортизона; |
— терапия клонидином. Недостаточная секреция адреналина и норадреналина как самостоятельная эндокринная патология не встречается. |
-вегетативные нейропатии, в том числе диабетическая; — паркинсонизм; -коллагенозы; -острые лейкозы (особенно у детей вследствие дегенерации хромаффинной ткани); -гипертонические кризы,связанные с поражением диэнцэфальной области; |
Диагностическое значение уровня катехоламинов и их метаболитов.Неадекватные длительные гиперкатехоламинемия или гипокатехоламинемия, обусловленные нарушением синтеза, секреции, инактивации или выведения катехоламинов, а также изменение чувствительности адренорецепторов тканей к отдельным катехоламинам ведут к нарушению физиологического баланса формирующих артериальное давление факторов, развитию стойких патологических гипер- или гипотензивных состояний.
Особенно опасны длительные гиперкатехоламинемии, в результате повышенной продукции или активности (например, вследствие генетического дефекта рецепторного аппарата) катехоламинов развивается стойкая артериальная гипертензия, характеризующаяся кризовым течением, гипертрофия миокарда с последующей миогенной дилатацией. Причинами этих патологических состояний:
Катехоламины стимулируют спазм подкожных и висцеральных сосудов, слизистых оболочек и почек путем взаимодействия с a-адренорецепторами, тем самым повышается общее периферическое сопротивление (ОПС)
Воздействия катехоламинов на сердечную мышцу (опосредовано через b1-адренорецепторы) приводит к увеличению частоты сердечных сокращений, усилению сократимости миокарда и увеличению скорости проведения возбуждения.
Катехоламины увеличивают также минутный объем сердца путем стимулирования веноконстрикции, увеличения венозного возврата и силы сокращения предсердий, тем самым вызывая увеличение диастолического объема, а следовательно, и длины волокон.
При повышении артериального давления в системе приносящих артерий почек меняется фильтрационная способность клубочков, запускается механизм ренин-ангиотензин-альдостероновой системы (РААС), в результате увеличивается объём циркулирующей крови, также один из продуктов (ангиотензин II) оказывает прямое вазоконстрикторное действие.
Психоневрология.
Моноамины и индолилалкиламины – очень важный класс нейромодуляторов.
Дофамин — тормозной модулятор, снижающий эффекты возбуждающего медиатора ацетилхолина. способствует как повышенному настроению и эмоциональному удовлетворению, так и нестандартной активности головного мозга (в том числе, вероятно, и творческой).
Норадреналин — вызывает накопление в клетке ионов Са 2+ (через α1-адренорецепторы) и цАМФ (через β-адренорецепторы). Активируется ретикулярная формация ствола, что тонизирует головной мозг, включая кору больших полушарий. Это стимулирует память, целесообразное поведение, эмоции и мышление. Введение веществ, которые уменьшают накопление КА в нервных клетках (резерпин), резко снижает активность мозга. Норадреналин выделяется из симпатических нервных окончаний в синапс и затем в кровь при гневе, ярости, психологической мобилизации
Серотонин — снижает агрессивность, страх, депрессию, стимулирует пищевое поведение, сон, увеличивает пищевые и снижает болевые условные рефлексы, способствует обучению и лидерству.
Паркинсонизм, экстрапирамидные гиперкинезы:
Паркинсонизм (болезнь Паркинсона) — хронический прогрессирующий нейродегеративный синдром, характеризующийся двигательными расстройствами, такими, как гипокинезия, тремор и ригидность мышц; нарушениями вегетативной регуляции и умственной деятельности вследствие поражений экстрапирамидной системы. Частота заболевания паркинсонизмом повышается с возрастом.
В современных представлениях о патофизиологии паркинсонизма:
nглавная роль отводится дегенерации дофаминергических нейронов компактной зоны черной субстанции,
nв меньшей степени – норадренергических нейронов голубого пятна.
Компактная зона черной субстанции посылает свои проекции в стриатум, который является интегральным центром стереотипического двигательного рефлекса мышц и регулирует движение, тонус мышц и ходьбу. Дофамин является первичным тормозным нейромедиатором в стриатуме. Изменение концентрации дофамина оказывает функциональные эффекты на другие медиаторы.
Диагностика паркинсонизма:
Определение содержания основного метаболита дофамина — гомованиллиновой кислоты (НVА).При паркинсонизме существенно снижается.
При экстрапирамидных гиперкинезах определение основных метаболитов дофамина и норадреналина гомованиллиновой кислоты (НVА) и ваниллилминдальной кислоты (VМА), промежуточного метаболита норадреналина- норметанефрина.
Депрессивные состояния.
Депрессии, согласно данным ВОЗ, в настоящий момент являются одним из наиболее распространённых психопатологических нарушений. Клиническая картина депрессивного синдрома характеризуется основной триадой симптомов: известной уже много лет: пониженное, подавленное настроение, идеаторная и моторная заторможенность.
Генез аффективных расстройствобусловлен патологическим функционированием структур мозга, в частности лимбико-таламической и гипоталамо-гипофизарной. При этом лимбическая система является основным координатором, образующим интегративную цепь, через которую кортикальные центры регуляции эмоций посылают импульсы к гипоталамусу, а гипоталамические импульсы передаются гиппокампу.
Одним из ведущих нейрохимических механизмов формирования депрессий является истощение катехоламиновой нейротрансмиттерной системы. Кроме того, формирование аффективных расстройств обусловлено дисбалансом (гипо-, гипер- или дисфункция) взаимодействий между норадренергической, серотонинергической, а также пептидергической системами.
Диагностическое значение для выявления причин развития депрессивного состояния, а также оценки проводимой терапии имеют метаболиты катехоламинов и серотонина:
VМА (ванилилминдальная кислота)основной метаболит адреналина и норадреналина
5-НIАА (5-гидроксииндолуксусная кислота)- основной метаболит серотонина
Уровень серотонина в плазме кровиможет предоставить достоверную информацию относительно уровня активного трансмиттера в синоптической щели центральных синапсов .
Важно отметить, что лечение антидепрессантами и нейролептиками должно проводиться под контролем врача и согласно особенностям каждого конкретного организма. Поэтому необходимо качественно выявить патогенетический вариант и проводить терапевтический лекарственный мониторинг.
Эпилепсия, эпилептический синдром.
Повторные судорожные (чаще) или бессудорожные припадки, возникающие при активно текущих церебральных патологических процессах (опухоль, черепно-мозговая травма, нейроинфекция, патология сосудов, нарушение метаболизма и др.) или при выраженных их последствиях. Припадки обычно прекращаются после устранения неврологической патологии.
nВ процессе центральной нервной регуляции вегетативных функций большое значение приобретает степень участия катехоламинов и серотонина. Являясь одновременно гормонами и медиаторами симпатико-адреналовой системы, катехоламины участвуют в развитии приспособительных реакций организма.
nСуществует некоторая связь между характером судорожного припадка и уровнем экскреции катехоламинов в моче. Обычно большому судорожному припадку предшествует (за сутки) повышенная экскреция норадреналина, его метаболита. При частых больших судорожных припадках отмечается снижение экскреции катехоламинов, что свидетельствует о некотором функциональном истощении симпатико-адреналовой системы.
Диагностическое значение имеет определение уровня катехоламинов, серотонина и их метаболитов в моче.
Шизофрения.
Шизофрения — это болезнь головного мозга, которая нарушает способность человека правильно мыслить, контролировать свои эмоции, принимать решения и общаться с другими людьми.
Среди биологических теорий шизофрении в настоящее время наиболее широкое распространение получили нейротрансмиттерные, особенно дофаминовая.
Дофаминовая теория: при этом заболевании имеет место повышение активности дофаминовой системы мозга с увеличением выделения дофамина, усилением дофаминовой нейротрансмиссии и гиперчувствительностью дофаминовых рецепторов, т. е. предполагается, что дофаминовые нейроны находятся в гиперактивном состоянии.
Серотониновая теория: развитие шизофрении обусловлено недостаточностью серотонинергической нейротрансмиссии. Эта гипотеза родилась на основе наблюдений за психотомиметическим действием диэтиламида лизергиновой кислоты (ЛСД), который является блокатором серотониновых рецепторов.
Норадренергическая гипотеза: воснове шизофрении лежит дегенерация норадренергических нейронов. На появление этой гипотезы в определенной мере повлияли наблюдения за эффектами 6-оксидофамина, который как нейротоксин избирательно поражает норадренергические нейроны. Дефицит норадренергической нейротрансмиссии может объяснить не только возникновение симптомов острой шизофрении, но и развитие дефектных состояний и негативных проявлений болезни (потерю энергетического потенциала, ангедонию и др.).
Наркотическая и алкогольная зависимость.
При первичных пробах наркотических веществ происходит активация системы положительного подкрепления, которая, в первую очередь, проявляется в быстрых рецепторных и метаболических изменениях, в основном в системах моноаминов и опиоидов. По-видимому, эти изменения и приводят к формированию патологического влечения.
При длительном употреблении наркотиков может развиться дефицит нейромедиаторов, сам по себе угрожающий жизнедеятельности организма. В качестве механизма компенсации этого явления выступают усиленный синтез катехоламинов и подавление активности ферментов их метаболизма, в первую очередь моноаминоксидазы и дофамин-b-гидроксилазы, контролирующих превращение дофамина в норадреналин. Таким образом, стимулируемый очередным приемом наркотиков выброс катехоламинов и их ускоренное, избыточное разрушение сочетаются с компенсаторно-усиленным синтезом этих нейромедиаторов. Формируется ускоренный кругооборот катехоламинов. Теперь при прекращении приема наркотика, т.е. при абстиненции, усиленного высвобождения катехоламинов из депо не происходит, но сохраняется их ускоренный синтез. Вследствие изменения активности ферментов в биологических жидкостях и тканях (главным образом в мозге) накапливается дофамин. Именно этот процесс обусловливает развитие основных клинических признаков абстинентного синдрома — высокой тревожности, напряженности, возбуждения, подъема артериального давления, учащения пульса, появления других вегетативных расстройств, нарушения сна и др. Иными словами, описанные выше изменения нейрохимических функций мозга формируют физическую зависимость от наркотических препаратов.
Уровень дофамина в крови четко коррелирует с клинической тяжестью абстинентного синдрома:в начальном ее периоде он несколько повышен, затем, как правило, опускается ниже нормы. Очевидно, дефицит дофамина в структурах мозга, связанных с подкреплением, является основой остающегося патологического влечения к наркотикам и высокой вероятности рецидива заболевания.
Действие дофамина и серотонина связано с настроением, эмоциями, мотивациями, целенаправленным поведением, вниманием, процессом мышления перед тем, как что-то делать… Если обмен серотонина нарушен, изменен баланс серотонина и дофамина, все эти важнейшие психические функции пострадают, а организм начнет искать способ устранить неприятные ощущения: возникнет тяга к алкоголю, наркотикам, сладостям, сигаретам… Разными биохимическими путями никотин, наркотики, алкоголь, глюкоза могут на время снизить или даже полностью компенсировать эмоциональное напряжение, плохое настроение, отвлечь от ощущения невозможности достичь какой-то цели; и здоровые люди на себе это испытывали.
У пациентов с наркотической и алкогольной зависимостью:
Выявлено повышенное значение метаболитов катехоламинов HVAи VMA
Выявлено сниженное значение концентрации 5-HIAA